2026年一本密卷高考化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年一本密卷高考化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第49页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
1. (2025·湖北黄冈·三模)春节是中华民族的传统节日,在进行节日庆祝时用到了许多物品都与化学知识相关,下列有关说法错误的是(

A.A
B.B
C.C
D.D
C
)
A.A
B.B
C.C
D.D
答案:
1.[答案] C
[解析] A.糯米年糕中含有支链淀粉,在糊化时能形成凝胶,故A正确;B.激发态能量大于基态,金属元素原子的电子从激发态跃迁回基态并释放能量,故B正确;C.陶器烧制的温度通常在950~1165℃之间,而瓷器的烧制温度一般都在1280~1400℃以上,因此瓷器需要的烧制温度比陶器高,故C错误;D.鞣酸亚铁中(Fe²⁺)被氧化为黑色沉淀鞣酸铁(Fe³⁺),铁含量直接影响最终产物的浓度,铁含量越大颜色越深,故D正确;故答案为C。
[解析] A.糯米年糕中含有支链淀粉,在糊化时能形成凝胶,故A正确;B.激发态能量大于基态,金属元素原子的电子从激发态跃迁回基态并释放能量,故B正确;C.陶器烧制的温度通常在950~1165℃之间,而瓷器的烧制温度一般都在1280~1400℃以上,因此瓷器需要的烧制温度比陶器高,故C错误;D.鞣酸亚铁中(Fe²⁺)被氧化为黑色沉淀鞣酸铁(Fe³⁺),铁含量直接影响最终产物的浓度,铁含量越大颜色越深,故D正确;故答案为C。
2. (2025·江西上饶·二模)下列化学用语使用正确的是(
A.基态硫原子的价层电子轨道表示式: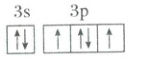
B.MgCl₂的电子式:Mg²⁺[:$\ddot{Cl}$:]₂⁻
C.H₂O₂的空间填充模型:
D.氨水中NH₃与H₂O分子间氢键主要形式可表示为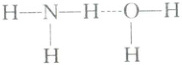
A
)A.基态硫原子的价层电子轨道表示式:

B.MgCl₂的电子式:Mg²⁺[:$\ddot{Cl}$:]₂⁻
C.H₂O₂的空间填充模型:

D.氨水中NH₃与H₂O分子间氢键主要形式可表示为
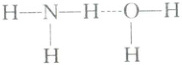
答案:
2.[答案] A
[解析] A.基态硫原子价层电子为3s²3p⁴,价层电子轨道表示式,故A正确;B.MgCl₂是离子化合物,电子式为[:Cl:]⁻Mg²⁺[:Cl:]⁻,故B错误;C.H₂O₂的空间构型是二面角结构,故C错误;D.氨水中NH₃与H₂O分子间氢键主要形式可表示为 ,故D错误;故选A。
,故D错误;故选A。
2.[答案] A
[解析] A.基态硫原子价层电子为3s²3p⁴,价层电子轨道表示式,故A正确;B.MgCl₂是离子化合物,电子式为[:Cl:]⁻Mg²⁺[:Cl:]⁻,故B错误;C.H₂O₂的空间构型是二面角结构,故C错误;D.氨水中NH₃与H₂O分子间氢键主要形式可表示为
 ,故D错误;故选A。
,故D错误;故选A。 3. (2025·山东·三模)化学品在造纸工业中有着重要的应用。下列说法错误的是(
A.碳酸钠用作纸浆抗氧化剂
B.双氧水用作纸浆漂白剂
C.氢氧化钠用于脱除木质素
D.氧化铁红用作纸张染色剂
A
)A.碳酸钠用作纸浆抗氧化剂
B.双氧水用作纸浆漂白剂
C.氢氧化钠用于脱除木质素
D.氧化铁红用作纸张染色剂
答案:
3.[答案] A
[解析] A.碳酸钠是强碱弱酸盐,主要用作调节pH或软化水,而非抗氧化剂(抗氧化剂需具备还原性),A错误;B.双氧水具有强氧化性、漂白性,可氧化纸浆中的有色物质,实现漂白作用,B正确;C.氢氧化钠在制浆过程中用于溶解木质素(如硫酸盐法),从而分离纤维素,C正确;D.氧化铁红(Fe₂O₃)是红色颜料,可用于纸张染色,D正确;故选A。
[解析] A.碳酸钠是强碱弱酸盐,主要用作调节pH或软化水,而非抗氧化剂(抗氧化剂需具备还原性),A错误;B.双氧水具有强氧化性、漂白性,可氧化纸浆中的有色物质,实现漂白作用,B正确;C.氢氧化钠在制浆过程中用于溶解木质素(如硫酸盐法),从而分离纤维素,C正确;D.氧化铁红(Fe₂O₃)是红色颜料,可用于纸张染色,D正确;故选A。
4. (2025·河南开封·二模)硫及其化合物部分转化关系如图所示。设Nₐ为阿伏加德罗常数的值。下列说法正确的是(
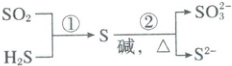
A.100 mL 0.1 mol·L⁻¹ Na₂S溶液中S²⁻数目为0.01Nₐ
B.反应①每消耗3.4 g H₂S,生成物中硫原子数目为0.15Nₐ
C.反应②每生成1 mol氧化产物,转移电子数目为2Nₐ
D.32 g S₈与足量的H₂完全反应生成H₂S,断裂的S—S键数目为2Nₐ
B
)
A.100 mL 0.1 mol·L⁻¹ Na₂S溶液中S²⁻数目为0.01Nₐ
B.反应①每消耗3.4 g H₂S,生成物中硫原子数目为0.15Nₐ
C.反应②每生成1 mol氧化产物,转移电子数目为2Nₐ
D.32 g S₈与足量的H₂完全反应生成H₂S,断裂的S—S键数目为2Nₐ
答案:
4.[答案] B
[解析] A.Na₂S为强碱弱酸盐,溶液中存在水解,导致该溶液中S²⁻数目小于0.01Nₐ,A错误;B.反应①方程式:2H₂S + SO₂ = 3S↓ + 2H₂O,每消耗3.4gH₂S,对应物质的量为0.1mol,生成硫原子数目为0.15Nₐ,B正确;C.反应②为S在碱性条件下的歧化反应,部分S元素化合价从0价升至+4价,发生氧化反应,生成氧化产物,每生成1mol氧化产物,转移电子数目为4Nₐ,C错误;D.S₈分子为环状结构,每个S₈分子含8个S—S键。32gS₈的物质的量为32g÷(32×8)g/mol = 0.125mol,与H₂反应时需断裂全部S—S键,断裂的S—S键数目为0.125mol×8 = 1mol,即Nₐ,D错误;答案选B。
[解析] A.Na₂S为强碱弱酸盐,溶液中存在水解,导致该溶液中S²⁻数目小于0.01Nₐ,A错误;B.反应①方程式:2H₂S + SO₂ = 3S↓ + 2H₂O,每消耗3.4gH₂S,对应物质的量为0.1mol,生成硫原子数目为0.15Nₐ,B正确;C.反应②为S在碱性条件下的歧化反应,部分S元素化合价从0价升至+4价,发生氧化反应,生成氧化产物,每生成1mol氧化产物,转移电子数目为4Nₐ,C错误;D.S₈分子为环状结构,每个S₈分子含8个S—S键。32gS₈的物质的量为32g÷(32×8)g/mol = 0.125mol,与H₂反应时需断裂全部S—S键,断裂的S—S键数目为0.125mol×8 = 1mol,即Nₐ,D错误;答案选B。
查看更多完整答案,请扫码查看


