2026年一本密卷高考化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年一本密卷高考化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第4页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
13. 草酸广泛应用于食品、药品等领域。常温下,通过下列实验探究了草酸的性质:
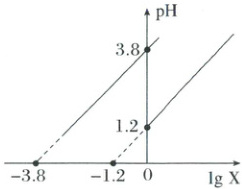
实验1:向$10mL0.2mol·L^{-1}H_2C_2O_4$溶液中滴入一定量$0.2mol·L^{-1}KOH$溶液。混合溶液的$pH$与$lgX[X = \frac{c(HC_2O_4^-)}{c(H_2C_2O_4)}$或$\frac{c(C_2O_4^{2-})}{c(HC_2O_4^-)}]$的关系如图所示。
实验2:向$10mL0.2mol·L^{-1}H_2C_2O_4$溶液中加入$10mL0.2mol·L^{-1}BaCl_2$溶液。
已知:$25℃$时,$K_{sp}(BaC_2O_4) = 10^{-7.6}$。混合后溶液体积变化忽略不计。
下列说法错误的是()
A.实验1,当溶液中$c(H_2C_2O_4) = c(C_2O_4^{2-})$时,$pH = 2.5$
B.实验1,当溶液呈中性时:$c(C_2O_4^{2-}) > c(HC_2O_4^-) > c(H_2C_2O_4)$
C.实验2,溶液中有沉淀生成
D.实验2,溶液中存在:$2c(Ba^{2+}) + c(H^+) = c(Cl^-) + c(HC_2O_4^-) + 2c(C_2O_4^{2-})$

实验1:向$10mL0.2mol·L^{-1}H_2C_2O_4$溶液中滴入一定量$0.2mol·L^{-1}KOH$溶液。混合溶液的$pH$与$lgX[X = \frac{c(HC_2O_4^-)}{c(H_2C_2O_4)}$或$\frac{c(C_2O_4^{2-})}{c(HC_2O_4^-)}]$的关系如图所示。
实验2:向$10mL0.2mol·L^{-1}H_2C_2O_4$溶液中加入$10mL0.2mol·L^{-1}BaCl_2$溶液。
已知:$25℃$时,$K_{sp}(BaC_2O_4) = 10^{-7.6}$。混合后溶液体积变化忽略不计。
下列说法错误的是()
A.实验1,当溶液中$c(H_2C_2O_4) = c(C_2O_4^{2-})$时,$pH = 2.5$
B.实验1,当溶液呈中性时:$c(C_2O_4^{2-}) > c(HC_2O_4^-) > c(H_2C_2O_4)$
C.实验2,溶液中有沉淀生成
D.实验2,溶液中存在:$2c(Ba^{2+}) + c(H^+) = c(Cl^-) + c(HC_2O_4^-) + 2c(C_2O_4^{2-})$
答案:
13.[答案] D
[分析] K_a1 = c(HC₂O₄⁻)c(H⁺)/c(H₂C₂O₄)、K_a2 = c(C₂O₄²⁻)c(H⁺)/c(HC₂O₄⁻),根据K_a1 > K_a2可知,当lgX = 0时,K_a1对应的c(H⁺)大,pH数值小,因此K_a1 = c(HC₂O₄⁻)c(H⁺)/c(H₂C₂O₄)=10⁻¹·²,K_a2 = c(C₂O₄²⁻)c(H⁺)/c(HC₂O₄⁻)=10⁻³·⁸,以此解题。
[解析] A.K_a1×K_a2 = c(HC₂O₄⁻)c(H⁺)/c(H₂C₂O₄)× c(C₂O₄²⁻)c(H⁺)/c(HC₂O₄⁻) = c(C₂O₄²⁻)c²(H⁺)/c(H₂C₂O₄) = 10⁻⁵·⁰,当溶液中c(H₂C₂O₄)=c(C₂O₄²⁻)时,c(H⁺)=10⁻²·⁵mol/L,pH = 2.5,A正确;B.当溶液呈中性时,c(H⁺)=10⁻⁷mol/L,由两步电离平衡常数可知,c(HC₂O₄⁻)/c(H₂C₂O₄) = 10⁻¹·²/10⁻⁷ > 1,c(HC₂O₄⁻)>c(H₂C₂O₄),同理:c(C₂O₄²⁻)/c(HC₂O₄⁻) = 10⁻³·⁸/10⁻⁷ > 1,c(C₂O₄²⁻)>c(HC₂O₄⁻),B正确;C.实验2的离子方程式:H₂C₂O₄(aq) + Ba²⁺(aq)⇌ BaC₂O₄(s) + 2H⁺(aq),平衡常数:K = c²(H⁺)/c(Ba²⁺)×c(H₂C₂O₄)= c(H⁺)c(HC₂O₄⁻)×c(H⁺)c(C₂O₄²⁻)/c(Ba²⁺)×c(C₂O₄²⁻)×c(HC₂O₄⁻)×c(H₂C₂O₄)= K_a1×K_a2/K_sp(BaC₂O₄) = 10⁻⁵/10⁻⁷·⁶ = 10²·⁶,平衡常数较大,该反应进行的程度较大,判断可产生沉淀;或进行定量计算,两步电离平衡反应式相加,得到H₂C₂O₄⇌ 2H⁺ + C₂O₄²⁻,K = 10⁻⁵·⁰,二者等体积混合,c(H₂C₂O₄)=0.1mol/L,列三段式:
H₂C₂O₄⇌ 2H⁺ + C₂O₄²⁻
始mol/L 0.1 0 0
变mol/L x 2x x
平mol/L 0.1 - x 2x x
则4x³/(0.1 - x) = 10⁻⁵·⁰,估算x的数量级为10⁻³,故Q = c(Ba²⁺)×c(C₂O₄²⁻)≈0.1×10⁻³ = 10⁻⁴ > K_sp(BaC₂O₄)=10⁻⁷·⁶,故有沉淀生成,C正确;D.电荷守恒中右侧缺少了OH⁻的浓度项,D错误;故选D。
[分析] K_a1 = c(HC₂O₄⁻)c(H⁺)/c(H₂C₂O₄)、K_a2 = c(C₂O₄²⁻)c(H⁺)/c(HC₂O₄⁻),根据K_a1 > K_a2可知,当lgX = 0时,K_a1对应的c(H⁺)大,pH数值小,因此K_a1 = c(HC₂O₄⁻)c(H⁺)/c(H₂C₂O₄)=10⁻¹·²,K_a2 = c(C₂O₄²⁻)c(H⁺)/c(HC₂O₄⁻)=10⁻³·⁸,以此解题。
[解析] A.K_a1×K_a2 = c(HC₂O₄⁻)c(H⁺)/c(H₂C₂O₄)× c(C₂O₄²⁻)c(H⁺)/c(HC₂O₄⁻) = c(C₂O₄²⁻)c²(H⁺)/c(H₂C₂O₄) = 10⁻⁵·⁰,当溶液中c(H₂C₂O₄)=c(C₂O₄²⁻)时,c(H⁺)=10⁻²·⁵mol/L,pH = 2.5,A正确;B.当溶液呈中性时,c(H⁺)=10⁻⁷mol/L,由两步电离平衡常数可知,c(HC₂O₄⁻)/c(H₂C₂O₄) = 10⁻¹·²/10⁻⁷ > 1,c(HC₂O₄⁻)>c(H₂C₂O₄),同理:c(C₂O₄²⁻)/c(HC₂O₄⁻) = 10⁻³·⁸/10⁻⁷ > 1,c(C₂O₄²⁻)>c(HC₂O₄⁻),B正确;C.实验2的离子方程式:H₂C₂O₄(aq) + Ba²⁺(aq)⇌ BaC₂O₄(s) + 2H⁺(aq),平衡常数:K = c²(H⁺)/c(Ba²⁺)×c(H₂C₂O₄)= c(H⁺)c(HC₂O₄⁻)×c(H⁺)c(C₂O₄²⁻)/c(Ba²⁺)×c(C₂O₄²⁻)×c(HC₂O₄⁻)×c(H₂C₂O₄)= K_a1×K_a2/K_sp(BaC₂O₄) = 10⁻⁵/10⁻⁷·⁶ = 10²·⁶,平衡常数较大,该反应进行的程度较大,判断可产生沉淀;或进行定量计算,两步电离平衡反应式相加,得到H₂C₂O₄⇌ 2H⁺ + C₂O₄²⁻,K = 10⁻⁵·⁰,二者等体积混合,c(H₂C₂O₄)=0.1mol/L,列三段式:
H₂C₂O₄⇌ 2H⁺ + C₂O₄²⁻
始mol/L 0.1 0 0
变mol/L x 2x x
平mol/L 0.1 - x 2x x
则4x³/(0.1 - x) = 10⁻⁵·⁰,估算x的数量级为10⁻³,故Q = c(Ba²⁺)×c(C₂O₄²⁻)≈0.1×10⁻³ = 10⁻⁴ > K_sp(BaC₂O₄)=10⁻⁷·⁶,故有沉淀生成,C正确;D.电荷守恒中右侧缺少了OH⁻的浓度项,D错误;故选D。
14. 环氧化合物是重要的有机合成中间体。以钛掺杂沸石为催化剂,由丙烯( )为原料生产环氧丙烷( )的反应机理如图所示。下列说法正确的是( )
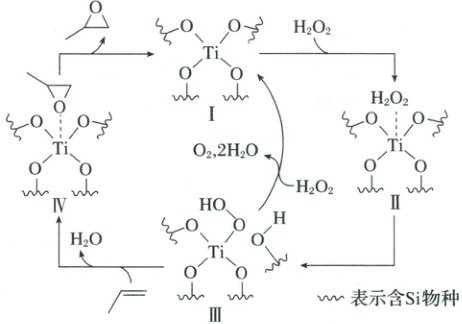
A.过程中Ⅱ是催化剂
B.过程中有极性键和非极性键的断裂和形成
C.过程中$Ti$元素的化合价发生了变化
D.丙烯与双氧水反应生成环氧丙烷的原子利用率为$100\%$

A.过程中Ⅱ是催化剂
B.过程中有极性键和非极性键的断裂和形成
C.过程中$Ti$元素的化合价发生了变化
D.丙烯与双氧水反应生成环氧丙烷的原子利用率为$100\%$
答案:
14.[答案] B
[解析] A.根据反应原理,Ⅰ先消耗再生成,是整个历程的催化剂,Ⅱ先生成,再消耗,是中间产物,A错误;B.过程中存在H₂O₂中O—O非极性键的断裂,以及O₂中非极性键的形成;还存在O—H极性键的断裂,以及O—C极性键的形成,B正确;C.过程中Ti的化学键(Ti—O)始终是4个,配位键不会改变Ti的化合价,故Ti元素的化合价不变,C错误;D.反应生成了H₂O,且存在H₂O₂的分解反应,原子利用率小于100%,D错误;故选B。
[解析] A.根据反应原理,Ⅰ先消耗再生成,是整个历程的催化剂,Ⅱ先生成,再消耗,是中间产物,A错误;B.过程中存在H₂O₂中O—O非极性键的断裂,以及O₂中非极性键的形成;还存在O—H极性键的断裂,以及O—C极性键的形成,B正确;C.过程中Ti的化学键(Ti—O)始终是4个,配位键不会改变Ti的化合价,故Ti元素的化合价不变,C错误;D.反应生成了H₂O,且存在H₂O₂的分解反应,原子利用率小于100%,D错误;故选B。
15. (14分)苯胺是重要的有机化工原料,其实验室制备原理如下:
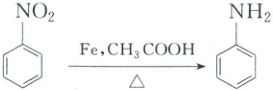
相关信息如下:
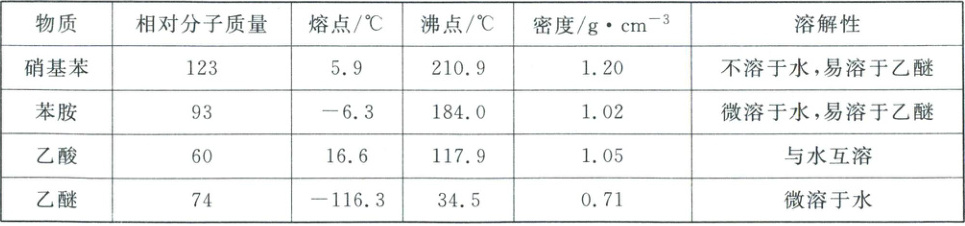
反应装置Ⅰ和蒸馏装置Ⅱ(加热、夹持等装置略)如下:

实验步骤为:
①向装置Ⅰ双颈烧瓶中加入$13.5g$铁粉、$25.0mL$水及$1.50mL$乙酸,加热煮沸$10min$;
②稍冷后,通过恒压滴液漏斗缓慢滴入$8.20mL$硝基苯($0.08mol$),再加热回流$30min$;
③将装置Ⅰ改成水蒸气蒸馏装置,蒸馏收集苯胺-水馏出液;
④将苯胺-水馏出液用$NaCl$饱和后,转入分液漏斗静置分层,分出有机层;水层用乙醚萃取,分出醚层;合并有机层和醚层,用粒状氢氧化钠干燥,得到苯胺醚溶液;
⑤将苯胺醚溶液加入圆底烧瓶(装置Ⅱ),先蒸馏回收乙醚,再蒸馏收集$180~185℃$馏分,得到$5.58g$苯胺。
回答下列问题:
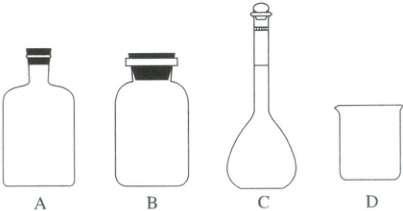
(1)实验室保存硝基苯的玻璃容器是
(2)装置Ⅰ中冷凝管的进水口为
(3)步骤④中将苯胺-水馏出液用$NaCl$饱和的原因是_。
(4)步骤④中第二次分液,醚层位于
(5)蒸馏回收乙醚时,锥形瓶需冰水浴的原因是
(6)下列说法正确的是
A. 缓慢滴加硝基苯是为了减小反应速率
B. 蒸馏时需加沸石,防止暴沸
C. 用红外光谱不能判断苯胺中是否含有硝基苯
D. 蒸馏回收乙醚,无需尾气处理
(7)苯胺的产率为

相关信息如下:

反应装置Ⅰ和蒸馏装置Ⅱ(加热、夹持等装置略)如下:

实验步骤为:
①向装置Ⅰ双颈烧瓶中加入$13.5g$铁粉、$25.0mL$水及$1.50mL$乙酸,加热煮沸$10min$;
②稍冷后,通过恒压滴液漏斗缓慢滴入$8.20mL$硝基苯($0.08mol$),再加热回流$30min$;
③将装置Ⅰ改成水蒸气蒸馏装置,蒸馏收集苯胺-水馏出液;
④将苯胺-水馏出液用$NaCl$饱和后,转入分液漏斗静置分层,分出有机层;水层用乙醚萃取,分出醚层;合并有机层和醚层,用粒状氢氧化钠干燥,得到苯胺醚溶液;
⑤将苯胺醚溶液加入圆底烧瓶(装置Ⅱ),先蒸馏回收乙醚,再蒸馏收集$180~185℃$馏分,得到$5.58g$苯胺。

回答下列问题:
(1)实验室保存硝基苯的玻璃容器是
A
(填标号)。(2)装置Ⅰ中冷凝管的进水口为
a
(填“a”或“b”)。(3)步骤④中将苯胺-水馏出液用$NaCl$饱和的原因是_。
(4)步骤④中第二次分液,醚层位于
上
层(填“上”或“下”)。(5)蒸馏回收乙醚时,锥形瓶需冰水浴的原因是
防止其挥发损失并提高冷凝效率
;回收乙醚后,需要放出冷凝管中的冷凝水再蒸馏,这样操作的原因是避免冷凝水残留影响后续高温蒸馏时冷凝管的效率或防止高温下冷凝管因温差过大破裂
。(6)下列说法正确的是
B
(填标号)。A. 缓慢滴加硝基苯是为了减小反应速率
B. 蒸馏时需加沸石,防止暴沸
C. 用红外光谱不能判断苯胺中是否含有硝基苯
D. 蒸馏回收乙醚,无需尾气处理
(7)苯胺的产率为
75%
。
答案:
15.
(1)A
(2)a
(3)利用盐析效应,加入NaCl可降低苯胺的溶解度,使其析出,提升产率
(4)上
(5)防止其挥发损失并提高冷凝效率 避免冷凝水残留影响后续高温蒸馏时冷凝管的效率或防止高温下冷凝管因温差过大破裂
(6)B
(7)75%
(1)A
(2)a
(3)利用盐析效应,加入NaCl可降低苯胺的溶解度,使其析出,提升产率
(4)上
(5)防止其挥发损失并提高冷凝效率 避免冷凝水残留影响后续高温蒸馏时冷凝管的效率或防止高温下冷凝管因温差过大破裂
(6)B
(7)75%
查看更多完整答案,请扫码查看


