2025年名校课堂九年级化学全一册鲁教版广西专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年名校课堂九年级化学全一册鲁教版广西专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第120页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
11. (2024·梧州二模)学习了常见的酸、碱后,同学们对碱的化学性质进行整理归纳,并进行以下实验活动:
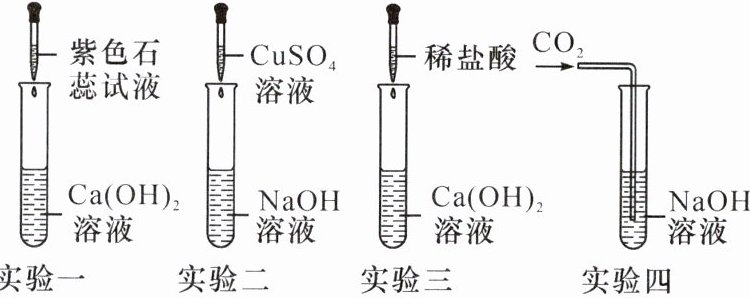
(1)实验一中紫色石蕊试液变蓝,说明Ca(OH)₂溶液显
(2)实验二反应的现象为
(3)同学们发现实验三、实验四无明显现象,无法确定是否发生了化学反应。于是继续进行探究。
Ⅰ. 取少量实验三中的溶液于试管中,滴加
Ⅱ. 取少量实验四中的溶液于试管中,滴加
(4)对于没有明显现象的化学反应,可以通过

(1)实验一中紫色石蕊试液变蓝,说明Ca(OH)₂溶液显
碱
性。(2)实验二反应的现象为
产生蓝色沉淀
。(3)同学们发现实验三、实验四无明显现象,无法确定是否发生了化学反应。于是继续进行探究。
Ⅰ. 取少量实验三中的溶液于试管中,滴加
无色酚酞试液
,溶液仍为无色,证明稀盐酸和Ca(OH)₂溶液发生了化学反应。Ⅱ. 取少量实验四中的溶液于试管中,滴加
稀盐酸
,观察到产生气泡,证CO₂和NaOH溶液发生了化学反应。(4)对于没有明显现象的化学反应,可以通过
证明反应物消失或者有新物质生成
的方法证明反应发生。
答案:
11.
(1)碱
(2)产生蓝色沉淀
(3)Ⅰ.无色酚酞试液 Ⅱ.稀盐酸
(4)证明反应物消失或者有新物质生成
(1)碱
(2)产生蓝色沉淀
(3)Ⅰ.无色酚酞试液 Ⅱ.稀盐酸
(4)证明反应物消失或者有新物质生成
12. (2024·贵港二模)阅读下列短文,回答相关问题。
人体的体液有一定的酸碱性,且其酸碱度保持在一个相对稳定的范围内,这样才能维持人体正常的生命活动。正常人体血浆pH为7.35~7.45,但CO₂扩散到血液中时会引起血浆pH略有改变。
人体胃液担负着食物的消化,胃液pH为0.9~1.5,20世纪初科学家在人体胃内发现了幽门螺杆菌,幽门螺杆菌能引起慢性胃炎,它主要是通过其产生的脲酶分解尿素产生氨而中和人体胃酸,导致人体胃内酸碱失衡,胃液分泌异常。
如图是一组胃病患者在空腹状态下24h胃液pH的变化曲线,科学家发现人体胃液的pH影响人体对药物的吸收,胃液pH低时,胃对弱酸性药物的吸收相对多;胃液pH高时,有利于弱碱性类药物的吸收。

(1)脲酶分解尿素反应的化学方程式为CO(NH₂)₂+H₂O=X+2NH₃↑,则X的化学式为
(2)分析上图,患者服用含氢氧化铝的胃药时,最适宜的用药时间约为
(3)下列说法不正确的是
A. 胃酸能帮助消化食物,胃酸分泌越多越有利于人体健康
B. 患者的用药时间也会影响药效
C. 胃液的酸性比血浆的酸性弱
人体的体液有一定的酸碱性,且其酸碱度保持在一个相对稳定的范围内,这样才能维持人体正常的生命活动。正常人体血浆pH为7.35~7.45,但CO₂扩散到血液中时会引起血浆pH略有改变。
人体胃液担负着食物的消化,胃液pH为0.9~1.5,20世纪初科学家在人体胃内发现了幽门螺杆菌,幽门螺杆菌能引起慢性胃炎,它主要是通过其产生的脲酶分解尿素产生氨而中和人体胃酸,导致人体胃内酸碱失衡,胃液分泌异常。
如图是一组胃病患者在空腹状态下24h胃液pH的变化曲线,科学家发现人体胃液的pH影响人体对药物的吸收,胃液pH低时,胃对弱酸性药物的吸收相对多;胃液pH高时,有利于弱碱性类药物的吸收。

(1)脲酶分解尿素反应的化学方程式为CO(NH₂)₂+H₂O=X+2NH₃↑,则X的化学式为
CO₂
。(2)分析上图,患者服用含氢氧化铝的胃药时,最适宜的用药时间约为
09:00
,反应的化学方程式为$\mathrm{Al(OH)_3+3HCl\xlongequal[]{}AlCl_3+3H_2O}$
。(3)下列说法不正确的是
AC
(填字母)。A. 胃酸能帮助消化食物,胃酸分泌越多越有利于人体健康
B. 患者的用药时间也会影响药效
C. 胃液的酸性比血浆的酸性弱
答案:
12.
(1)CO₂
(2)09:00 $\mathrm{Al(OH)_3+3HCl\xlongequal[]{}AlCl_3+3H_2O}$
(3)AC
(1)CO₂
(2)09:00 $\mathrm{Al(OH)_3+3HCl\xlongequal[]{}AlCl_3+3H_2O}$
(3)AC
13. (2022·梧州)实验室用质量分数为20.0%的稀硫酸处理含Ba(OH)₂的废液。向100.0g废液中加入稀硫酸至溶液恰好呈中性,最终得到2.33g沉淀。请计算:
(1)配制490.0g20.0%的稀硫酸需质量分数为98.0%的浓硫酸
(2)废液中Ba(OH)₂的质量分数。
(1)配制490.0g20.0%的稀硫酸需质量分数为98.0%的浓硫酸
100
g。(2)废液中Ba(OH)₂的质量分数。
答案:
13.
(1)100
(2)解:设废液中氢氧化钡的质量为x。$ Ba(OH)₂+H₂SO₄=\!=\!=BaSO₄↓+2H₂O 171 233 x 2.33 g \frac{171}{233}=\frac{x}{2.33 g} x=1.71 g $废液中Ba(OH)₂的质量分数为$\frac{1.71 g}{100 g}×100\%=1.71\% $答:废液中Ba(OH)₂的质量分数为1.71\%。
(1)100
(2)解:设废液中氢氧化钡的质量为x。$ Ba(OH)₂+H₂SO₄=\!=\!=BaSO₄↓+2H₂O 171 233 x 2.33 g \frac{171}{233}=\frac{x}{2.33 g} x=1.71 g $废液中Ba(OH)₂的质量分数为$\frac{1.71 g}{100 g}×100\%=1.71\% $答:废液中Ba(OH)₂的质量分数为1.71\%。
查看更多完整答案,请扫码查看


