第83页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
1.(2023·湖北武汉)某管道疏通剂标签上的部分文字如图所示。下列说法正确的是 (
A. 氢氧化钠中阴离子的符号为OH-2
B. 氢氧化钠中含有一种金属元素
C. 铝原子的结构示意图为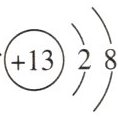
D. 硝酸钠的化学式为NO3Na

B
)A. 氢氧化钠中阴离子的符号为OH-2
B. 氢氧化钠中含有一种金属元素
C. 铝原子的结构示意图为

D. 硝酸钠的化学式为NO3Na

答案:
B
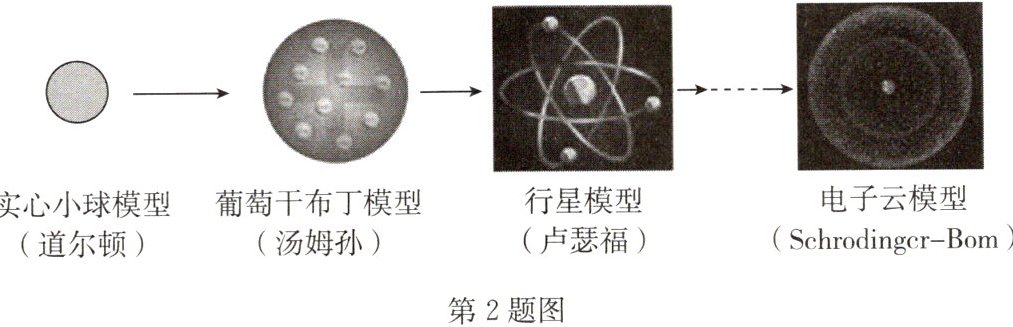
2.(2024·山东济南一模)人类不同阶段认识原子的模型示意图如图,其中卢瑟福的“α粒子轰击金箔”实验对认识原子起到了关键作用。结合你所学的知识判断,下列有关说法中,不正确的是 (
A. 汤姆孙发现了电子,推翻了道尔顿原子不可再分的认识
B. “α粒子轰击金箔”实验证实相对于整个原子而言,原子核的质量和体积都很小
C. “α粒子轰击金箔”实验证实原子内的正电荷集中在居于原子中心的原子核上
D. 电子云模型形象说明电子在原子核外作无规则的高速运动
B
)A. 汤姆孙发现了电子,推翻了道尔顿原子不可再分的认识
B. “α粒子轰击金箔”实验证实相对于整个原子而言,原子核的质量和体积都很小
C. “α粒子轰击金箔”实验证实原子内的正电荷集中在居于原子中心的原子核上
D. 电子云模型形象说明电子在原子核外作无规则的高速运动

答案:
B 点拨:汤姆孙通过实验发现了电子,提出“葡萄干布丁”模型,推翻了道尔顿原子不可再分的认识,故A选项说法正确;卢瑟福的“α粒子轰击金箔”实验中,有极少数α粒子被反弹了回来,证实了原子内的正电荷集中在居于原子中心的原子核上,相对于整个原子而言,原子核的质量大,但体积却很小,故B选项说法错误;卢瑟福的“α粒子轰击金箔”实验中,有极少数α粒子被反弹了回来,证实了原子内的正电荷集中在居于原子中心的原子核上,故C选项说法正确;现代科学家们在实验中发现电子在原子核周围像“云雾”一样,并没有固定的运动轨迹,电子云模型形象说明电子在原子核外作无规则的高速运动,故D选项说法正确。故本题选B。
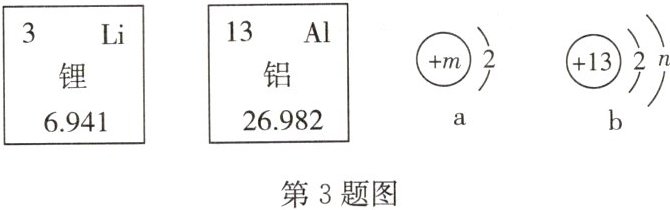
3.(2023·内蒙古呼和浩特)2023年5月底,国产飞机C919顺利完成商业首飞,C919客机机身材料大量使用了第三代铝锂合金。如图为锂和铝两种元素在元素周期表中的信息及相关的离子结构示意图。以下说法不正确的是 (
A. m=3,n=8
B. 氧化锂的化学式为LiO
C. 图b表示铝离子,离子符号为Al3+
D. 图中两种元素的本质区别是核内质子数不同
B
)A. m=3,n=8
B. 氧化锂的化学式为LiO
C. 图b表示铝离子,离子符号为Al3+
D. 图中两种元素的本质区别是核内质子数不同

答案:
B 点拨:根据锂元素在周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为3;根据原子中原子序数=核电荷数=质子数,则m=3;同样根据铝元素在周期表中的一格可知,该元素的原子核外电子数为13,核外有3个电子层,第一层上有2个电子,第二层上有8个电子,最外层上有3个电子,在化学反应中易失去3个电子而形成阳离子,则n=8,故A选项说法正确;根据锂元素在周期表中的一格可知,该元素的原子序数为3,则锂原子的核外电子数为3,核外有2个电子层,第一层上有2个电子,第二层上有1个电子,在化学反应中易失去1个电子而形成带1个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为+1价,氧元素显-2价,氧化锂的化学式为Li₂O,故B选项说法错误;n=8,图b表示铝离子,质子数=13,核外电子数=10,质子数>核外电子数,为带3个单位正电荷的铝离子,其离子符号为Al³⁺,故C选项说法正确;元素是质子数(即核电荷数)相同的一类原子的总称,图中两种元素的本质区别是核内质子数不同,故D选项说法正确。故本题选B。
查看更多完整答案,请扫码查看


