第79页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
13. A 标出下列化学式中画线元素的化合价。
$\underline{Cl}_2$ NaCl$\underline{Cl}$O₂ K$\underline{Cl}$O₃ K₂$\underline{Mn}$O₄ $\underline{Fe}$
$\underline{Fe}$Cl₂ $\underline{Fe}$₂(SO₄)₃ H₂$\underline{S}$ H₂$\underline{S}$O₄ $\underline{S}$O₂
$\underline{Cl}_2$ NaCl$\underline{Cl}$O₂ K$\underline{Cl}$O₃ K₂$\underline{Mn}$O₄ $\underline{Fe}$
$\underline{Fe}$Cl₂ $\underline{Fe}$₂(SO₄)₃ H₂$\underline{S}$ H₂$\underline{S}$O₄ $\underline{S}$O₂
答案:
${\overset{0}{Cl}_{2}}$ ${Na\overset{+3}{Cl}O_{2}}$ ${K\overset{+5}{Cl}O_{3}}$ ${K_{2}\overset{+6}{Mn}O_{4}}$ ${\overset{0}{Fe}}$ ${\overset{+2}{Fe}Cl_{2}}$ ${\overset{+3}{Fe}_{2}(SO_{4})_{3}}$ ${H_{2}\overset{-2}{S}}$ ${H_{2}\overset{+6}{S}O_{4}}$ ${\overset{+4}{S}O_{2}}$
14. A 写出下列物质的化学式。
氖气:
硝酸镁:
氯化钡:
氖气:
${Ne}$
氧化铁:${Fe_{2}O_{3}}$
硫酸铝:${Al_{2}(SO_{4})_{3}}$
氢氧化钙:${Ca(OH)_{2}}$
硝酸镁:
${Mg(NO_{3})_{2}}$
碳酸钠:${Na_{2}CO_{3}}$
氯气:${Cl_{2}}$
硝酸银:${AgNO_{3}}$
氯化钡:
${BaCl_{2}}$
硫酸铵:${(NH_{4})_{2}SO_{4}}$
答案:
${Ne}$ ${Fe_{2}O_{3}}$ ${Al_{2}(SO_{4})_{3}}$ ${Ca(OH)_{2}}$ ${Mg(NO_{3})_{2}}$ ${Na_{2}CO_{3}}$ ${Cl_{2}}$ ${AgNO_{3}}$ ${BaCl_{2}}$ ${(NH_{4})_{2}SO_{4}}$
15. A 写出下列物质的名称。
Hg:
Ar:
Hg:
汞
NH₄Cl:氯化铵
Ca(NO₃)₂:硝酸钙
Fe(OH)₂:氢氧化亚铁
Ar:
氩气
K₂CO₃:碳酸钾
答案:
汞 氯化铵 硝酸钙 氢氧化亚铁 氩气 碳酸钾
16. B (2023 秋·福建南平期中)请从 H、C、N、O、Na、Cl、K、Ca 中选取相关元素,用合适的化学用语填空。
(1)已知 NO₂⁻,请标出$\underset{\cdot}{N}$(NO₂)₃中加点 N 的化合价______
(2)含有 2 核 10 电子的阴离子______
(3)厨房中最常见的调味品______(填化学式,下同)
(4)有刺激性气味的含氧化合物______
(5)实验室中可在 MnO₂催化下制 O₂的物质______(含 2 种元素)
(6)可作补钙剂的物质______
(1)已知 NO₂⁻,请标出$\underset{\cdot}{N}$(NO₂)₃中加点 N 的化合价______
${\overset{+3}{N}(NO_{2})_{3}}$
;(2)含有 2 核 10 电子的阴离子______
${OH^{-}}$
;(3)厨房中最常见的调味品______(填化学式,下同)
${NaCl}$
;(4)有刺激性气味的含氧化合物______
${NH_{4}HCO_{3}}$
;(5)实验室中可在 MnO₂催化下制 O₂的物质______(含 2 种元素)
${H_{2}O_{2}}$
、______(含 3 种元素)${KClO_{3}}$
;(6)可作补钙剂的物质______
${CaCO_{3}}$
。
答案:
(1)${\overset{+3}{N}(NO_{2})_{3}}$
(2)${OH^{-}}$
(3)${NaCl}$
(4)${NH_{4}HCO_{3}}$
(5)${H_{2}O_{2}}$ ${KClO_{3}}$
(6)${CaCO_{3}}$ 点拨:
(1)已知${NO^{-}_{2}}$,说明${NO^{-}_{2}}$的化合价是$-1$,设加点氮元素化合价为$x$,根据题意有:$x+(-1)×3=0$,$x=+3$;
(2)含有 2 核 10 电子的阴离子是氢氧根离子,每个氢氧根离子带 1 个单位负电荷,表示为${OH^{-}}$;
(3)厨房中最常见的调味品是氯化钠,氯化钠中,钠元素化合价是$+1$,氯元素化合价是$-1$,根据化合物中各元素化合价代数和为零可知,氯化钠中钠离子和氯离子的个数比是$1:1$,表示为${NaCl}$;
(4)有刺激性气味的含氧化合物是碳酸氢铵,碳酸氢铵中,铵根的化合价是$+1$,氢元素的化合价是$+1$,碳酸根的化合价是$-2$,根据化合物中各元素化合价代数和为零可知,碳酸氢铵的化学式为${NH_{4}HCO_{3}}$;
(5)实验室中可在${MnO_{2}}$催化下制${O_{2}}$的物质是过氧化氢、氯酸钾,每个过氧化氢分子由 2 个氢原子和 2 个氧原子构成,氯酸钾中钾离子和氯酸根个数比是$1:1$,因此过氧化氢、氯酸钾分别表示为${H_{2}O_{2}}$、${KClO_{3}}$;
(6)可作补钙剂的物质是碳酸钙,碳酸钙中,钙离子和碳酸根的个数比是$1:1$,表示为${CaCO_{3}}$。
(1)${\overset{+3}{N}(NO_{2})_{3}}$
(2)${OH^{-}}$
(3)${NaCl}$
(4)${NH_{4}HCO_{3}}$
(5)${H_{2}O_{2}}$ ${KClO_{3}}$
(6)${CaCO_{3}}$ 点拨:
(1)已知${NO^{-}_{2}}$,说明${NO^{-}_{2}}$的化合价是$-1$,设加点氮元素化合价为$x$,根据题意有:$x+(-1)×3=0$,$x=+3$;
(2)含有 2 核 10 电子的阴离子是氢氧根离子,每个氢氧根离子带 1 个单位负电荷,表示为${OH^{-}}$;
(3)厨房中最常见的调味品是氯化钠,氯化钠中,钠元素化合价是$+1$,氯元素化合价是$-1$,根据化合物中各元素化合价代数和为零可知,氯化钠中钠离子和氯离子的个数比是$1:1$,表示为${NaCl}$;
(4)有刺激性气味的含氧化合物是碳酸氢铵,碳酸氢铵中,铵根的化合价是$+1$,氢元素的化合价是$+1$,碳酸根的化合价是$-2$,根据化合物中各元素化合价代数和为零可知,碳酸氢铵的化学式为${NH_{4}HCO_{3}}$;
(5)实验室中可在${MnO_{2}}$催化下制${O_{2}}$的物质是过氧化氢、氯酸钾,每个过氧化氢分子由 2 个氢原子和 2 个氧原子构成,氯酸钾中钾离子和氯酸根个数比是$1:1$,因此过氧化氢、氯酸钾分别表示为${H_{2}O_{2}}$、${KClO_{3}}$;
(6)可作补钙剂的物质是碳酸钙,碳酸钙中,钙离子和碳酸根的个数比是$1:1$,表示为${CaCO_{3}}$。
17. C 了解物质的组成与结构,有助于认识物质的性质。
(1)如图表示核电荷数为 11~17 的元素最高和最低化合价。
①从图中可以看出,氯元素的最高正价是
②若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为
③写出图中元素的化合价随着核电荷数递增的一条变化规律:
(2)我们知道,金属的化学性质越活泼,越容易失去电子。某金属原子的结构示意图为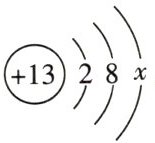
,则最外层电子数 x=

(1)如图表示核电荷数为 11~17 的元素最高和最低化合价。
①从图中可以看出,氯元素的最高正价是
+7
价。②若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为
8
。③写出图中元素的化合价随着核电荷数递增的一条变化规律:
从左到右元素的最高正化合价从+1价逐渐升高到+7价(合理即可)
。(2)我们知道,金属的化学性质越活泼,越容易失去电子。某金属原子的结构示意图为

,则最外层电子数 x=
3
;若失去最外层电子,达到相对稳定结构,该带电粒子的符号为Al³⁺
。
答案:
(1)①$+7$ ②8 ③从左到右元素的最高正化合价从$+1$价逐渐升高到$+7$价(合理即可)
(2)3 ${Al^{3+}}$ 点拨:
(1)①从图中可以看出,氯元素的最高正价是$+7$价;②若某元素既可显正价,又可显负价,以氯元素为例,它的最高正价与最低负价绝对值的代数和为$|+7|+|-1|=8$;③根据图中提供的信息可以看出,从左到右,各元素原子的最外层电子数逐渐递增,因此,各元素的最高正价逐渐递增,而最低负价则从$-4$逐渐递增到$-1$。
(2)图示原子为核电荷数为 13 的元素的原子,即铝元素的原子,根据核电荷数$=$核外电子数,可求得$x=3$;失去最外层 3 个电子后变为带 3 个单位正电荷的阳离子,符号为${Al^{3+}}$。
(1)①$+7$ ②8 ③从左到右元素的最高正化合价从$+1$价逐渐升高到$+7$价(合理即可)
(2)3 ${Al^{3+}}$ 点拨:
(1)①从图中可以看出,氯元素的最高正价是$+7$价;②若某元素既可显正价,又可显负价,以氯元素为例,它的最高正价与最低负价绝对值的代数和为$|+7|+|-1|=8$;③根据图中提供的信息可以看出,从左到右,各元素原子的最外层电子数逐渐递增,因此,各元素的最高正价逐渐递增,而最低负价则从$-4$逐渐递增到$-1$。
(2)图示原子为核电荷数为 13 的元素的原子,即铝元素的原子,根据核电荷数$=$核外电子数,可求得$x=3$;失去最外层 3 个电子后变为带 3 个单位正电荷的阳离子,符号为${Al^{3+}}$。
查看更多完整答案,请扫码查看


