第47页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
6. B (2024秋·苏州期中)氧烛常为密闭空间的应急氧源,某种氧烛产氧药块主要成分为$NaClO_{3}$(化学性质与$KClO_{3}$相似)、金属粉(燃烧时放热,提供$NaClO_{3}$分解所需热量)和催化剂等,工作时敲击火帽,火帽点燃后能持续燃烧,使内部药块反应放出高纯氧气,可持续工作达1小时以上。下列说法中不正确的是 (
A. 氧烛在工作时,有一定的照明功能
B. 氧烛中催化剂的质量随着反应的进行不发生改变
C. 金属粉质量的多少不会影响氧烛释放出氧气的质量
D. 氧烛释放的氧气主要来自产氧药块中的$NaClO_{3}$
C
)A. 氧烛在工作时,有一定的照明功能
B. 氧烛中催化剂的质量随着反应的进行不发生改变
C. 金属粉质量的多少不会影响氧烛释放出氧气的质量
D. 氧烛释放的氧气主要来自产氧药块中的$NaClO_{3}$
答案:
C 点拨: 金属粉燃烧会发光, 所以氧烛在使用时可能具有照明的功能, 故 A 选项说法正确; 在化学反应前后, 催化剂的质量和化学性质均不发生改变, 所以其质量在反应前后不变, 故 B 选项说法正确; 金属粉过少导致金属粉燃烧产生的热量少, 使得 NaClO₃无法分解产生氧气; 金属粉过多, 燃烧时会消耗较多的氧气, 从而减少产氧量, 故 C 选项说法错误; NaClO₃化学性质与 KClO₃相似, 在催化剂作用下受热分解为氯化钠和氧气, 所以氧烛释放的氧气主要来自产氧药块中的 NaClO₃, 故 D 选项说法正确。故本题选 C。
7. A (2024秋·江苏连云港期中)如图是实验室制取气体常用的发生装置和收集装置,请按要求回答下列问题:
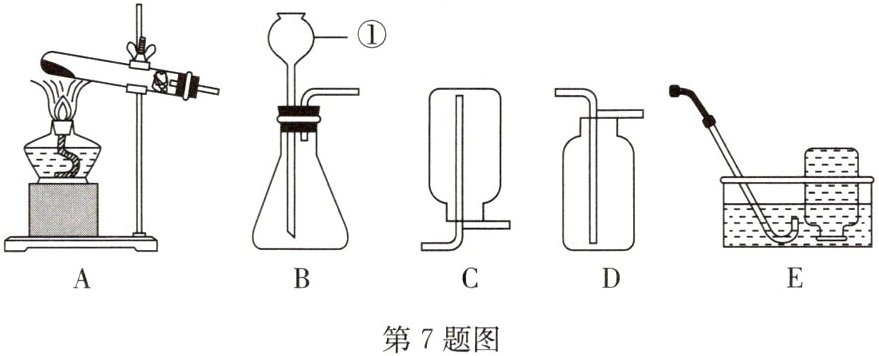
(1)写出仪器①的名称:________。
(2)实验室用过氧化氢和二氧化锰制取氧气常选用的发生装置和收集装置是________(填字母),反应的符号表达式为________。
(3)选用装置A制氧气,反应的符号表达式为________,试管口塞一团棉花的作用是________;用E收集氧气的优点是________。
(4)氧烛是一种简易制氧机。它体积小、质量轻,贮存期长,产氧量大,适用于在缺氧环境急救。有以下几种制氧剂,根据提供的信息选择一种适合氧烛的制氧剂。

你选择的制氧剂是________,理由是________。
(1)写出仪器①的名称:
(2)实验室用过氧化氢和二氧化锰制取氧气常选用的发生装置和收集装置是
(3)选用装置A制氧气,反应的符号表达式为
(4)氧烛是一种简易制氧机。它体积小、质量轻,贮存期长,产氧量大,适用于在缺氧环境急救。有以下几种制氧剂,根据提供的信息选择一种适合氧烛的制氧剂。

你选择的制氧剂是

(1)写出仪器①的名称:________。
(2)实验室用过氧化氢和二氧化锰制取氧气常选用的发生装置和收集装置是________(填字母),反应的符号表达式为________。
(3)选用装置A制氧气,反应的符号表达式为________,试管口塞一团棉花的作用是________;用E收集氧气的优点是________。
(4)氧烛是一种简易制氧机。它体积小、质量轻,贮存期长,产氧量大,适用于在缺氧环境急救。有以下几种制氧剂,根据提供的信息选择一种适合氧烛的制氧剂。

你选择的制氧剂是________,理由是________。
(1)写出仪器①的名称:
长颈漏斗
。(2)实验室用过氧化氢和二氧化锰制取氧气常选用的发生装置和收集装置是
BD或BE
(填字母),反应的符号表达式为$H₂O₂\xrightarrow{MnO₂}H₂O + O₂$
。(3)选用装置A制氧气,反应的符号表达式为
$KMnO₄\xrightarrow{加热}K₂MnO₄ + MnO₂ + O₂$
,试管口塞一团棉花的作用是防止加热时固体粉末进入导管
;用E收集氧气的优点是收集的氧气更纯净
。(4)氧烛是一种简易制氧机。它体积小、质量轻,贮存期长,产氧量大,适用于在缺氧环境急救。有以下几种制氧剂,根据提供的信息选择一种适合氧烛的制氧剂。

你选择的制氧剂是
氯酸钠
,理由是在催化剂的作用下,加热分解持续快速释放氧气
。
答案:
(1) 长颈漏斗
(2) BD 或$ BE H₂O₂\xrightarrow{MnO₂}H₂O + O₂ (3) KMnO₄\xrightarrow{加热}K₂MnO₄ + MnO₂ + O₂ $防止加热时固体粉末进入导管 收集的氧气更纯净
(4) 氯酸钠 在催化剂的作用下, 加热分解持续快速释放氧气
(1) 长颈漏斗
(2) BD 或$ BE H₂O₂\xrightarrow{MnO₂}H₂O + O₂ (3) KMnO₄\xrightarrow{加热}K₂MnO₄ + MnO₂ + O₂ $防止加热时固体粉末进入导管 收集的氧气更纯净
(4) 氯酸钠 在催化剂的作用下, 加热分解持续快速释放氧气
8. B 某化学兴趣小组对如下三个实验进行了探究:
【实验一】如图1是小组最终制成的简易制氧机成品,小组使用实验室常见制氧药剂,将一种白色粉末和黑色粉末的混合物装填在制氧机中。

回答下列问题:
(1)写出该制氧机内发生反应的文字表达式:________。
(2)撞击火帽的目的是________。
【实验二】混制“富氧空气”
(3)用纯氮气及上述实验制取的氧气,混制一瓶(集气瓶容积为250mL)氧气体积分数为40%的“富氧空气”,可使用图2所示装置,先在如图装置中装满水,再从导管________(填“a”或“b”)通入氮气,排出________mL水,然后再通入氧气排出80mL水。
【实验三】探究二氧化锰、氧化铜对过氧化氢分解的催化效果,设计了如下对比实验:
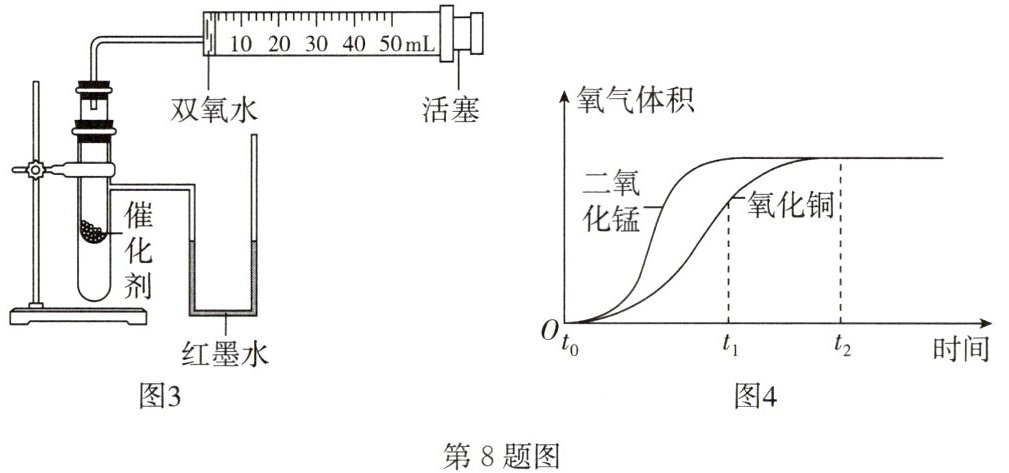
(4)图3实验中造成U形管内红墨水液面左低右高的原因是________。
(5)分析图4图像,比较________(写出比较的量),能得到二氧化锰催化效果比氧化铜好,还能得出的结论是________。
(6)图4中$t_{1}\sim t_{2}$时间段反应速率逐渐变________(填“快”或“慢”),可能的原因是________。
(1)
【实验一】如图1是小组最终制成的简易制氧机成品,小组使用实验室常见制氧药剂,将一种白色粉末和黑色粉末的混合物装填在制氧机中。

回答下列问题:
(1)写出该制氧机内发生反应的文字表达式:________。
(2)撞击火帽的目的是________。
【实验二】混制“富氧空气”
(3)用纯氮气及上述实验制取的氧气,混制一瓶(集气瓶容积为250mL)氧气体积分数为40%的“富氧空气”,可使用图2所示装置,先在如图装置中装满水,再从导管________(填“a”或“b”)通入氮气,排出________mL水,然后再通入氧气排出80mL水。
【实验三】探究二氧化锰、氧化铜对过氧化氢分解的催化效果,设计了如下对比实验:

(4)图3实验中造成U形管内红墨水液面左低右高的原因是________。
(5)分析图4图像,比较________(写出比较的量),能得到二氧化锰催化效果比氧化铜好,还能得出的结论是________。
(6)图4中$t_{1}\sim t_{2}$时间段反应速率逐渐变________(填“快”或“慢”),可能的原因是________。
(1)
氯酸钾$\xrightarrow[$加热]{二氧化锰}氯化钾 + 氧气
(2) 加热, 使温度达到氯酸钾的分解温度
(3) b
120
(4) 反应放出热量, 使得在试管内温度升高, 压强变大
(5) 相同时间注射器内氧气的体积
催化剂不能改变生成氧气的量
(6) 慢
过氧化氢溶液浓度下降
答案:
(1) 氯酸钾$\xrightarrow[$加热]{二氧化锰}氯化钾 + 氧气
(2) 加热, 使温度达到氯酸钾的分解温度
(3) b 120
(4) 反应放出热量, 使得在试管内温度升高, 压强变大
(5) 相同时间注射器内氧气的体积 催化剂不能改变生成氧气的量
(6) 慢 过氧化氢溶液浓度下降 点拨:
(1) 氯酸钾是一种白色粉末, 二氧化锰是一种黑色粉末, 制氧机中, 氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气;
(2) 撞击火帽的目的是加热, 使温度达到氯酸钾的分解温度;
(3) 用纯氮气及上述实验制取的氧气, 混制一瓶(集气瓶容积为 250mL)氧气体积分数为 40%的“富氧空气”, 可使用图 2 装置, 先在装置中装满水, 再从导管 b 通入氮气, 排出 xmL 水, 后再通入氧气排出 80mL 水, 此时氧气体积分数为 80mL/(xmL + 80mL)×100% = 40%, 解得 x = 120;
(4) 图 3 实验中造成 U 形管内红墨水液面左低右高的原因是反应放出热量;
(5) 要比较两种催化剂的催化效果, 主要比较相同时间内收集的氧气体积, 相同时间收集的氧气体积越大, 说明催化效果越好; 由图像分析得出, 当反应结束时, 无论是用何种催化剂, 等体积、等浓度的过氧化氢溶液生成的氧气体积相等, 说明催化剂不能改变生成氧气的量;
(6) t₁ ~ t₂ 时间段曲线逐渐变平缓, 说明反应速率逐渐变慢, 这是因为随着反应的进行, 过氧化氢溶液浓度在不断下降。
(1) 氯酸钾$\xrightarrow[$加热]{二氧化锰}氯化钾 + 氧气
(2) 加热, 使温度达到氯酸钾的分解温度
(3) b 120
(4) 反应放出热量, 使得在试管内温度升高, 压强变大
(5) 相同时间注射器内氧气的体积 催化剂不能改变生成氧气的量
(6) 慢 过氧化氢溶液浓度下降 点拨:
(1) 氯酸钾是一种白色粉末, 二氧化锰是一种黑色粉末, 制氧机中, 氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气;
(2) 撞击火帽的目的是加热, 使温度达到氯酸钾的分解温度;
(3) 用纯氮气及上述实验制取的氧气, 混制一瓶(集气瓶容积为 250mL)氧气体积分数为 40%的“富氧空气”, 可使用图 2 装置, 先在装置中装满水, 再从导管 b 通入氮气, 排出 xmL 水, 后再通入氧气排出 80mL 水, 此时氧气体积分数为 80mL/(xmL + 80mL)×100% = 40%, 解得 x = 120;
(4) 图 3 实验中造成 U 形管内红墨水液面左低右高的原因是反应放出热量;
(5) 要比较两种催化剂的催化效果, 主要比较相同时间内收集的氧气体积, 相同时间收集的氧气体积越大, 说明催化效果越好; 由图像分析得出, 当反应结束时, 无论是用何种催化剂, 等体积、等浓度的过氧化氢溶液生成的氧气体积相等, 说明催化剂不能改变生成氧气的量;
(6) t₁ ~ t₂ 时间段曲线逐渐变平缓, 说明反应速率逐渐变慢, 这是因为随着反应的进行, 过氧化氢溶液浓度在不断下降。
查看更多完整答案,请扫码查看


