第57页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
9.(2023秋·江苏扬州期中)某化学兴趣小组开展“测定密闭容器中氧气的体积分数”的实验探究。
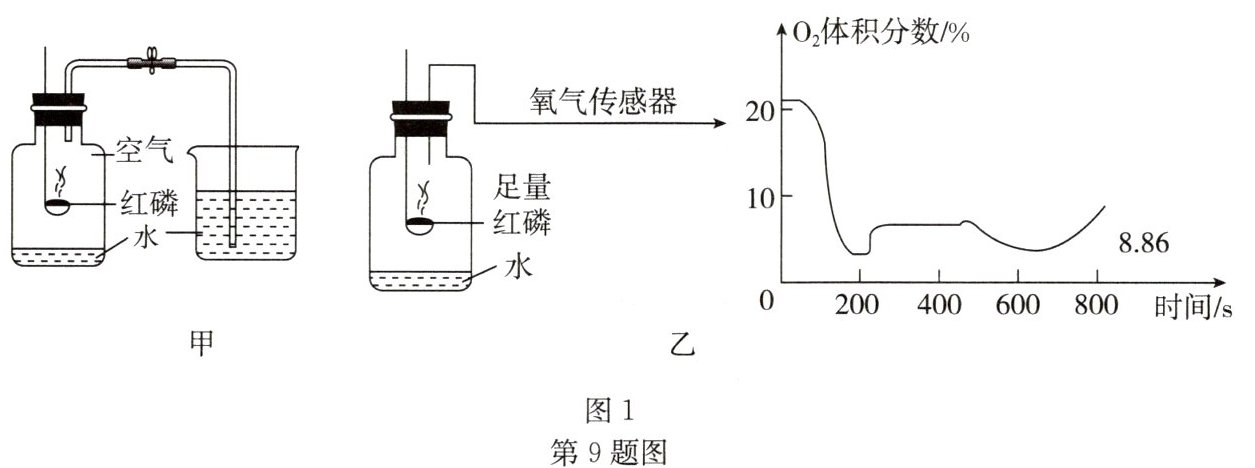
Ⅰ.图1甲为我们熟悉的测定空气中氧气含量的实验。
(1)红磷燃烧的主要现象为
(2)若实验过程中,发现烧杯中导管口出现气泡,则最终测得数据会
Ⅱ.图1乙实验中,小组成员利用传感器记录集气瓶内氧气体积分数随时间变化的情况。
(3)从以上数据分析,最终集气瓶中的氧气没有消耗完的依据是
(4)实验开始时氧气的含量持续下降,氧气被消耗,但在200s时氧气的含量又有所上升,若实验过程中红磷量充足,其可能原因是
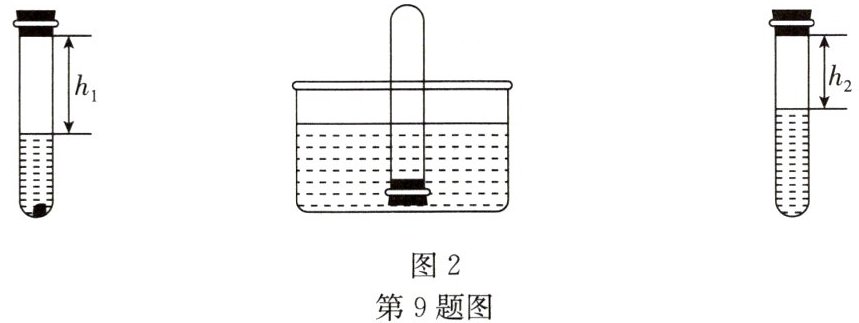
Ⅲ.小组成员通过查阅资料对教材实验进行改进,利用四硫化二钠(Na₂S₄)固体可替代红磷进行实验,其反应原理为Na₂S₄+O₂+H₂O→S+NaOH(S和NaOH均为固体,对实验结果无影响),实验设计如图2。
实验步骤如下:
①取足量的四硫化二钠(Na₂S₄)固体置于试管中,加入适量的水,并迅速塞紧橡胶塞,再充分振荡;
②测量液面至橡胶塞下沿的距离,记录数据h₁;
③将该试管插入水中,取下橡胶塞,观察到试管内液面上升;
④当管内液面稳定时塞紧橡胶塞,将试管取出倒转过来,测量液面至橡胶塞下沿的距离,记录数据h₂。
(5)步骤①中进行充分振荡的目的是
(6)空气中氧气的体积分数约为
(7)该实验与教材中的实验相比,优点是
Ⅰ.图1甲为我们熟悉的测定空气中氧气含量的实验。
(1)红磷燃烧的主要现象为
产生大量白烟,放热,生成白色固体
,反应的符号表达式是$P+O_{2}\xrightarrow{点燃}P_{2}O_{5}$
,反应的基本类型是化合反应
。(2)若实验过程中,发现烧杯中导管口出现气泡,则最终测得数据会
偏大
(填“偏大”“偏小”或“无影响”)。Ⅱ.图1乙实验中,小组成员利用传感器记录集气瓶内氧气体积分数随时间变化的情况。
(3)从以上数据分析,最终集气瓶中的氧气没有消耗完的依据是
完全反应后氧气体积分数是8.86%
。(4)实验开始时氧气的含量持续下降,氧气被消耗,但在200s时氧气的含量又有所上升,若实验过程中红磷量充足,其可能原因是
装置突然漏气(合理即可)
。Ⅲ.小组成员通过查阅资料对教材实验进行改进,利用四硫化二钠(Na₂S₄)固体可替代红磷进行实验,其反应原理为Na₂S₄+O₂+H₂O→S+NaOH(S和NaOH均为固体,对实验结果无影响),实验设计如图2。
实验步骤如下:
①取足量的四硫化二钠(Na₂S₄)固体置于试管中,加入适量的水,并迅速塞紧橡胶塞,再充分振荡;
②测量液面至橡胶塞下沿的距离,记录数据h₁;
③将该试管插入水中,取下橡胶塞,观察到试管内液面上升;
④当管内液面稳定时塞紧橡胶塞,将试管取出倒转过来,测量液面至橡胶塞下沿的距离,记录数据h₂。
(5)步骤①中进行充分振荡的目的是
使氧气充分反应
。(6)空气中氧气的体积分数约为
$(h_{1}-h_{2})/h_{1}×100\%$
(用含h₁和h₂的式子表示)。(7)该实验与教材中的实验相比,优点是
实验结果更准确、更环保(合理即可)
(写出一点即可)。

答案:
(1)产生大量白烟,放热,生成白色固体 $P+O_{2}\xrightarrow{点燃}P_{2}O_{5}$ 化合反应
(2)偏大
(3)完全反应后氧气体积分数是8.86%
(4)装置突然漏气(合理即可)
(5)使氧气充分反应
(6)$(h_{1}-h_{2})/h_{1}×100\%$
(7)实验结果更准确、更环保(合理即可)
点拨:
(1)红磷燃烧的主要现象为产生大量白烟,放热,生成白色固体,反应物为磷和氧气,生成物为五氧化二磷,故反应的基本类型是化合反应。
(2)若实验过程中,发现烧杯中导管口出现气泡,是因为止水夹夹得不紧,导致部分气体膨胀逸出,则最终测得数据会偏大。
(3)从以上数据分析,最终完全反应后集气瓶中的氧气体积分数是8.86%,所以集气瓶中的氧气没有消耗完。
(4)实验开始时氧气的含量持续下降,氧气被消耗,但在200s时氧气的含量又有所上升,若实验过程中红磷量充足,其可能原因是装置突然漏气或温度升高体积膨胀等。
(5)步骤①中进行充分振荡的目的是使氧气充分反应。
(6)由实验可知,空气中氧气的体积分数约为$(h_{1}-h_{2})/h_{1}×100\%$。
(7)该实验与教材中的实验相比,优点是实验结果更准确、更环保。
(1)产生大量白烟,放热,生成白色固体 $P+O_{2}\xrightarrow{点燃}P_{2}O_{5}$ 化合反应
(2)偏大
(3)完全反应后氧气体积分数是8.86%
(4)装置突然漏气(合理即可)
(5)使氧气充分反应
(6)$(h_{1}-h_{2})/h_{1}×100\%$
(7)实验结果更准确、更环保(合理即可)
点拨:
(1)红磷燃烧的主要现象为产生大量白烟,放热,生成白色固体,反应物为磷和氧气,生成物为五氧化二磷,故反应的基本类型是化合反应。
(2)若实验过程中,发现烧杯中导管口出现气泡,是因为止水夹夹得不紧,导致部分气体膨胀逸出,则最终测得数据会偏大。
(3)从以上数据分析,最终完全反应后集气瓶中的氧气体积分数是8.86%,所以集气瓶中的氧气没有消耗完。
(4)实验开始时氧气的含量持续下降,氧气被消耗,但在200s时氧气的含量又有所上升,若实验过程中红磷量充足,其可能原因是装置突然漏气或温度升高体积膨胀等。
(5)步骤①中进行充分振荡的目的是使氧气充分反应。
(6)由实验可知,空气中氧气的体积分数约为$(h_{1}-h_{2})/h_{1}×100\%$。
(7)该实验与教材中的实验相比,优点是实验结果更准确、更环保。
查看更多完整答案,请扫码查看


