2025年5年高考3年模拟高中化学必修第二册苏教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年5年高考3年模拟高中化学必修第二册苏教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第68页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
6. (2025 江苏镇江期中) 丙炔酸甲酯(${CH\equiv C - COOCH_{3}}$)是一种重要的有机化工原料,沸点为$103\sim 105\ ^{\circ} C$。实验室制备少量丙炔酸甲酯的反应为${CH\equiv C - COOH + CH_{3}OH \underset{\lower{7mu}{\Delta}}{\overset{ 浓硫酸}{⇌}} CH\equiv C - COOCH_{3} + H_{2}O}$。实验步骤如下:
步骤1:在反应瓶中,加入$14.00\ g$丙炔酸、$50\ mL$甲醇和$2\ mL$浓硫酸,搅拌,加热回流一段时间。
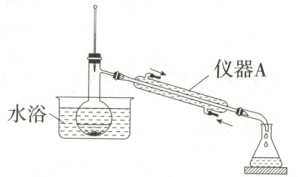
步骤2:蒸出过量的甲醇(装置如图)。
步骤3:反应液冷却后,依次用饱和$NaCl$溶液、$5\%\ {Na_{2}CO_{3}}$溶液、水洗涤,然后分离出有机相。
步骤4:有机相经无水${Na_{2}SO_{4}}$干燥、过滤、蒸馏,得丙炔酸甲酯$10.08\ g$。
(1)步骤1中,加入过量甲醇的目的是
(2)步骤2中,如图所示的装置中仪器A的名称是
(3)步骤3中,用$5\%\ {Na_{2}CO_{3}}$溶液洗涤,主要除去的物质是
(4)步骤4中,蒸馏时不能用水浴加热的原因是
(5)实验中丙炔酸甲酯的产率为
]
步骤1:在反应瓶中,加入$14.00\ g$丙炔酸、$50\ mL$甲醇和$2\ mL$浓硫酸,搅拌,加热回流一段时间。
步骤2:蒸出过量的甲醇(装置如图)。
步骤3:反应液冷却后,依次用饱和$NaCl$溶液、$5\%\ {Na_{2}CO_{3}}$溶液、水洗涤,然后分离出有机相。
步骤4:有机相经无水${Na_{2}SO_{4}}$干燥、过滤、蒸馏,得丙炔酸甲酯$10.08\ g$。

(1)步骤1中,加入过量甲醇的目的是
提高丙炔酸的利用率(合理即可)
。(2)步骤2中,如图所示的装置中仪器A的名称是
直形冷凝管
;蒸馏烧瓶中加入碎瓷片的目的是防止暴沸
。(3)步骤3中,用$5\%\ {Na_{2}CO_{3}}$溶液洗涤,主要除去的物质是
丙炔酸
;分离出有机相的操作名称为分液
。(4)步骤4中,蒸馏时不能用水浴加热的原因是
丙炔酸甲酯的沸点比水的高
。(5)实验中丙炔酸甲酯的产率为
60%
。]
答案:
6.答案
(1)提高丙炔酸的利用率(合理即可)
(2)直形冷凝管 防止暴沸
(3)丙炔酸 分液
(4)丙炔酸甲酯的沸点比水的高
(5)60%
解析
(1)步骤 1 中,由于酯化反应为可逆反应,甲醇过量,有利于丙炔酸的转化,可提高丙炔酸的利用率。
(2)仪器 A 的名称是直形冷凝管;蒸馏烧瓶中加入碎瓷片能防止液体混合物受热时暴沸。
(3)5% $\mathrm{Na_2CO_3}$ 溶液能与丙炔酸反应,故步骤 3 中用 5% $\mathrm{Na_2CO_3}$ 溶液洗涤,主要除去的物质是丙炔酸。洗涤后液体分层,分离出有机相的操作为分液。
(4)丙炔酸甲酯沸点比水的高,水浴加热温度不够高,因此步骤 4 蒸馏时不能用水浴加热。
(5)甲醇过量,根据丙炔酸来计算丙炔酸甲酯的理论产量,14.00 g 丙炔酸为 0.2 mol,则理论上生成 0.2 mol 丙炔酸甲酯,丙炔酸甲酯的产率为$\frac{10.08\ g}{0.2\ mol × 84\ g · mol^{-1}} × 100\% = 60\%$。
(1)提高丙炔酸的利用率(合理即可)
(2)直形冷凝管 防止暴沸
(3)丙炔酸 分液
(4)丙炔酸甲酯的沸点比水的高
(5)60%
解析
(1)步骤 1 中,由于酯化反应为可逆反应,甲醇过量,有利于丙炔酸的转化,可提高丙炔酸的利用率。
(2)仪器 A 的名称是直形冷凝管;蒸馏烧瓶中加入碎瓷片能防止液体混合物受热时暴沸。
(3)5% $\mathrm{Na_2CO_3}$ 溶液能与丙炔酸反应,故步骤 3 中用 5% $\mathrm{Na_2CO_3}$ 溶液洗涤,主要除去的物质是丙炔酸。洗涤后液体分层,分离出有机相的操作为分液。
(4)丙炔酸甲酯沸点比水的高,水浴加热温度不够高,因此步骤 4 蒸馏时不能用水浴加热。
(5)甲醇过量,根据丙炔酸来计算丙炔酸甲酯的理论产量,14.00 g 丙炔酸为 0.2 mol,则理论上生成 0.2 mol 丙炔酸甲酯,丙炔酸甲酯的产率为$\frac{10.08\ g}{0.2\ mol × 84\ g · mol^{-1}} × 100\% = 60\%$。
7.(2025江苏徐州第三中学开学考试)对溴甲苯(${H_{3}C - \underset{}{\overset{}{ 苯环}} - Br}$)是一种有机合成原料,广泛应用于医药合成。实验室中由甲苯和${Br_{2}}$反应制取对溴甲苯并检验部分产物的装置如图所示。
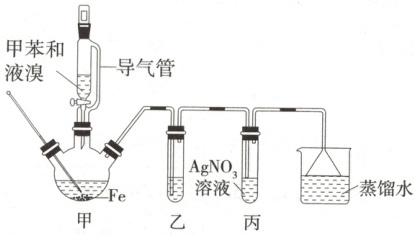
(1)装置甲中导气管的作用为
(2)装置甲中主要发生反应的化学方程式为
(3)装置乙中需盛放的试剂名称为
(4)取装置甲中反应后的液体混合物,经过下列操作可获得纯净的对溴甲苯。
步骤1:水洗,分液;
步骤2:用$NaOH$稀溶液洗涤,除去
步骤3:水洗,分液;
步骤4:加入无水${CaCl_{2}}$干燥,过滤;
步骤5:通过
a.过滤
b.蒸馏
c.蒸发
(5)关于该实验,下列说法正确的是
a.可以用溴水代替液溴
b.装置丙中的导管可以插入溶液中
c.装置丙中有淡黄色沉淀生成,说明该反应为取代反应
]

(1)装置甲中导气管的作用为
平衡气压,使甲苯和液溴混合溶液顺利滴下
。(2)装置甲中主要发生反应的化学方程式为
$\mathrm{H_3C—◯ +Br_2\xrightarrow{FeBr_3}H_3C—◯—Br +HBr}$
。(3)装置乙中需盛放的试剂名称为
苯或四氯化碳
。(4)取装置甲中反应后的液体混合物,经过下列操作可获得纯净的对溴甲苯。
步骤1:水洗,分液;
步骤2:用$NaOH$稀溶液洗涤,除去
$\mathrm{Br_2}$
(填化学式),分液;步骤3:水洗,分液;
步骤4:加入无水${CaCl_{2}}$干燥,过滤;
步骤5:通过
b
(填字母),分离对溴甲苯和甲苯。a.过滤
b.蒸馏
c.蒸发
(5)关于该实验,下列说法正确的是
c
(填字母)。a.可以用溴水代替液溴
b.装置丙中的导管可以插入溶液中
c.装置丙中有淡黄色沉淀生成,说明该反应为取代反应
]
答案:
7.答案
(1)平衡气压,使甲苯和液溴混合溶液顺利滴下
(2)$\mathrm{H_3C—◯ +Br_2\xrightarrow{FeBr_3}H_3C—◯—Br +HBr}$
(3)苯或四氯化碳
(4)$\mathrm{Br_2}$ b
(5)c
解析
(1)导气管的作用是平衡气压,使甲苯和液溴混合溶液顺利滴下。
(2)装置甲中甲苯与溴单质发生取代反应,其化学方程式为 $\mathrm{H_3C—◯ +Br_2\xrightarrow{FeBr_3}H_3C—◯—Br +HBr}$。
(3)$\mathrm{HBr}$ 中可能混有 $\mathrm{Br_2}$,$\mathrm{Br_2}$ 通入 $\mathrm{AgNO_3}$ 溶液中也有淡黄色沉淀生成,影响 $\mathrm{HBr}$ 的检验,故要使混合气体通入苯或四氯化碳中除去 $\mathrm{Br_2}$。
(4)反应后的混合液中有少量 $\mathrm{Br_2}$,可用 $\mathrm{NaOH}$ 溶液除去。由于对溴甲苯和甲苯的沸点相差较大,故采取蒸馏的方法分离甲苯和对溴甲苯。
(5)甲苯不与溴水反应,a 错误;丙的导管插入液面下会发生倒吸,b 错误;淡黄色沉淀是 $\mathrm{AgBr}$,丙中生成淡黄色沉淀说明甲苯与 $\mathrm{Br_2}$ 发生取代反应生成了 $\mathrm{HBr}$,c 正确。
(1)平衡气压,使甲苯和液溴混合溶液顺利滴下
(2)$\mathrm{H_3C—◯ +Br_2\xrightarrow{FeBr_3}H_3C—◯—Br +HBr}$
(3)苯或四氯化碳
(4)$\mathrm{Br_2}$ b
(5)c
解析
(1)导气管的作用是平衡气压,使甲苯和液溴混合溶液顺利滴下。
(2)装置甲中甲苯与溴单质发生取代反应,其化学方程式为 $\mathrm{H_3C—◯ +Br_2\xrightarrow{FeBr_3}H_3C—◯—Br +HBr}$。
(3)$\mathrm{HBr}$ 中可能混有 $\mathrm{Br_2}$,$\mathrm{Br_2}$ 通入 $\mathrm{AgNO_3}$ 溶液中也有淡黄色沉淀生成,影响 $\mathrm{HBr}$ 的检验,故要使混合气体通入苯或四氯化碳中除去 $\mathrm{Br_2}$。
(4)反应后的混合液中有少量 $\mathrm{Br_2}$,可用 $\mathrm{NaOH}$ 溶液除去。由于对溴甲苯和甲苯的沸点相差较大,故采取蒸馏的方法分离甲苯和对溴甲苯。
(5)甲苯不与溴水反应,a 错误;丙的导管插入液面下会发生倒吸,b 错误;淡黄色沉淀是 $\mathrm{AgBr}$,丙中生成淡黄色沉淀说明甲苯与 $\mathrm{Br_2}$ 发生取代反应生成了 $\mathrm{HBr}$,c 正确。
查看更多完整答案,请扫码查看


