2025年5年高考3年模拟高中化学必修第二册苏教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年5年高考3年模拟高中化学必修第二册苏教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第48页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
7. (2025 广东,15)按图组装装置并进行实验:将铜丝插入溶液中①,当$c$中红色褪去②时,将铜丝拔离液面。下列叙述错误的是 (

A.$a$中有化合反应发生,并有颜色变化
B.$b$中气体变红棕色时,所含氮氧化物至少有两种
C.$c$中溶液红色刚好褪去时,${HCO^{-}_{3}}$恰好完全反应
D.若将$a$中稀硝酸换为浓硫酸并加热,则$c$中溶液颜色会褪去
①看图说“化” $a$中$Cu$与稀硝酸反应生成$NO$;对点突破 P180 知识点2
②关键点拨 $c$中红色褪去,说明$c$中溶液碱性减弱但不一定呈中性或酸性
C
)
A.$a$中有化合反应发生,并有颜色变化
B.$b$中气体变红棕色时,所含氮氧化物至少有两种
C.$c$中溶液红色刚好褪去时,${HCO^{-}_{3}}$恰好完全反应
D.若将$a$中稀硝酸换为浓硫酸并加热,则$c$中溶液颜色会褪去
①看图说“化” $a$中$Cu$与稀硝酸反应生成$NO$;对点突破 P180 知识点2
②关键点拨 $c$中红色褪去,说明$c$中溶液碱性减弱但不一定呈中性或酸性
答案:
7.C
考教衔接
联想教材中铜与稀硝酸的反应,可确定a中涉及的反应有:3Cu+8HNO₃(稀)=3Cu(NO₃)₂+2NO↑+4H₂O、2NO+O₂=2NO₂、3NO₂+H₂O=2HNO₃+NO。
a中铜与稀硝酸发生反应:3Cu+8HNO₃(稀)=3Cu(NO₃)₂+2NO↑+4H₂O,NO会与a内少量O₂发生化合反应:2NO+O₂=2NO₂,会有颜色变化,A正确;a中生成的NO进入b后,与O₂反应生成NO₂,且存在2NO₂⇌N₂O₄,故b中所含氮氧化物至少有两种,B正确;酚酞变色的pH范围为8.2~10.0,c中溶液红色刚好褪去时,溶液仍显碱性,HCO₃⁻未反应完全,C错误;若将a中稀硝酸换为浓硫酸并加热,铜与浓硫酸发生反应:Cu+2H₂SO₄(浓)$\xlongequal{△}$CuSO₄+SO₂↑+2H₂O,生成的SO₂进入c后,与NaHCO₃溶液反应生成CO₂,溶液碱性减弱,c中溶液颜色会褪去,D正确。
考教衔接
联想教材中铜与稀硝酸的反应,可确定a中涉及的反应有:3Cu+8HNO₃(稀)=3Cu(NO₃)₂+2NO↑+4H₂O、2NO+O₂=2NO₂、3NO₂+H₂O=2HNO₃+NO。
a中铜与稀硝酸发生反应:3Cu+8HNO₃(稀)=3Cu(NO₃)₂+2NO↑+4H₂O,NO会与a内少量O₂发生化合反应:2NO+O₂=2NO₂,会有颜色变化,A正确;a中生成的NO进入b后,与O₂反应生成NO₂,且存在2NO₂⇌N₂O₄,故b中所含氮氧化物至少有两种,B正确;酚酞变色的pH范围为8.2~10.0,c中溶液红色刚好褪去时,溶液仍显碱性,HCO₃⁻未反应完全,C错误;若将a中稀硝酸换为浓硫酸并加热,铜与浓硫酸发生反应:Cu+2H₂SO₄(浓)$\xlongequal{△}$CuSO₄+SO₂↑+2H₂O,生成的SO₂进入c后,与NaHCO₃溶液反应生成CO₂,溶液碱性减弱,c中溶液颜色会褪去,D正确。
8. (2023 湖北,18 节选)学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
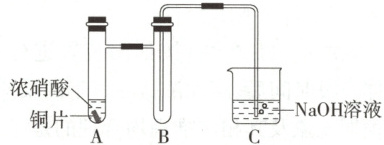
(1) 铜与浓硝酸反应的装置如下图,仪器$A$的名称为
(2) 铜与过量${H_{2}O_{2}}$反应的探究如下:
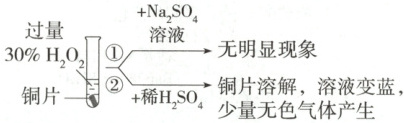
实验②中$Cu$溶解的离子方程式为
(3) 用足量$NaOH$处理实验②新制的溶液得到沉淀$X$,元素分析表明$X$为铜的氧化物,提纯干燥后的$X$在惰性氛围下加热,${\mathit{m}\ \mathrm{g}\ X}$完全分解为${\mathit{n}\ \mathrm{g}}$黑色氧化物$Y$,${\dfrac{\mathit{n}}{\mathit{m}} = \dfrac{5}{6}}$。$X$的化学式为
(1) 铜与浓硝酸反应的装置如下图,仪器$A$的名称为
具支试管
,装置$B$的作用为防止倒吸
。
(2) 铜与过量${H_{2}O_{2}}$反应的探究如下:

实验②中$Cu$溶解的离子方程式为
Cu+H₂O₂+2H⁺=Cu²⁺+2H₂O
;产生的气体为O₂
。比较实验①和②,从氧化还原角度说明${H^{+}}$的作用是增强H₂O₂的氧化性
。(3) 用足量$NaOH$处理实验②新制的溶液得到沉淀$X$,元素分析表明$X$为铜的氧化物,提纯干燥后的$X$在惰性氛围下加热,${\mathit{m}\ \mathrm{g}\ X}$完全分解为${\mathit{n}\ \mathrm{g}}$黑色氧化物$Y$,${\dfrac{\mathit{n}}{\mathit{m}} = \dfrac{5}{6}}$。$X$的化学式为
CuO₂
。
答案:
8.答案
(1)具支试管 防止倒吸
(2)Cu+H₂O₂+2H⁺=Cu²⁺+2H₂O O₂ 增强H₂O₂的氧化性
(3)CuO₂
解析
(2)根据实验现象“铜片溶解,溶液变蓝,少量无色气体产生”可知铜反应生成了硫酸铜,H₂O₂作氧化剂被还原,产物为H₂O,离子方程式为Cu+H₂O₂+2H⁺=Cu²⁺+2H₂O,H₂O₂在Cu²⁺催化下分解生成O₂和H₂O,无色气体为O₂。实验①Na₂SO₄溶液显中性,无明显现象,实验②稀硫酸呈酸性,反应现象明显,通过对比,说明H⁺的作用是增强H₂O₂的氧化性。
(3)由题意可知,黑色氧化物Y为CuO,根据原子守恒,X中m(Cu)=n g×$\frac{64}{80}$=$\frac{4}{5}$n g,已知$\frac{n}{m}$=$\frac{5}{6}$,则m(O)=n g×$\frac{16}{80}$+(m - n)g=$\frac{2}{5}$n g,X中$\frac{n(Cu)}{n(O)}$=$\frac{\frac{4n}{5×64}mol}{\frac{2n}{5×16}mol}$=$\frac{1}{2}$,X为CuO₂。
(1)具支试管 防止倒吸
(2)Cu+H₂O₂+2H⁺=Cu²⁺+2H₂O O₂ 增强H₂O₂的氧化性
(3)CuO₂
解析
(2)根据实验现象“铜片溶解,溶液变蓝,少量无色气体产生”可知铜反应生成了硫酸铜,H₂O₂作氧化剂被还原,产物为H₂O,离子方程式为Cu+H₂O₂+2H⁺=Cu²⁺+2H₂O,H₂O₂在Cu²⁺催化下分解生成O₂和H₂O,无色气体为O₂。实验①Na₂SO₄溶液显中性,无明显现象,实验②稀硫酸呈酸性,反应现象明显,通过对比,说明H⁺的作用是增强H₂O₂的氧化性。
(3)由题意可知,黑色氧化物Y为CuO,根据原子守恒,X中m(Cu)=n g×$\frac{64}{80}$=$\frac{4}{5}$n g,已知$\frac{n}{m}$=$\frac{5}{6}$,则m(O)=n g×$\frac{16}{80}$+(m - n)g=$\frac{2}{5}$n g,X中$\frac{n(Cu)}{n(O)}$=$\frac{\frac{4n}{5×64}mol}{\frac{2n}{5×16}mol}$=$\frac{1}{2}$,X为CuO₂。
9. (2024 河北,10)图示装置不能完成相应气体的发生和收集实验的是(加热、除杂和尾气处理装置任选) (

|选项|气体|试剂|
| ---- | ---- | ---- |
|A|${SO_{2}}$|饱和${Na_{2}SO_{3}}$溶液+浓硫酸|
|B|${Cl_{2}}$|${MnO_{2}}$+浓盐酸|
|C|${NH_{3}}$|固体${NH_{4}Cl}$+熟石灰|
|D|${CO_{2}}$|石灰石+稀盐酸|
①辅助设问 该装置可以用于哪些类型的反应制备气体?结合题目中四个选项举例说明
②辅助设问 该气体收集装置适用于哪些气体的收集?结合题目中四个选项举例说明
C
)
|选项|气体|试剂|
| ---- | ---- | ---- |
|A|${SO_{2}}$|饱和${Na_{2}SO_{3}}$溶液+浓硫酸|
|B|${Cl_{2}}$|${MnO_{2}}$+浓盐酸|
|C|${NH_{3}}$|固体${NH_{4}Cl}$+熟石灰|
|D|${CO_{2}}$|石灰石+稀盐酸|
①辅助设问 该装置可以用于哪些类型的反应制备气体?结合题目中四个选项举例说明
②辅助设问 该气体收集装置适用于哪些气体的收集?结合题目中四个选项举例说明
答案:
9.C 饱和Na₂SO₃溶液和浓硫酸反应可以制SO₂,使用固液不加热制气装置,SO₂密度比空气大,用向上排空气法收集,可以完成相应气体的发生和收集实验,A不符合题意;MnO₂和浓盐酸加热反应可以制Cl₂,使用固液加热制气装置,Cl₂密度比空气大,用向上排空气法收集,可以完成相应气体的发生和收集实验,B不符合题意;固体NH₄Cl与熟石灰加热可以制NH₃,需要使用固固加热制气装置,图中发生装置不合理,C符合题意;石灰石(主要成分为CaCO₃)和稀盐酸反应可以制CO₂,使用固液不加热制气装置,CO₂密度比空气大,用向上排空气法收集,可以完成相应气体的发生和收集实验,D不符合题意。
思维建模
气体制备实验的基本思路

发生装置→净化装置→干燥装置→收集装置→吸收装置
根据反应物状态及反应条件选择 根据气体及杂质的性质选择干燥剂 根据气体的水溶性及密度选择 根据气体的性质选择吸收剂
9.C 饱和Na₂SO₃溶液和浓硫酸反应可以制SO₂,使用固液不加热制气装置,SO₂密度比空气大,用向上排空气法收集,可以完成相应气体的发生和收集实验,A不符合题意;MnO₂和浓盐酸加热反应可以制Cl₂,使用固液加热制气装置,Cl₂密度比空气大,用向上排空气法收集,可以完成相应气体的发生和收集实验,B不符合题意;固体NH₄Cl与熟石灰加热可以制NH₃,需要使用固固加热制气装置,图中发生装置不合理,C符合题意;石灰石(主要成分为CaCO₃)和稀盐酸反应可以制CO₂,使用固液不加热制气装置,CO₂密度比空气大,用向上排空气法收集,可以完成相应气体的发生和收集实验,D不符合题意。
思维建模
气体制备实验的基本思路

发生装置→净化装置→干燥装置→收集装置→吸收装置
根据反应物状态及反应条件选择 根据气体及杂质的性质选择干燥剂 根据气体的水溶性及密度选择 根据气体的性质选择吸收剂
10. (2024 重庆,6)某小组用下图中甲作为气体发生装置,其他装置根据实验需求选用(加热及夹持装置略)。下列说法错误的是 (

A.若制取${NH_{3}}$,则$a$为浓氨水,$b$可为氧化钙
B.若制取${Cl_{2}}$,则乙可盛饱和食盐水以除去$HCl$
C.若制取${Cl_{2}}$,则丙可作气体收集装置
D.若制取${NH_{3}}$,则丁可盛水用作尾气处理装置
D
)
A.若制取${NH_{3}}$,则$a$为浓氨水,$b$可为氧化钙
B.若制取${Cl_{2}}$,则乙可盛饱和食盐水以除去$HCl$
C.若制取${Cl_{2}}$,则丙可作气体收集装置
D.若制取${NH_{3}}$,则丁可盛水用作尾气处理装置
答案:
10.D CaO和H₂O反应放出大量的热,促使氨水中的NH₃·H₂O分解释放出NH₃,A正确;Cl₂在饱和食盐水中溶解度很小,且饱和食盐水能吸收HCl,则制取Cl₂,乙可盛饱和食盐水以除去HCl,B正确;Cl₂密度大于空气,则丙中气体长导管进短导管出,可作Cl₂收集装置,C正确;NH₃极易溶于水,容易倒吸,没有防倒吸装置,D错误。
查看更多完整答案,请扫码查看


