2025年5年高考3年模拟高中化学必修第二册苏教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年5年高考3年模拟高中化学必修第二册苏教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第26页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
1. (2025北京,1)我国科研人员在研究嫦娥五号返回器带回的月壤时,发现月壤钛铁矿(${FeTiO_{3}}$)存在亚纳米孔道,吸附并储存了大量来自太阳风的氢原子。加热月壤钛铁矿可生成单质铁和大量水蒸气,水蒸气冷却为液态水储存起来以供使用。下列说法不正确的是 (
A.月壤钛铁矿中存在活泼氢
B.将地球上开采的钛铁矿直接加热也一定生成单质铁和水蒸气
C.月壤钛铁矿加热生成水蒸气的过程中发生了氧化还原反应
D.将获得的水蒸气冷却为液态水的过程会放出热量
B
)A.月壤钛铁矿中存在活泼氢
B.将地球上开采的钛铁矿直接加热也一定生成单质铁和水蒸气
C.月壤钛铁矿加热生成水蒸气的过程中发生了氧化还原反应
D.将获得的水蒸气冷却为液态水的过程会放出热量
答案:
1.B 已知月壤钛铁矿吸附并储存了大量来自太阳风的氢原子,加热月壤钛铁矿后氢原子会与FeTiO₃反应生成单质铁和水蒸气,说明月壤钛铁矿吸附的氢原子较为活泼,A项正确。若地球上开采的钛铁矿中不存在活泼氢,直接加热可能无法生成单质铁和水蒸气,B项错误。氢原子与FeTiO₃反应生成Fe和H₂O,反应中H元素和Fe元素的化合价发生变化,属于氧化还原反应,C项正确。水由气态变为液态时会放出热量,D项正确。
考场速决
钛铁矿(FeTiO₃)中不含氢元素,地球上开采的钛铁矿没有吸附和存储H,将其直接加热不可能得到水蒸气。
考场速决
钛铁矿(FeTiO₃)中不含氢元素,地球上开采的钛铁矿没有吸附和存储H,将其直接加热不可能得到水蒸气。
2. (2023新课标,29改编)氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。根据下图数据计算反应${\dfrac{1}{2}N_{2}(g) + \dfrac{3}{2}H_{2}(g)⇌ NH_{3}(g)}$的$\Delta H=\boldsymbol{$
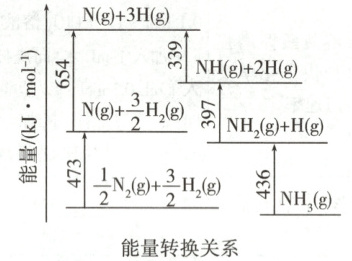
−45
$}\ \mathrm{kJ·\ mol^{-1}}$。
答案:
2.答案−45
解析根据题图,知1/2molN₂(g)和3/2molH₂(g)断键吸收的能量为473kJ+654kJ=1127kJ,形成1molNH₃(g)放出的能量为339kJ+397kJ+436kJ=1172kJ,则ΔH=(1127−1172)kJ·mol⁻¹=−45kJ·mol⁻¹。
名师点津
在高考中,热化学相关知识为高频考点,所占分值不多,难度相对较小,是大部分学生可以得分的点,该题目考查考生对数据的分析和计算能力,只要掌握相关知识,本题不难答出。
解析根据题图,知1/2molN₂(g)和3/2molH₂(g)断键吸收的能量为473kJ+654kJ=1127kJ,形成1molNH₃(g)放出的能量为339kJ+397kJ+436kJ=1172kJ,则ΔH=(1127−1172)kJ·mol⁻¹=−45kJ·mol⁻¹。
名师点津
在高考中,热化学相关知识为高频考点,所占分值不多,难度相对较小,是大部分学生可以得分的点,该题目考查考生对数据的分析和计算能力,只要掌握相关知识,本题不难答出。
3. (2024安徽,12)室温下,为探究纳米铁去除水样中${SeO^{2-}_{4}}$的影响因素,测得不同条件下${SeO^{2-}_{4}}$浓度随时间变化关系如图$^{①}$。
| 实验序号 | 水样体积/mL | 纳米铁质量/mg | 水样初始$pH$ |
| --- | --- | --- | --- |
| ① | $50$ | $8$ | $6$ |
| ② | $50$ | $2$ | $6$ |
| ③ | $50$ | $2$ | $8$ |
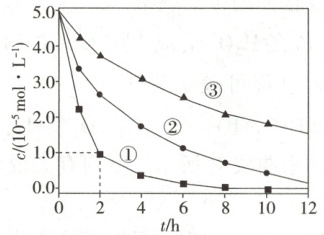
下列说法正确的是 (
A.实验①中,$0\sim2$小时内平均反应速率$v({SeO^{2-}_{4}})=2.0\ \mathrm{mol·\ L^{-1}· h^{-1}}$
B.实验③中,反应的离子方程式为${2Fe + SeO^{2-}_{4} + 8H^{+}\xlongequal{}2Fe^{3+} + Se + 4H_{2}O}$
C.其他条件相同时,适当增加纳米铁质量可加快反应速率
D.其他条件相同时,水样初始$pH$越小,${SeO^{2-}_{4}}$的去除效果越好
| 实验序号 | 水样体积/mL | 纳米铁质量/mg | 水样初始$pH$ |
| --- | --- | --- | --- |
| ① | $50$ | $8$ | $6$ |
| ② | $50$ | $2$ | $6$ |
| ③ | $50$ | $2$ | $8$ |

下列说法正确的是 (
C
)A.实验①中,$0\sim2$小时内平均反应速率$v({SeO^{2-}_{4}})=2.0\ \mathrm{mol·\ L^{-1}· h^{-1}}$
B.实验③中,反应的离子方程式为${2Fe + SeO^{2-}_{4} + 8H^{+}\xlongequal{}2Fe^{3+} + Se + 4H_{2}O}$
C.其他条件相同时,适当增加纳米铁质量可加快反应速率
D.其他条件相同时,水样初始$pH$越小,${SeO^{2-}_{4}}$的去除效果越好
答案:
3.C
真题降维
实验①②相比,只有纳米铁质量不同,实验②③相比,只有水样初始pH不同。
由题图知,实验①中,0~2小时内SeO₄²⁻浓度变化为(5.0−1.0)×10⁻⁵mol·L⁻¹=4.0×10⁻⁵mol·L⁻¹,故v(SeO₄²⁻)=4.0×10⁻⁵mol·L⁻¹/2h=2.0×10⁻⁵mol·L⁻¹·h⁻¹,A错误;实验③的水样初始pH为8,Fe(Ⅲ)在此环境下以Fe(OH)₃形式存在,B错误;由题图知实验①的反应速率大于实验②,实验①的纳米铁质量大,故其他条件相同时,适当增加纳米铁质量可加快反应速率,C正确;其他条件相同时,若水样初始pH太小,H⁺可能会与Fe反应而降低SeO₄²⁻的去除效果,D错误。
名师点睛
解答此类题目的两大关键
(1)控制变量思想:定多变一,即先确定其他因素不变,只变化一种因素,看这种因素与所探究问题存在的关系,再确定另一种;通过分析每种因素与所探究问题之间的关系,得出所有影响因素与所探究问题之间的关系。
(2)分析数据:数据要有效,且变量统一。
真题降维
实验①②相比,只有纳米铁质量不同,实验②③相比,只有水样初始pH不同。
由题图知,实验①中,0~2小时内SeO₄²⁻浓度变化为(5.0−1.0)×10⁻⁵mol·L⁻¹=4.0×10⁻⁵mol·L⁻¹,故v(SeO₄²⁻)=4.0×10⁻⁵mol·L⁻¹/2h=2.0×10⁻⁵mol·L⁻¹·h⁻¹,A错误;实验③的水样初始pH为8,Fe(Ⅲ)在此环境下以Fe(OH)₃形式存在,B错误;由题图知实验①的反应速率大于实验②,实验①的纳米铁质量大,故其他条件相同时,适当增加纳米铁质量可加快反应速率,C正确;其他条件相同时,若水样初始pH太小,H⁺可能会与Fe反应而降低SeO₄²⁻的去除效果,D错误。
名师点睛
解答此类题目的两大关键
(1)控制变量思想:定多变一,即先确定其他因素不变,只变化一种因素,看这种因素与所探究问题存在的关系,再确定另一种;通过分析每种因素与所探究问题之间的关系,得出所有影响因素与所探究问题之间的关系。
(2)分析数据:数据要有效,且变量统一。
4. (2024黑吉辽,10改编)异山梨醇是一种由生物质制备的高附加值化学品,$150\ ^{\circ} C$时其制备过程及相关物质浓度随时间变化如图所示,$15\ \mathrm{h}$后异山梨醇浓度不再变化。下列说法错误的是 (
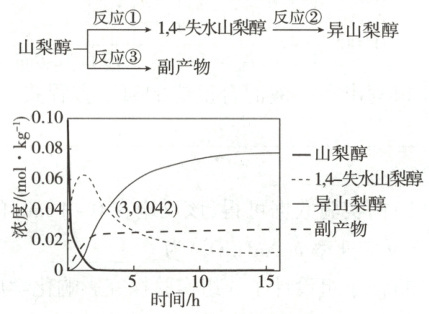
A.$3\ \mathrm{h}$时,反应②正、逆反应速率相等
B.$15\ \mathrm{h}$时反应正向进行程度:①$>$②
C.$0\sim3\ \mathrm{h}$平均速率$v$(异山梨醇)$=0.014\ \mathrm{mol·\ kg^{-1}· h^{-1}}$
D.反应②加入催化剂不改变其平衡转化率
A
)
A.$3\ \mathrm{h}$时,反应②正、逆反应速率相等
B.$15\ \mathrm{h}$时反应正向进行程度:①$>$②
C.$0\sim3\ \mathrm{h}$平均速率$v$(异山梨醇)$=0.014\ \mathrm{mol·\ kg^{-1}· h^{-1}}$
D.反应②加入催化剂不改变其平衡转化率
答案:
4.A 由题图可知,3h时,异山梨醇、1,4−失水山梨醇浓度恰好相等,但是3h后各自浓度仍在发生改变,即3h时反应②未达到平衡状态,正、逆反应速率不相等,A错误;根据15h时山梨醇和1,4−失水山梨醇的浓度可知反应正向进行程度①>②,B正确;0~3h平均速率v(异山梨醇)=0.042mol·kg⁻¹/3h=0.014mol·kg⁻¹·h⁻¹,C正确;催化剂不改变化学平衡转化率,D正确。
查看更多完整答案,请扫码查看


