2025年5年高考3年模拟高中化学必修第二册苏教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年5年高考3年模拟高中化学必修第二册苏教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第12页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
1. (2025 广东茂名化州第一中学期中) 下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是 (
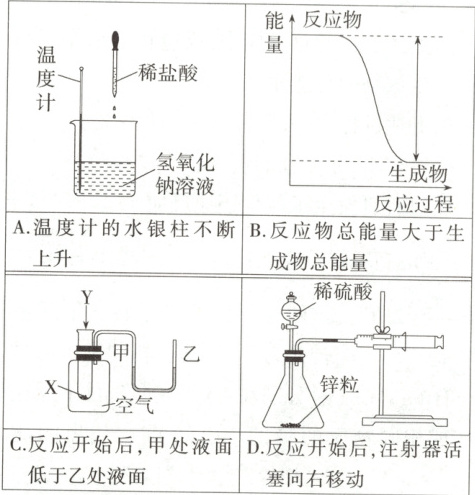
A.温度计的水银柱不断上升
B.反应物总能量大于生成物总能量
C.反应开始后, 甲处液面低于乙处液面
D.反应开始后, 注射器活塞向右移动
D
)
A.温度计的水银柱不断上升
B.反应物总能量大于生成物总能量
C.反应开始后, 甲处液面低于乙处液面
D.反应开始后, 注射器活塞向右移动
答案:
1.D 温度计的水银柱不断上升说明盐酸和氢氧化钠的反应为放热反应,A项不符合题意;该反应反应物总能量大于生成物总能量,为放热反应,B项不符合题意;反应开始后,甲处液面低于乙处液面说明X和Y的反应为放热反应,C项不符合题意;锌与稀硫酸反应生成硫酸锌和氢气,反应生成的氢气会使注射器活塞向右移动,反应开始后,注射器活塞向右移动不能说明锌与稀硫酸的反应为放热反应,D项符合题意。
2. (①易错题) (2024 广西玉林四校联考) 某化学反应包括 A(g) → B(g)、B(g) → C(g) 两步, 整个反应过程中的能量变化如图所示。下列说法正确的是 (
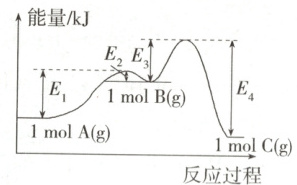
A.两步反应均为吸热反应
B.涉及的三种物质中 C(g) 最稳定
C.1 mol C(g) 与 1 mol A(g) 的能量差为 E₄ kJ
D.反应 A(g) → B(g) 一定要加热才能发生
B
)
A.两步反应均为吸热反应
B.涉及的三种物质中 C(g) 最稳定
C.1 mol C(g) 与 1 mol A(g) 的能量差为 E₄ kJ
D.反应 A(g) → B(g) 一定要加热才能发生
答案:
2.B 由题图可知,反应A(g)→B(g)中反应物总能量小于生成物总能量,为吸热反应,B(g)→C(g)中反应物总能量大于生成物总能量,为放热反应,A项错误;根据题图知,等物质的量的A(g)、B(g)、C(g)中C(g)的能量最低,最稳定,B项正确;根据题图知,1 mol C(g)与1 mol A(g)的能量差为(E₄-E₁+E₂-E₃)kJ,C项错误;反应A(g)→B(g)为吸热反应,但不一定要加热才能发生,D项错误。
易错分析
并不是所有的吸热反应都需要加热才能进行,如Ba(OH)₂·8H₂O晶体与NH₄Cl晶体的反应,常温下就可以进行。
易错分析
并不是所有的吸热反应都需要加热才能进行,如Ba(OH)₂·8H₂O晶体与NH₄Cl晶体的反应,常温下就可以进行。
3. (2025 江苏扬州段考) 某小组利用如图装置探究放热反应和吸热反应。
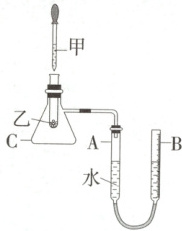
(1) 若一段时间后, A 管液面
(2) 若一段时间后, A 管液面低于 B 管液面, 则以下反应中符合该现象的是
a. 盐酸与烧碱反应
b. 钠和冷水反应
c. 铝和盐酸反应
d. 过氧化钠和水反应

(1) 若一段时间后, A 管液面
高
(填“低”或“高”) 于 B 管液面, 甲和乙可能分别为盐酸和小苏打。(2) 若一段时间后, A 管液面低于 B 管液面, 则以下反应中符合该现象的是
abcd
。a. 盐酸与烧碱反应
b. 钠和冷水反应
c. 铝和盐酸反应
d. 过氧化钠和水反应
答案:
3.答案
(1)高
(2)abcd
解析
(1)盐酸和小苏打的反应为吸热反应,发生该反应导致C内气体温度降低,装置内气体压强变小,一段时间后,A管液面高于B管液面。
(2)A管液面低于B管液面,说明装置内气体压强变大,甲和乙的反应为放热反应,a、b、c、d中反应均为放热反应,均符合题意。
(1)高
(2)abcd
解析
(1)盐酸和小苏打的反应为吸热反应,发生该反应导致C内气体温度降低,装置内气体压强变小,一段时间后,A管液面高于B管液面。
(2)A管液面低于B管液面,说明装置内气体压强变大,甲和乙的反应为放热反应,a、b、c、d中反应均为放热反应,均符合题意。
4. (2025 江苏宿迁段考) N₂(g) 和 O₂(g) 反应生成 NO(g) 过程中的能量变化如图所示。下列说法正确的是 (

A.通常情况下, NO 比 N₂ 稳定
B.2 mol NO(g) 的能量小于 1 mol N₂(g) 和 1 mol O₂(g) 的能量总和
C.N₂(g) + O₂(g) = 2NO(g) ΔH = 180 kJ·mol⁻¹
D.断开 1 mol NO(g) 中化学键需要放出 632 kJ 能量
C
)
A.通常情况下, NO 比 N₂ 稳定
B.2 mol NO(g) 的能量小于 1 mol N₂(g) 和 1 mol O₂(g) 的能量总和
C.N₂(g) + O₂(g) = 2NO(g) ΔH = 180 kJ·mol⁻¹
D.断开 1 mol NO(g) 中化学键需要放出 632 kJ 能量
答案:
4.C 断开1 mol N₂中的共价键消耗946 kJ能量,断开1 mol NO中的共价键消耗632 kJ能量,所以N₂比NO稳定,A错误;断键吸收的总能量大于成键放出的总能量,该反应吸热,2 mol NO(g)的能量大于1 mol N₂(g)和1 mol O₂(g)的能量总和,B错误;焓变=反应物总键能-生成物总键能,N₂(g)+O₂(g)=2NO(g) ΔH=(946+498-632×2) kJ·mol⁻¹ = 180 kJ·mol⁻¹,C正确;断开1 mol NO(g)中化学键需要吸收632 kJ能量,D错误。
5. (2025 湖南岳阳段考) 研究表明, 在一定条件下, 气态 HCN(a) 与 HNC(b) 的互变反应过程能量变化如图所示。下列说法正确的是 (
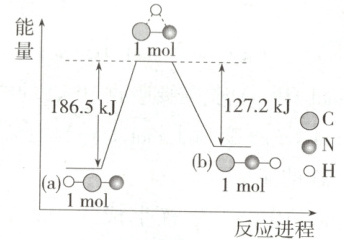
A.HNC(g) 比 HCN(g) 更稳定
B.HCN(g) → HNC(g) 为吸热反应且反应条件一定为加热
参加化学反应的每一种物质内部都贮存着一定的能量。
C.1 mol HCN(g) 中的所有化学键全部断开需要吸收 186.5 kJ 的热量
D.1 mol HCN(g) 转化为 1 mol HNC(g) 需要吸收 59.3 kJ 的热量
D
)
A.HNC(g) 比 HCN(g) 更稳定
B.HCN(g) → HNC(g) 为吸热反应且反应条件一定为加热
参加化学反应的每一种物质内部都贮存着一定的能量。
C.1 mol HCN(g) 中的所有化学键全部断开需要吸收 186.5 kJ 的热量
D.1 mol HCN(g) 转化为 1 mol HNC(g) 需要吸收 59.3 kJ 的热量
答案:
5.D 物质的能量越低越稳定,根据图示可知等物质的量的HCN(g)比HNC(g)的能量低,因此HCN(g)比HNC(g)更稳定,A错误;HCN(g)→HNC(g)为吸热反应,但反应不一定在加热条件下进行,B错误;根据图示可知1 mol HCN(g)转化为中间产物时需吸收186.5 kJ的热量,由于该中间产物中仍然存在化学键,因此1 mol HCN(g)中的所有化学键全部断开需要吸收的热量不是186.5 kJ,C错误;根据图示可知1 mol HCN(g)转化为1 mol HNC(g)需要吸收的热量为186.5 kJ-127.2 kJ=59.3 kJ,D正确。
查看更多完整答案,请扫码查看


