第90页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
1. 根据化学方程式计算的理论基础是
质量守恒
定律,质量守恒定律是一切化学反应都遵守的客观规律。对于一个确定的反应的化学方程式,各反应物和生成物之间的质量比是确定的,这个比值就是各反应物和生成物的相对分子质量
与化学计量数
的乘积之比,它们之间成正比例关系。
答案:
1. 质量守恒 相对分子质量 化学计量数
2. 根据化学方程式计算的一般步骤:
(1)解:设
(2)写出反应的
(3)找出比例关系,写出相关物质的______,以及已知量、未知量。
(4)列出
(5)简明地写出答案。
(1)解:设
未知量
,求什么就设什么。通常用x、y表示,且不写单位
。(2)写出反应的
化学方程式
。(3)找出比例关系,写出相关物质的______,以及已知量、未知量。
(4)列出
比例式
,求解。(5)简明地写出答案。
答案:
2.
(1)未知量 单位
(2)化学方程式
(3)化学计量数与相对分子质量的乘积
(4)比例式
(1)未知量 单位
(2)化学方程式
(3)化学计量数与相对分子质量的乘积
(4)比例式
1. 根据化学方程式进行计算,正确的解题步骤是(
① 正确地写出反应的化学方程式
② 列比例式,求未知量
③ 写出相关物质的化学计量数与相对分子质量的乘积以及已知量、未知量
④ 设未知量
⑤ 简明地写出答案
A.①③④②⑤
B.④①③②⑤
C.①②③④⑤
D.①④③②⑤
B
)① 正确地写出反应的化学方程式
② 列比例式,求未知量
③ 写出相关物质的化学计量数与相对分子质量的乘积以及已知量、未知量
④ 设未知量
⑤ 简明地写出答案
A.①③④②⑤
B.④①③②⑤
C.①②③④⑤
D.①④③②⑤
答案:
1. B
2. 砂子的主要成分是二氧化硅(SiO₂)。人们以砂子为原料,先制成粗硅,然后提纯制成高纯硅,再用高纯硅制造集成电路。生产粗硅的化学反应如下:2C + SiO₂ $\xlongequal{高温}$ Si + 2CO $↑$。
(1)二氧化硅中,硅、氧元素的原子个数比为
(2)生成的Si与CO的质量比为
(3)若所用砂子中SiO₂的质量分数为60%,则200 t砂子中SiO₂的质量为
(1)二氧化硅中,硅、氧元素的原子个数比为
1:2
。(2)生成的Si与CO的质量比为
1:2
。(3)若所用砂子中SiO₂的质量分数为60%,则200 t砂子中SiO₂的质量为
120
t,理论上可生产硅的质量为56
t。
答案:
2.
(1)1:2
(2)1:2
(3)120 56 解析:
(3)200 t砂子中SiO₂的质量为200 t×60% = 120 t。设理论上可生产硅的质量为x。
${2C + SiO_{2}\xlongequal{高温}Si + 2CO\uparrow}$
60 28
120 t x
$\frac{60}{28}=\frac{120\ t}{x}$ $x = 56\ t$
(1)1:2
(2)1:2
(3)120 56 解析:
(3)200 t砂子中SiO₂的质量为200 t×60% = 120 t。设理论上可生产硅的质量为x。
${2C + SiO_{2}\xlongequal{高温}Si + 2CO\uparrow}$
60 28
120 t x
$\frac{60}{28}=\frac{120\ t}{x}$ $x = 56\ t$
3. (2024·大同平城期末)“蛟龙”号是我国研制的大深度载人潜水器。为保证载人潜水器长时间潜水,需要在潜水器里配备供氧装置,利用过氧化物供氧是一种常见的供氧技术。
(1)过氧化钠(Na₂O₂)作供氧剂的化学原理为2Na₂O₂ + 2X = 2Na₂CO₃ + O₂,则反应物X的化学式为
(2)若用上述方法制取16 g氧气,则至少需要Na₂O₂的质量为多少?(写出计算过程)
(1)过氧化钠(Na₂O₂)作供氧剂的化学原理为2Na₂O₂ + 2X = 2Na₂CO₃ + O₂,则反应物X的化学式为
CO₂
。(2)若用上述方法制取16 g氧气,则至少需要Na₂O₂的质量为多少?(写出计算过程)
答案:
3.
(1)CO₂
(2)解:设至少需要Na₂O₂的质量为x。
${2Na_{2}O_{2} + 2CO_{2} = 2Na_{2}CO_{3} + O_{2}}$
156 32
x 16 g
$\frac{156}{32}=\frac{x}{16\ g}$ $x = 78\ g$
答:至少需要Na₂O₂的质量为78 g。
(1)CO₂
(2)解:设至少需要Na₂O₂的质量为x。
${2Na_{2}O_{2} + 2CO_{2} = 2Na_{2}CO_{3} + O_{2}}$
156 32
x 16 g
$\frac{156}{32}=\frac{x}{16\ g}$ $x = 78\ g$
答:至少需要Na₂O₂的质量为78 g。
4. (2024·山西省实验中学期中)兴趣小组用过氧化氢溶液和二氧化锰制取氧气,生成氧气的质量与反应时间的关系如图。
(1)反应生成氧气的质量为
(2)计算参加反应的过氧化氢的质量。
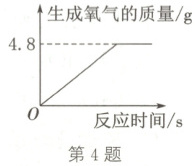
(1)反应生成氧气的质量为
4.8
g。(2)计算参加反应的过氧化氢的质量。

答案:
4.
(1)4.8
(2)解:设参加反应的过氧化氢的质量为x。
${2H_{2}O_{2}\xlongequal{{MnO_{2}}}2H_{2}O + O_{2}\uparrow}$
68 32
x 4.8 g
$\frac{68}{32}=\frac{x}{4.8\ g}$ $x = 10.2\ g$
答:参加反应的过氧化氢的质量为10.2 g。
(1)4.8
(2)解:设参加反应的过氧化氢的质量为x。
${2H_{2}O_{2}\xlongequal{{MnO_{2}}}2H_{2}O + O_{2}\uparrow}$
68 32
x 4.8 g
$\frac{68}{32}=\frac{x}{4.8\ g}$ $x = 10.2\ g$
答:参加反应的过氧化氢的质量为10.2 g。
查看更多完整答案,请扫码查看


