第38页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
6.(2024·临汾期中)下列关于氧气的说法错误的是(
A.鱼类能在水中生活,是因为水中溶解了一定量的氧气
B.氧气在空气中质量分数约为21%
C.自然界能自主弥补氧气的消耗,是因为绿色植物的光合作用
D.包装食品有时抽成真空,是为了避免食品被氧气氧化而变质
B
)A.鱼类能在水中生活,是因为水中溶解了一定量的氧气
B.氧气在空气中质量分数约为21%
C.自然界能自主弥补氧气的消耗,是因为绿色植物的光合作用
D.包装食品有时抽成真空,是为了避免食品被氧气氧化而变质
答案:
6.B
7. 对知识进行回顾与整理是学习化学的重要方法。现有四个反应的文字表达式:
① 镁+氧气$\xrightarrow{点燃}$氧化镁
② 碳+氧气$\xrightarrow{点燃}$二氧化碳
③ 铁+氧气$\xrightarrow{点燃}$四氧化三铁
④ 铜+氧气+水+二氧化碳→碱式碳酸铜
(1)从反应物和生成物的数目看,它们的共同点是______,这类反应属于______反应;再写一个符合这个特点的反应的文字表达式:______。
(2)天然气的主要成分是甲烷,它充分燃烧的文字表达式为甲烷+氧气$\xrightarrow{点燃}$二氧化碳+水。该反应与上述①②③三个反应既有相同点也有不同点,不同点是______;相同点是它们可以归纳为一类反应,即______。
(3)下列化学反应中,属于缓慢氧化的是
A. 木炭燃烧
B. 钢铁生锈
C. 光合作用
D. 呼吸作用
① 镁+氧气$\xrightarrow{点燃}$氧化镁
② 碳+氧气$\xrightarrow{点燃}$二氧化碳
③ 铁+氧气$\xrightarrow{点燃}$四氧化三铁
④ 铜+氧气+水+二氧化碳→碱式碳酸铜
(1)从反应物和生成物的数目看,它们的共同点是______,这类反应属于______反应;再写一个符合这个特点的反应的文字表达式:______。
(2)天然气的主要成分是甲烷,它充分燃烧的文字表达式为甲烷+氧气$\xrightarrow{点燃}$二氧化碳+水。该反应与上述①②③三个反应既有相同点也有不同点,不同点是______;相同点是它们可以归纳为一类反应,即______。
(3)下列化学反应中,属于缓慢氧化的是
BD
(填字母)。A. 木炭燃烧
B. 钢铁生锈
C. 光合作用
D. 呼吸作用
答案:
7.
(1)都是由两种或两种以上物质生成一种物质的反应 化合 红磷+氧气$\stackrel{点燃}{→}$五氧化二磷(合理答案均可)
(2)甲烷充分燃烧的生成物有两种(合理答案即可) 氧化反应
(3)BD
(1)都是由两种或两种以上物质生成一种物质的反应 化合 红磷+氧气$\stackrel{点燃}{→}$五氧化二磷(合理答案均可)
(2)甲烷充分燃烧的生成物有两种(合理答案即可) 氧化反应
(3)BD
8.(2024·晋中祁县期中)化学是一门以实验为基础的科学,化学所取得的丰硕成果与实验的重要作用是分不开的。结合图Ⅰ所示的实验装置图回答问题:
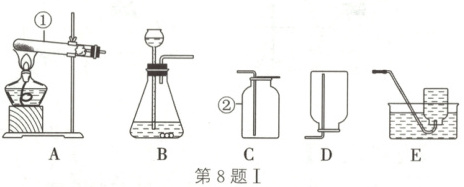
(1)写出指定仪器的名称:①
(2)如图Ⅱ所示的四种途径都可得到氧气:
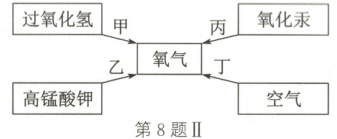
写出实验室中通过乙制取氧气的文字表达式:
化学实验的绿色化就是以绿色化学的理念和原则来指导实验工作。从节能和环保角度考虑,你认为在中学化学实验室中,甲、乙、丙三种制取氧气的途径中,
(3)实验室用高锰酸钾制取氧气时,可采用的发生装置是
(4)实验室用过氧化氢溶液制取氧气时,可选用的发生装置是

(1)写出指定仪器的名称:①
试管
;② 集气瓶
。(2)如图Ⅱ所示的四种途径都可得到氧气:

写出实验室中通过乙制取氧气的文字表达式:
高锰酸钾锰酸钾+二氧化锰+氧气
。化学实验的绿色化就是以绿色化学的理念和原则来指导实验工作。从节能和环保角度考虑,你认为在中学化学实验室中,甲、乙、丙三种制取氧气的途径中,
甲
(填“甲”“乙”或“丙”)途径更体现化学实验的绿色化追求。(3)实验室用高锰酸钾制取氧气时,可采用的发生装置是
A
,用E装置收集氧气当观察到导管口有连续且均匀的气泡冒出
时,开始收集。(4)实验室用过氧化氢溶液制取氧气时,可选用的发生装置是
B
(填字母)。某同学观察到发生装置内有大量气泡时,开始用C装置收集氧气,过一段时间后用带火星的木条伸入瓶口、瓶中和瓶底,都未见木条复燃,其原因是长颈漏斗未液封(或装置漏气)
。
答案:
8.
(1)①试管 ②集气瓶
(2)高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气 甲
(3)A 导管口有连续且均匀的气泡冒出
(4)B 长颈漏斗未液封(或装置漏气)
(1)①试管 ②集气瓶
(2)高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气 甲
(3)A 导管口有连续且均匀的气泡冒出
(4)B 长颈漏斗未液封(或装置漏气)
9. 某化学小组对如下两个实验进行了探究。回答下列问题:
实验一:混制“富氧空气”。
(1)用纯氮气及氧气混制一瓶(集气瓶容积为250mL)氧气体积分数为40%的“富氧空气”,可使用如图所示装置,先在装置中装满水,再从导管______(填“a”或“b”)通入氮气,排出______mL水,然后再通入氧气排出80mL水。

实验二:探究氧化铁能否作过氧化氢分解的催化剂。
(2)取一定量的过氧化氢溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,木条没有复燃,说明
(3)在(2)的试管中加入$Wg$氧化铁粉末,有大量气泡产生,然后伸入带火星的木条,木条复燃,说明
(4)待反应结束后,将试管里的不溶物滤出,并洗涤、干燥、称量,固体质量仍为$Wg$,说明
【实验结论】A同学认为,氧化铁粉末可以作为过氧化氢分解的催化剂。
(5)B同学认为要证明A同学的结论正确,仅做以上实验还不充分,需要再补充一个探究实验。该实验是______(写出实验操作、现象、结论)。
实验一:混制“富氧空气”。
(1)用纯氮气及氧气混制一瓶(集气瓶容积为250mL)氧气体积分数为40%的“富氧空气”,可使用如图所示装置,先在装置中装满水,再从导管______(填“a”或“b”)通入氮气,排出______mL水,然后再通入氧气排出80mL水。

实验二:探究氧化铁能否作过氧化氢分解的催化剂。
(2)取一定量的过氧化氢溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,木条没有复燃,说明
过氧化氢溶液常温下分解缓慢
。(3)在(2)的试管中加入$Wg$氧化铁粉末,有大量气泡产生,然后伸入带火星的木条,木条复燃,说明
氧化铁加快了过氧化氢分解的速率
。(4)待反应结束后,将试管里的不溶物滤出,并洗涤、干燥、称量,固体质量仍为$Wg$,说明
反应前后氧化铁质量不变
。【实验结论】A同学认为,氧化铁粉末可以作为过氧化氢分解的催化剂。
(5)B同学认为要证明A同学的结论正确,仅做以上实验还不充分,需要再补充一个探究实验。该实验是______(写出实验操作、现象、结论)。
答案:
9.
(1)b 120
(2)过氧化氢溶液常温下分解缓慢
(3)氧化铁加快了过氧化氢分解的速率
(4)反应前后氧化铁质量不变
(5)向试管中加入少量过氧化氢溶液,加入
(4)中的固体,有大量气泡产生,然后伸入带火星的木条,木条复燃,说明反应前后氧化铁的化学性质不变。 解析:
(1)在装置中装满水后,应从导管b通入氮气,设通入氮气排出水的体积为x,则$\frac{80mL}{x+80mL}×100\%=40\%,$解得x=120mL。
(2)取一定量的过氧化氢溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,木条没有复燃,说明过氧化氢溶液常温下分解缓慢。
(3)在
(2)的试管中加入Wg氧化铁粉末,有大量气泡产生,然后伸入带火星的木条,木条复燃,说明加入氧化铁后产生氧气的速率加快了很多,说明氧化铁加快了过氧化氢分解的速率。
(4)反应结束后将试管里的不溶物滤出,并洗涤、干燥、称量,固体质量仍为Wg,说明反应前后氧化铁质量不变。
(5)催化剂在反应前后本身质量和化学性质都不变,所以不仅要证明反应前后氧化铁质量不变,还需要证明化学性质不变,向试管中加入少量过氧化氢溶液,加入
(4)中的固体,有大量气泡产生,然后伸入带火星的木条,木条复燃,说明反应前后氧化铁的化学性质不变。
(1)b 120
(2)过氧化氢溶液常温下分解缓慢
(3)氧化铁加快了过氧化氢分解的速率
(4)反应前后氧化铁质量不变
(5)向试管中加入少量过氧化氢溶液,加入
(4)中的固体,有大量气泡产生,然后伸入带火星的木条,木条复燃,说明反应前后氧化铁的化学性质不变。 解析:
(1)在装置中装满水后,应从导管b通入氮气,设通入氮气排出水的体积为x,则$\frac{80mL}{x+80mL}×100\%=40\%,$解得x=120mL。
(2)取一定量的过氧化氢溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,木条没有复燃,说明过氧化氢溶液常温下分解缓慢。
(3)在
(2)的试管中加入Wg氧化铁粉末,有大量气泡产生,然后伸入带火星的木条,木条复燃,说明加入氧化铁后产生氧气的速率加快了很多,说明氧化铁加快了过氧化氢分解的速率。
(4)反应结束后将试管里的不溶物滤出,并洗涤、干燥、称量,固体质量仍为Wg,说明反应前后氧化铁质量不变。
(5)催化剂在反应前后本身质量和化学性质都不变,所以不仅要证明反应前后氧化铁质量不变,还需要证明化学性质不变,向试管中加入少量过氧化氢溶液,加入
(4)中的固体,有大量气泡产生,然后伸入带火星的木条,木条复燃,说明反应前后氧化铁的化学性质不变。
查看更多完整答案,请扫码查看


