第59页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
17. 氮化镓是制造芯片的材料之一,图甲是镓元素(元素符号为$Ga$)的原子结构示意图,图乙是元素周期表的一部分。下列说法错误的是(
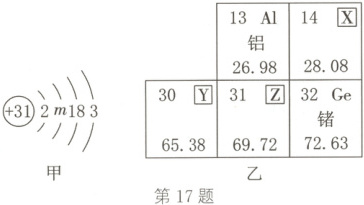
A.图甲中,$m = 8$
B.图乙中,$Z$为$Ga$
C.锗原子中有$4$个电子层
D.$Ga$与$Al$的原子的核外电子数相同
D
)
A.图甲中,$m = 8$
B.图乙中,$Z$为$Ga$
C.锗原子中有$4$个电子层
D.$Ga$与$Al$的原子的核外电子数相同
答案:
17.D
18. 如图是某化学反应的微观示意图,其中“○”和“●”表示不同元素的原子。下列说法错误的是(
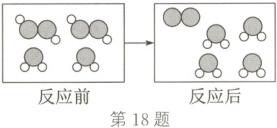
A.该反应涉及$3$种物质
B.生成物的分子个数比为$1:4$
C.体现了化学反应中分子可分,原子不可再分
D.该反应属于分解反应
B
)
A.该反应涉及$3$种物质
B.生成物的分子个数比为$1:4$
C.体现了化学反应中分子可分,原子不可再分
D.该反应属于分解反应
答案:
18.B
19. “青花瓷”在中国瓷器中是最具代表性的。绘制青花瓷纹饰的原料中主要含有氧化钴()。在元素周期表中钴元素与铁元素同位于第Ⅷ族。如图是它们在元素周期表中的位置及原子结构示意图,回答下列问题:
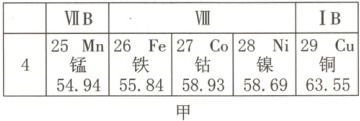
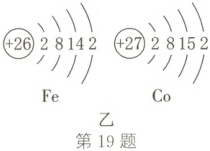
(1)图甲中元素都在第
(2)图乙中铁元素与钴元素化学性质相似,其原因是
(3)钴也能在氧气中燃烧生成四氧化三钴,该反应的文字表达式为


(1)图甲中元素都在第
4
周期,都是金属
(填“金属”或“非金属”)元素,根据图甲信息,镍元素的相对原子质量是58.69
。铁原子的结构示意图如图乙,在化学反应中易失去
(填“得到”或“失去”)电子。(2)图乙中铁元素与钴元素化学性质相似,其原因是
最外层电子数相同
。(3)钴也能在氧气中燃烧生成四氧化三钴,该反应的文字表达式为
钴+氧气\overset{点燃}{\longrightarrow}四氧化三钴
。
答案:
19.(1)4 金属 58.69 失去 (2)最外层电子数相同 (3)钴+氧气$\overset{点燃}{\longrightarrow}$四氧化三钴
20. 如图所示为元素周期表的一部分,请分析图中信息回答下列问题:
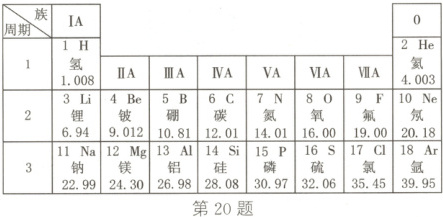
(1)磷元素的相对原子质量为
(2)在元素周期表中,氪元素排在氩元素的正下方,推测氪气的化学性质比较
(3)研究表明:在同一周期中,除稀有气体元素外,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强。由此推断:第周期中得电子能力最强的是
(4)某元素的原子结构示意图为,则它位于元素周期表中的第

(1)磷元素的相对原子质量为
30.97
,该元素属于非金属
(填“金属”或“非金属”)元素;根据元素周期表中的信息,不能
(填“能”或“不能”)得出磷原子的中子数。(2)在元素周期表中,氪元素排在氩元素的正下方,推测氪气的化学性质比较
稳定
(填“活泼”或“稳定”),从原子结构上分析,其原因是原子的最外层电子数是8,达到相对稳定结构
。(3)研究表明:在同一周期中,除稀有气体元素外,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强。由此推断:第周期中得电子能力最强的是
氟(或F)
原子,失电子能力最强的是锂(或Li)
原子,具有相对稳定结构的是氖(或Ne)
原子。(4)某元素的原子结构示意图为,则它位于元素周期表中的第
5
周期,该元素的化学性质与图中第ⅦA
族元素的化学性质相似。
答案:
20.(1)30.97 非金属 不能 (2)稳定 原子的最外层电子数是8,达到相对稳定结构 (3)氟(或F) 锂(或Li) 氖(或Ne) (4)5 ⅦA 解析:(4)同周期的元素原子核外电子层数相同,且周期数等于电子层数。由该元素的原子结构示意图可知,该元素位于元素周期表中的第5周期,该元素原子核的最外层有7个电子,所以其化学性质与第ⅦA族元素的化学性质相似。
查看更多完整答案,请扫码查看


