第76页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
21. (12分)(2023·云南节选)“乌铜走银”是云南省石屏县始创的一种独特的铜制工艺品技艺,迄今已有300余年的历史。
(1)乌铜是一种合金,其硬度比纯铜的
(2)“乌铜走银”的技艺是在乌铜上雕刻各种图案,然后将熔化的银水填入图案中,冷却后打磨光滑。银长时间放置后依然光亮,原因是
(3)乌铜表面的黑色物质主要是氧化铜。利用稀硫酸和铁从氧化铜中得到铜单质可通过以下两种方案实现。
方案一$:Fe\xrightarrow{H_2SO_4}H_2\xrightarrow[△]{CuO}Cu方案二:CuO\xrightarrow{H_2SO_4}CuSO_4\xrightarrow{Fe}Cu①$上述两种方案中较优的是
②西汉刘安所著《淮南万毕术》中提到“曾青得铁则化为铜”,方案二中体现这一过程的化学方程式为
(1)乌铜是一种合金,其硬度比纯铜的
大
(填“大”或“小”);乌铜经锻打、碾压可做成不同厚度的乌铜片,说明乌铜具有良好的延展性
。(2)“乌铜走银”的技艺是在乌铜上雕刻各种图案,然后将熔化的银水填入图案中,冷却后打磨光滑。银长时间放置后依然光亮,原因是
银的化学性质稳定
。(3)乌铜表面的黑色物质主要是氧化铜。利用稀硫酸和铁从氧化铜中得到铜单质可通过以下两种方案实现。
方案一$:Fe\xrightarrow{H_2SO_4}H_2\xrightarrow[△]{CuO}Cu方案二:CuO\xrightarrow{H_2SO_4}CuSO_4\xrightarrow{Fe}Cu①$上述两种方案中较优的是
方案二
,理由是不需要加热,操作方便安全,且节省原料
。②西汉刘安所著《淮南万毕术》中提到“曾青得铁则化为铜”,方案二中体现这一过程的化学方程式为
$\mathrm{F}\mathrm{e}+\mathrm{C}\mathrm{u}\mathrm{S}{\mathrm{O}}_{4}\xlongequal{\;\;}\mathrm{C}\mathrm{u}+\mathrm{F}\mathrm{e}\mathrm{S}{\mathrm{O}}_{4}$
。
答案:
(1)大 延展性 (2)银的化学性质稳定(3)① 方案二 不需要加热,操作方便安全,且节省原料 ② $\mathrm{F}\mathrm{e}+\mathrm{C}\mathrm{u}\mathrm{S}{\mathrm{O}}_{4}\xlongequal{\;\;}\mathrm{C}\mathrm{u}+\mathrm{F}\mathrm{e}\mathrm{S}{\mathrm{O}}_{4}$
22. (12分)(2025·河北衡水期末改编)某小组的同学对炼铁高炉中发生的主要反应进行了知识网络建构,各物质之间的转化关系如图所示(反应条件已略去)。A~H是初中化学常见物质,其中B、D、G为高炉炼铁原料的主要成分,且G为红棕色氧化物。请回答下列问题。
(1)G的化学式为______
(2)反应②的基本反应类型为______
(3)反应③的化学方程式为______
(4)反应①和③在高炉炼铁中的作用分别是______
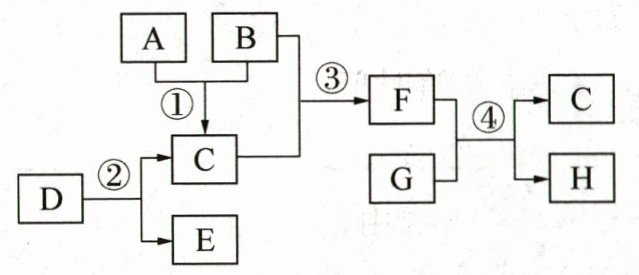
(1)G的化学式为______
$\mathrm{F}{\mathrm{e}}_{2}{\mathrm{O}}_{3}$
。(2)反应②的基本反应类型为______
分解反应
。(3)反应③的化学方程式为______
$\mathrm{C}{\mathrm{O}}_{2}+\mathrm{C}\xlongequal{\text{高温}}2\mathrm{C}\mathrm{O}$
;反应④的化学方程式为______$\mathrm{F}{\mathrm{e}}_{2}{\mathrm{O}}_{3}+3\mathrm{C}\mathrm{O}\xlongequal{\text{高温}}2\mathrm{F}\mathrm{e}+3\mathrm{C}{\mathrm{O}}_{2}$
。(4)反应①和③在高炉炼铁中的作用分别是______
提供反应所需热量
、______提供还原性物质一氧化碳
。
答案:
(1)$\mathrm{F}{\mathrm{e}}_{2}{\mathrm{O}}_{3}$(2)分解反应 (3)$\mathrm{C}{\mathrm{O}}_{2}+\mathrm{C}\xlongequal{\text{高温}}2\mathrm{C}\mathrm{O}$$\mathrm{F}{\mathrm{e}}_{2}{\mathrm{O}}_{3}+3\mathrm{C}\mathrm{O}\xlongequal{\text{高温}}2\mathrm{F}\mathrm{e}+3\mathrm{C}{\mathrm{O}}_{2}$(4)提供反应所需热量 提供还原性物质一氧化碳解析:A~H是初中化学常见物质。B、D、G为高炉炼铁原料的主要成分,且G为红棕色氧化物,则G是氧化铁。A、B能转化成C,B、C能转化成F,F能与氧化铁反应,则A是氧气,B是碳,C是二氧化碳,F是一氧化碳。一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,则H是铁。D为高炉炼铁原料的主要成分,D能转化成二氧化碳和E,则D是碳酸钙,E是氧化钙。经过验证,推导正确。
23. 新趋势 创新实验 (18分)金属是现代社会广泛使用的材料。
Ⅰ. 人类使用金属的大致历史年代如图所示。
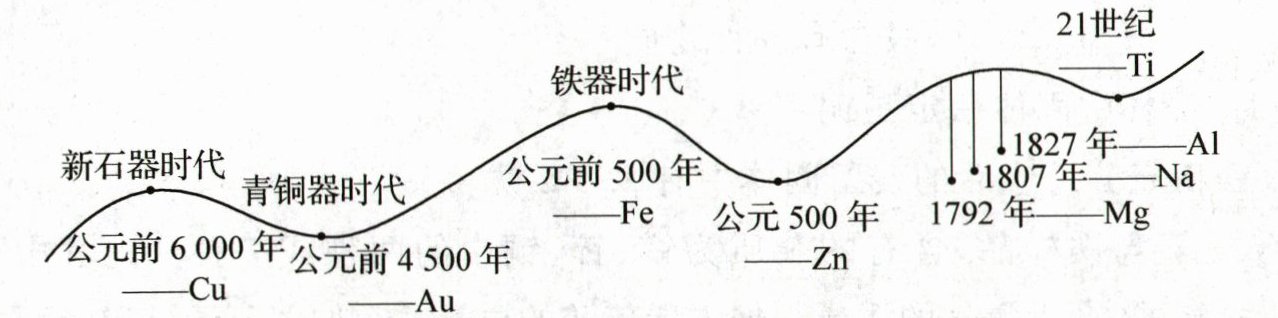
(1)明代宋应星所著的《天工开物》中有煅烧炉甘石$(ZnCO_3)$和煤炭(C)炼锌的记载,写出该反应的化学方程式:
(2)金属铝在空气中有“自我保护”能力的原因是
Ⅱ. 探究金属铁锈蚀的条件(如图所示)。
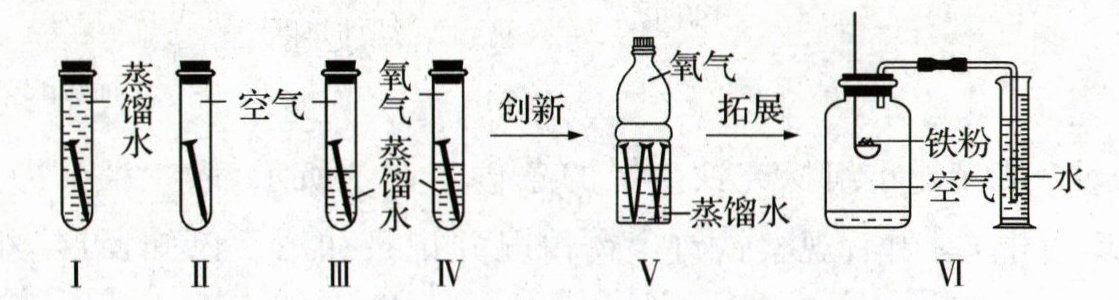
(3)实验Ⅴ在软塑料瓶中完成,一周后可观察到铁钉生锈,软塑料瓶变瘪,靠近水面附近的部分铁钉锈蚀得最厉害。由此可知:铁生锈实际是铁与
(4)对比分析实验Ⅲ、Ⅳ可知,铁生锈速率与
(5)实验Ⅵ还可用来完成
Ⅲ. 探究金属的冶炼。
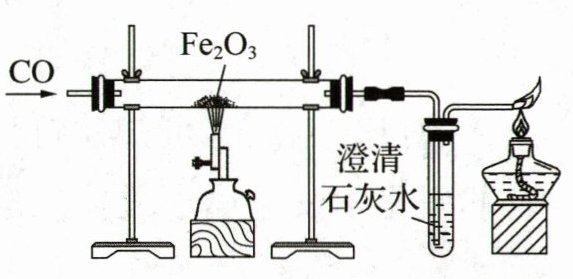
(6)如图为化学实验室模拟炼铁的实验装置图,该装置中酒精灯的作用是
Ⅰ. 人类使用金属的大致历史年代如图所示。

(1)明代宋应星所著的《天工开物》中有煅烧炉甘石$(ZnCO_3)$和煤炭(C)炼锌的记载,写出该反应的化学方程式:
$\mathrm{Z}\mathrm{n}\mathrm{C}{\mathrm{O}}_{3}+2\mathrm{C}\xlongequal{\text{高温}}\mathrm{Z}\mathrm{n}+3\mathrm{C}\mathrm{O}\uparrow$
。(2)金属铝在空气中有“自我保护”能力的原因是
$4\mathrm{A}\mathrm{l}+3{\mathrm{O}}_{2}\xlongequal{\;\;}2\mathrm{A}{\mathrm{l}}_{2}{\mathrm{O}}_{3}$
(用化学方程式表示)。Ⅱ. 探究金属铁锈蚀的条件(如图所示)。

(3)实验Ⅴ在软塑料瓶中完成,一周后可观察到铁钉生锈,软塑料瓶变瘪,靠近水面附近的部分铁钉锈蚀得最厉害。由此可知:铁生锈实际是铁与
${\mathrm{O}}_{2}$、${\mathrm{H}}_{2}\mathrm{O}$
(填化学式)共同作用的结果,请写出一种防锈措施:保持铁制品表面洁净干燥(或刷漆、涂油等,答案合理即可)
。(4)对比分析实验Ⅲ、Ⅳ可知,铁生锈速率与
氧气的浓度
有关。(5)实验Ⅵ还可用来完成
测定空气中氧气的含量
(填实验名称)。Ⅲ. 探究金属的冶炼。
(6)如图为化学实验室模拟炼铁的实验装置图,该装置中酒精灯的作用是
进行尾气处理
,写出试管中发生反应的化学方程式:$\mathrm{C}{\mathrm{O}}_{2}+\mathrm{C}\mathrm{a}(\mathrm{O}\mathrm{H}{)}_{2}\xlongequal{\;\;}\mathrm{C}\mathrm{a}\mathrm{C}{\mathrm{O}}_{3}\downarrow +{\mathrm{H}}_{2}\mathrm{O}$
,反应前后固体减小的质量小于
(填“大于”“小于”或“等于”)生成的二氧化碳中氧元素的质量。
答案:
(1)$\mathrm{Z}\mathrm{n}\mathrm{C}{\mathrm{O}}_{3}+2\mathrm{C}\xlongequal{\text{高温}}\mathrm{Z}\mathrm{n}+3\mathrm{C}\mathrm{O}\uparrow$(2)$4\mathrm{A}\mathrm{l}+3{\mathrm{O}}_{2}\xlongequal{\;\;}2\mathrm{A}{\mathrm{l}}_{2}{\mathrm{O}}_{3}$(3)${\mathrm{O}}_{2}$、${\mathrm{H}}_{2}\mathrm{O}$保持铁制品表面洁净干燥(或刷漆、涂油等,答案合理即可)(4)氧气的浓度(5)测定空气中氧气的含量(6)进行尾气处理$\mathrm{C}{\mathrm{O}}_{2}+\mathrm{C}\mathrm{a}(\mathrm{O}\mathrm{H}{)}_{2}\xlongequal{\;\;}\mathrm{C}\mathrm{a}\mathrm{C}{\mathrm{O}}_{3}\downarrow +{\mathrm{H}}_{2}\mathrm{O}$小于解析:
(6)反应前固体为氧化铁,反应后固体为铁,故反应前后固体减小的质量为氧元素的质量,二氧化碳中的氧元素一部分来自一氧化碳,另一部分来自氧化铁,故反应前后固体减小的质量小于生成的二氧化碳中氧元素的质量。
(6)反应前固体为氧化铁,反应后固体为铁,故反应前后固体减小的质量为氧元素的质量,二氧化碳中的氧元素一部分来自一氧化碳,另一部分来自氧化铁,故反应前后固体减小的质量小于生成的二氧化碳中氧元素的质量。
查看更多完整答案,请扫码查看


