第92页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
10. 已知:H_2 + CuO $\xlongequal{\triangle}$ Cu + H_2O。有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜(Cu_2O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液。某兴趣小组对此开展如下探究。
Ⅰ. 设计如图所示实验装置,开展氢气还原氧化铜实验并检验固体产物。
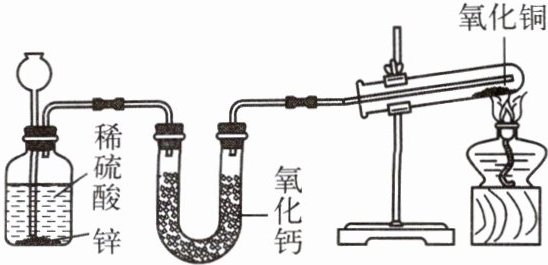
(1)制取氢气的化学方程式为______。
(2)氧化钙的作用是______。
(3)取反应后的红色固体于烧杯中,加入氨水并搅拌,观察到______,证明固体产物有Cu_2O。
Ⅱ. 探究反应生成Cu_2O的变化情况。
称取若干份质量均为0.6000g的CuO,在相同条件下分别用氢气还原不同时间(t),检测所得固体中Cu_2O的质量(m),结果如图所示。
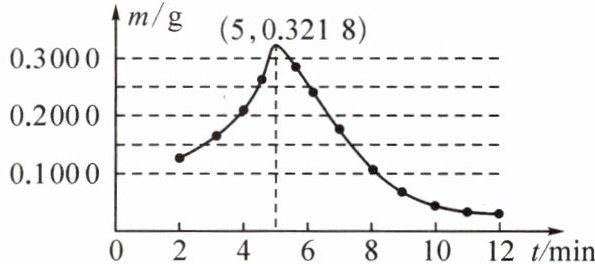
(4)由图可知,在氢气还原氧化铜的反应过程中,Cu_2O质量的变化趋势是______。
(5)为确保氢气还原氧化铜所得固体产物不含Cu_2O,应采取的措施是______。
Ⅲ. 探究反应生成Cu_2O的原因。
为解释实验结果,兴趣小组对氢气还原氧化铜的反应过程提出如下假设:
假设1. 经历2CuO + H_2 $\xlongequal{\triangle}$ Cu_2O + H_2O、H_2 + Cu_2O $\xlongequal{\triangle}$ 2Cu + H_2O两个反应,且在同一条件下两个反应同时进行。
假设2. 先后经历CuO + H_2 $\xlongequal{\triangle}$ Cu + H_2O、Cu + CuO $\xlongequal{\triangle}$ Cu_2O、H_2 + Cu_2O $\xlongequal{\triangle}$ 2Cu + H_2O三个反应。
(6)结合探究Ⅱ结果计算分析,假设1中“在同一条件下两个反应能同时进行”合理的依据是______。
(7)若要确认“假设2”是否合理,在探究Ⅱ的基础上,还需进行的实验是______。
Ⅰ. 设计如图所示实验装置,开展氢气还原氧化铜实验并检验固体产物。

(1)制取氢气的化学方程式为______。
(2)氧化钙的作用是______。
(3)取反应后的红色固体于烧杯中,加入氨水并搅拌,观察到______,证明固体产物有Cu_2O。
Ⅱ. 探究反应生成Cu_2O的变化情况。
称取若干份质量均为0.6000g的CuO,在相同条件下分别用氢气还原不同时间(t),检测所得固体中Cu_2O的质量(m),结果如图所示。

(4)由图可知,在氢气还原氧化铜的反应过程中,Cu_2O质量的变化趋势是______。
(5)为确保氢气还原氧化铜所得固体产物不含Cu_2O,应采取的措施是______。
Ⅲ. 探究反应生成Cu_2O的原因。
为解释实验结果,兴趣小组对氢气还原氧化铜的反应过程提出如下假设:
假设1. 经历2CuO + H_2 $\xlongequal{\triangle}$ Cu_2O + H_2O、H_2 + Cu_2O $\xlongequal{\triangle}$ 2Cu + H_2O两个反应,且在同一条件下两个反应同时进行。
假设2. 先后经历CuO + H_2 $\xlongequal{\triangle}$ Cu + H_2O、Cu + CuO $\xlongequal{\triangle}$ Cu_2O、H_2 + Cu_2O $\xlongequal{\triangle}$ 2Cu + H_2O三个反应。
(6)结合探究Ⅱ结果计算分析,假设1中“在同一条件下两个反应能同时进行”合理的依据是______。
(7)若要确认“假设2”是否合理,在探究Ⅱ的基础上,还需进行的实验是______。
答案:
Ⅰ.
(1)${Zn + H2SO4\xlongequal{}ZnSO4 + H2\uparrow}$
(2)除去氢气中混有的水蒸气
(3)溶液变蓝色 Ⅱ.
(4)$5\ \text{min}$之前氧化亚铜的质量增大,$5\ \text{min}$之后氧化亚铜的质量减小
(5)延长加热时间 Ⅲ.
(6)$0.6000\ \text{g}\ {CuO}$中${Cu}$元素质量为$0.48\ \text{g}$,若先生成氧化亚铜,氧化亚铜质量的最大值一定大于$0.48\ \text{g}$,不会是$0.3218\ \text{g}$
(7)刚开始反应一段时间后,取样,滴加氨水,观察溶液是否变蓝
(1)${Zn + H2SO4\xlongequal{}ZnSO4 + H2\uparrow}$
(2)除去氢气中混有的水蒸气
(3)溶液变蓝色 Ⅱ.
(4)$5\ \text{min}$之前氧化亚铜的质量增大,$5\ \text{min}$之后氧化亚铜的质量减小
(5)延长加热时间 Ⅲ.
(6)$0.6000\ \text{g}\ {CuO}$中${Cu}$元素质量为$0.48\ \text{g}$,若先生成氧化亚铜,氧化亚铜质量的最大值一定大于$0.48\ \text{g}$,不会是$0.3218\ \text{g}$
(7)刚开始反应一段时间后,取样,滴加氨水,观察溶液是否变蓝
查看更多完整答案,请扫码查看


