第13页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
1. 如图所示为大自然中的氧循环示意图,下列说法错误的是 (
A.氧循环过程中发生的是化学变化
B.物质燃烧说明氧气能支持燃烧,说明氧气具有可燃性
C.食物腐败发生的是缓慢氧化反应
D.氧气能供给动植物呼吸,是一种重要的资源
B
)A.氧循环过程中发生的是化学变化
B.物质燃烧说明氧气能支持燃烧,说明氧气具有可燃性
C.食物腐败发生的是缓慢氧化反应
D.氧气能供给动植物呼吸,是一种重要的资源
答案:
B
2. (娄底中考)认真观察、准确记录和仔细分析实验现象是学习化学的重要方法。下列有关实验现象的描述不正确的是 (
A.红磷在空气中燃烧产生大量的白烟
B.细铁丝在氧气中燃烧,火星四射,生成黑色固体
C.木炭在氧气中燃烧发出白光,生成能使澄清石灰水变浑浊的气体
D.镁条在空气中燃烧发出耀眼的白光,生成氧化镁
D
)A.红磷在空气中燃烧产生大量的白烟
B.细铁丝在氧气中燃烧,火星四射,生成黑色固体
C.木炭在氧气中燃烧发出白光,生成能使澄清石灰水变浑浊的气体
D.镁条在空气中燃烧发出耀眼的白光,生成氧化镁
答案:
D
3. (2024·南通如皋月考)如图所示,如果用一个圆表示化合反应,另一个圆表示氧化反应,下列各选项中,属于图中“A”区域的是 (
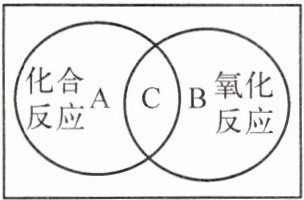
A.氧化汞$\xrightarrow{加热}$汞+氧气
B.碳+氧气$\xrightarrow{点燃}$二氧化碳
C.石蜡+氧气$\xrightarrow{点燃}$二氧化碳+水
D.二氧化碳+水→碳酸
D
)
A.氧化汞$\xrightarrow{加热}$汞+氧气
B.碳+氧气$\xrightarrow{点燃}$二氧化碳
C.石蜡+氧气$\xrightarrow{点燃}$二氧化碳+水
D.二氧化碳+水→碳酸
答案:
D
4. 如图所示装置(不可倒置)有多种用途,下列叙述正确的是 (
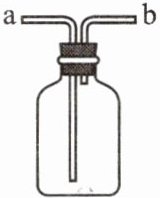
A.若用排空气法收集$O_2,$气体从b端通入
B.若用排水法收集$O_2,$气体从b端通入
C.干燥$CO_2$可在装置中装入浓硫酸(具有吸水性),气体从b端通入
D.若用水将此装置中的$O_2$排出,水应当从b端进入
B
)
A.若用排空气法收集$O_2,$气体从b端通入
B.若用排水法收集$O_2,$气体从b端通入
C.干燥$CO_2$可在装置中装入浓硫酸(具有吸水性),气体从b端通入
D.若用水将此装置中的$O_2$排出,水应当从b端进入
答案:
B 提示:若用排空气法收集气体,密度比空气大的气体从长管通入,密度比空气小的气体从短管通入;若用排水法收集O₂,瓶内先装满水,气体从装置b端通入,将水从a端排出;用浓硫酸干燥气体时,被干燥的气体应通入浓硫酸中,气体应从a端通入;用水将装置中的O₂排出,水应该从长管a端进入,气体从短管b端排出。
5. (无锡惠山期中)某同学误将少量$KMnO_4$当成$MnO_2$加入$KClO_3$中进行加热制取氧气,部分物质质量随时间变化如图所示。下列关于该过程的说法正确的是 (
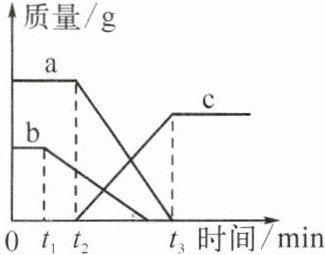
A.c代表氧气
B.t_1min,KMnO_4$开始分解$
$C.t_2min,$开始有$MnO_2$生成
D.高锰酸钾是氯酸钾分解的催化剂
B
)
A.c代表氧气
B.t_1min,KMnO_4$开始分解$
$C.t_2min,$开始有$MnO_2$生成
D.高锰酸钾是氯酸钾分解的催化剂
答案:
B 提示:由图可知,一开始a的质量多,b的质量少,且两者质量均随时间的增加而减少,所以a代表KClO₃,b代表KMnO₄。t₁min KMnO₄分解就有氧气产生,故c不代表氧气,a(KClO₃)分解后立即产生c,说明c代表KCl;t₁min KMnO₄开始分解产生氧气,同时生成二氧化锰;高锰酸钾分解产生的二氧化锰是氯酸钾分解的催化剂。
Ⅰ. 分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的$FeCl_3$溶液,观察
Ⅱ. 为进一步判断上述实验结论的准确性,用如图所示装置,小刚同学进行了如下所示实验方案设计。
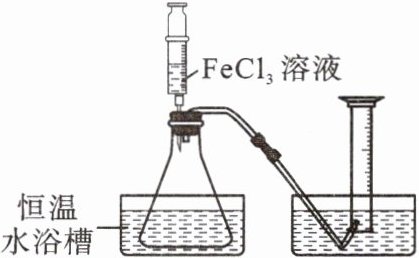
方案一:在不同过氧化氢浓度下,测定收集相同气体体积所需时间。
方案二:在不同过氧化氢浓度下,测定
方案二的实验测量结果如下表所示:
|物理量|实验序号|
| |1|2|
|$30%H_2O_2$溶液的体积/mL|5|10|
|$2%FeCl_3$溶液的体积/mL|
|加入$H_2O$的体积/mL|20|15|
|反应的时间/min|5|
|生成$O_2$的体积/mL|$V_1$|$V_2$|
表中x=
实验结论:通过测量,若$V_1$
产生气泡的快慢
,就可以粗略判断,得出实验结果。Ⅱ. 为进一步判断上述实验结论的准确性,用如图所示装置,小刚同学进行了如下所示实验方案设计。

方案一:在不同过氧化氢浓度下,测定收集相同气体体积所需时间。
方案二:在不同过氧化氢浓度下,测定
相同时间内收集到的气体体积
。方案二的实验测量结果如下表所示:
|物理量|实验序号|
| |1|2|
|$30%H_2O_2$溶液的体积/mL|5|10|
|$2%FeCl_3$溶液的体积/mL|
3
|3||加入$H_2O$的体积/mL|20|15|
|反应的时间/min|5|
5
||生成$O_2$的体积/mL|$V_1$|$V_2$|
表中x=
3
,y=5
。实验结论:通过测量,若$V_1$
<
(填“>”“=”或$“<”)V_2,$说明相同的反应时间内,过氧化氢浓度越大,分解速率越快
。
答案:
Ⅰ. 产生气泡的快慢 Ⅱ. 相同时间内收集到的气体体积 3 5 < 相同的反应时间内,过氧化氢浓度越大,分解速率越快
查看更多完整答案,请扫码查看


