第23页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
1. (2025·怒江期末)化学学习小组的同学们开展跨学科实践活动,利用塑料瓶、注射器、吸管、输液管等设计并制作了如图所示的简易供氧装置,向右侧瓶中装入适量的水,向左侧瓶中加入制氧试剂,下列有关说法中不正确的是 (
A. 该装置可根据需要调节氧气流量
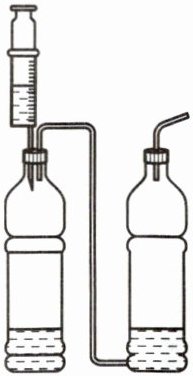
B. 左侧瓶中加入的制氧试剂是高锰酸钾
C. 右侧瓶中的水有除杂、降温的作用
D. 设计供氧器需要综合考虑便捷、安全、环保等因素
2. 化学学习要求大家能有意识地应用化学知识,自主调用物理、数学等多个学科的相关知识,参与实践活动,不断改进,提升解决问题的能力。用鱼缸养鱼时要定期供氧。某化学兴趣小组的同学决定利用所学化学知识“设计和制作简易供氧器”,给鱼缸提供氧气。
(1) 实验室里一般不能制得氧气的物质是______(填字母)。
A. 高锰酸钾($KMnO_{4}$) B. 氯酸钾($KClO_{3}$)
C. 氯化钠($NaCl$) D. 过氧化氢($H_{2}O_{2}$)
(2) 同学们综合考虑了成本、环保、安全等因素后,决定利用$H_{2}O_{2}$溶液制备氧气的原理给鱼缸暂时供氧。请回答下列问题:
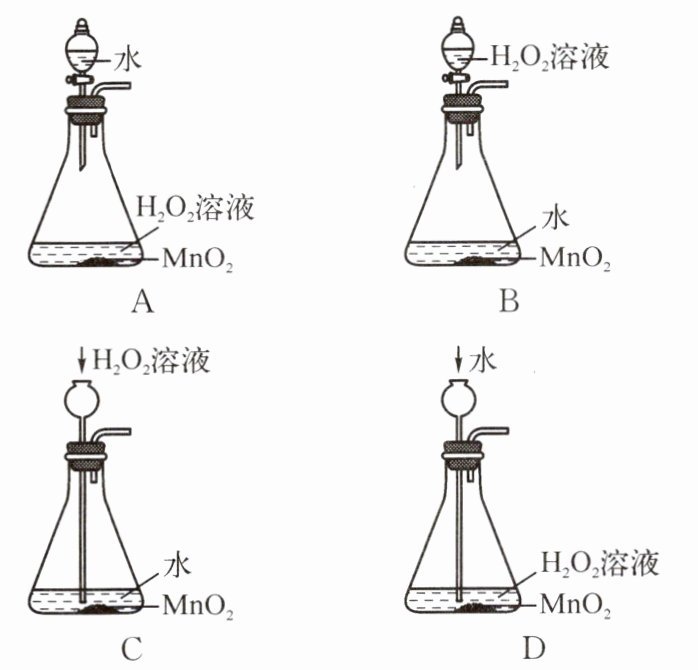
同学们向鱼缸供氧是因为氧气有______的性质。若利用浓度为30%的$H_{2}O_{2}溶液和MnO_{2}$制备氧气,反应速率太快。为获得平稳的气流,发生装置(下图)最合适的是______(填字母);发生反应的文字表达式为______。
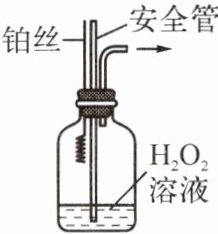
(3) 实验改进:用$H_{2}O_{2}$制取氧气时,也可用铂丝代替$MnO_{2}$作催化剂。催化剂的特点是在化学反应前后其______没有发生改变。下图装置可通过铂丝的上下移动控制______,若制备过程中体系内压强过大,则安全管中的现象是______,此时应将铂丝抽离过氧化氢溶液。
活动反思:请大家从原理、装置、技术、实际需求等方面进行反思,如铂丝的价格过高等,课余时间合作尝试用不同方法解决问题。
3. (泉州鲤城期中)学习小组开展了“设计和制作简易供氧器”的实践活动。
某品牌制氧机的制氧剂为二氧化锰和过碳酸钠(化学式:$2Na_{2}CO_{3}\cdot 3H_{2}O_{2}$,白色固体,是过氧化氢与碳酸钠的加合物,遇水后能产生氧气)。
【活动一】认识制氧机(图1)。
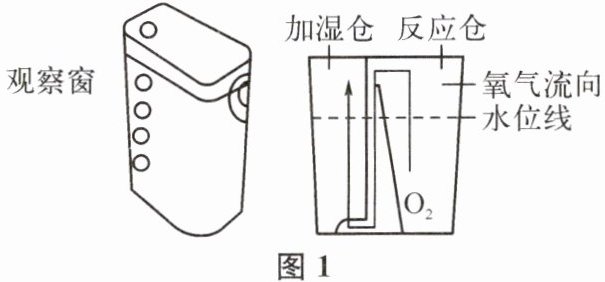
(1) 观察窗的作用是______。
(2) 加湿仓的作用是______(答2点)。
【活动二】探究制氧过程。
(3) Ⅰ.反应原理探究。
|实验操作|现象|结论|
|向锥形瓶a中加入1.5g过碳酸钠|分别加入100mL蒸馏水,观察;将一根带火星的木条伸入锥形瓶内,用手触摸锥形瓶外壁|瓶中有少许气泡产生;带火星木条不复燃;瓶壁不发烫|使用过碳酸钠制氧,需要加入二氧化锰固体;该反应是放热反应|
|向锥形瓶b中加入1.5g过碳酸钠和0.2g二氧化锰,混匀|①______②______|
(4) 小组同学向反应后的锥形瓶b中重复多次加入1.5g过碳酸钠,混匀后均又出现上述现象,反应后将剩余固体过滤、洗净、干燥、称量,固体质量仍为0.2g,则$MnO_{2}$在此反应中作______。
Ⅱ. 制氧剂的选择。
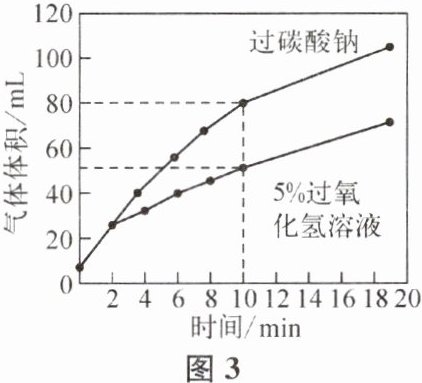
小组同学想到过氧化氢溶液常温下也可以快速制氧,为什么不选用过氧化氢溶液而选用过碳酸钠呢? 于是该兴趣小组对两者的制氧效率进行探究,并筛选合适的制氧剂。
【查阅资料】常温常压下产生150mL的氧气,以5%的过氧化氢溶液为制氧剂需要9.1mL;以过碳酸钠为制氧剂需要1.41g。
【实验方案】
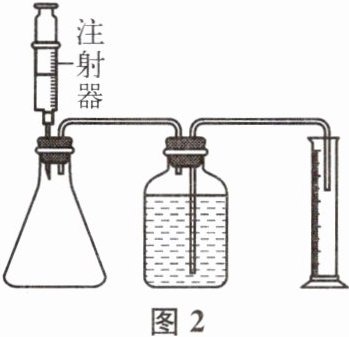
(5) 利用图2装置设计下列实验并记录0~20min量筒中水的体积(图3)。
|实验|锥形瓶中药品|注射器中药品|
|实验1|0.2g二氧化锰|9.1mL5%过氧化氢溶液|
|实验2|1.41g过碳酸钠 and 0.2g二氧化锰|______mL水|
Ⅲ. 加水量的探究。
向锥形瓶中加入1.41g过碳酸钠、0.2g$MnO_{2}$和9.11mL水,再分别用不同体积的水进行实验。记录并处理20min内数据如图4所示。
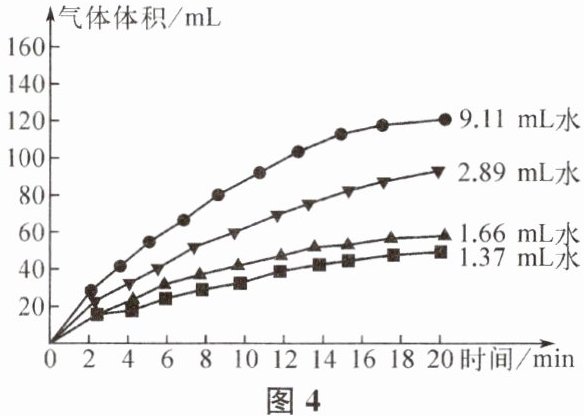
(6) 由图4可得出的结论______。
【活动三】制作供氧器______。
(7) 结合图3中数据,制氧剂选择过碳酸钠的依据是______ ______。
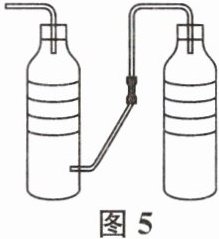
(8) 学习小组利用身边物品自制了如图5所示的简易供氧器______ ______ ______。
A. 产氧和洗气装置组合不用一体化
B. 内部气体流向采用高进低出方式
C. 特定需求是选择制氧方法的重要依据______。
B
)A. 该装置可根据需要调节氧气流量

B. 左侧瓶中加入的制氧试剂是高锰酸钾
C. 右侧瓶中的水有除杂、降温的作用
D. 设计供氧器需要综合考虑便捷、安全、环保等因素
2. 化学学习要求大家能有意识地应用化学知识,自主调用物理、数学等多个学科的相关知识,参与实践活动,不断改进,提升解决问题的能力。用鱼缸养鱼时要定期供氧。某化学兴趣小组的同学决定利用所学化学知识“设计和制作简易供氧器”,给鱼缸提供氧气。
(1) 实验室里一般不能制得氧气的物质是______(填字母)。
A. 高锰酸钾($KMnO_{4}$) B. 氯酸钾($KClO_{3}$)
C. 氯化钠($NaCl$) D. 过氧化氢($H_{2}O_{2}$)
(2) 同学们综合考虑了成本、环保、安全等因素后,决定利用$H_{2}O_{2}$溶液制备氧气的原理给鱼缸暂时供氧。请回答下列问题:
同学们向鱼缸供氧是因为氧气有______的性质。若利用浓度为30%的$H_{2}O_{2}溶液和MnO_{2}$制备氧气,反应速率太快。为获得平稳的气流,发生装置(下图)最合适的是______(填字母);发生反应的文字表达式为______。
(3) 实验改进:用$H_{2}O_{2}$制取氧气时,也可用铂丝代替$MnO_{2}$作催化剂。催化剂的特点是在化学反应前后其______没有发生改变。下图装置可通过铂丝的上下移动控制______,若制备过程中体系内压强过大,则安全管中的现象是______,此时应将铂丝抽离过氧化氢溶液。

活动反思:请大家从原理、装置、技术、实际需求等方面进行反思,如铂丝的价格过高等,课余时间合作尝试用不同方法解决问题。

3. (泉州鲤城期中)学习小组开展了“设计和制作简易供氧器”的实践活动。
某品牌制氧机的制氧剂为二氧化锰和过碳酸钠(化学式:$2Na_{2}CO_{3}\cdot 3H_{2}O_{2}$,白色固体,是过氧化氢与碳酸钠的加合物,遇水后能产生氧气)。
【活动一】认识制氧机(图1)。

(1) 观察窗的作用是______。
(2) 加湿仓的作用是______(答2点)。
【活动二】探究制氧过程。
(3) Ⅰ.反应原理探究。
|实验操作|现象|结论|
|向锥形瓶a中加入1.5g过碳酸钠|分别加入100mL蒸馏水,观察;将一根带火星的木条伸入锥形瓶内,用手触摸锥形瓶外壁|瓶中有少许气泡产生;带火星木条不复燃;瓶壁不发烫|使用过碳酸钠制氧,需要加入二氧化锰固体;该反应是放热反应|
|向锥形瓶b中加入1.5g过碳酸钠和0.2g二氧化锰,混匀|①______②______|
(4) 小组同学向反应后的锥形瓶b中重复多次加入1.5g过碳酸钠,混匀后均又出现上述现象,反应后将剩余固体过滤、洗净、干燥、称量,固体质量仍为0.2g,则$MnO_{2}$在此反应中作______。
Ⅱ. 制氧剂的选择。
小组同学想到过氧化氢溶液常温下也可以快速制氧,为什么不选用过氧化氢溶液而选用过碳酸钠呢? 于是该兴趣小组对两者的制氧效率进行探究,并筛选合适的制氧剂。
【查阅资料】常温常压下产生150mL的氧气,以5%的过氧化氢溶液为制氧剂需要9.1mL;以过碳酸钠为制氧剂需要1.41g。
【实验方案】
(5) 利用图2装置设计下列实验并记录0~20min量筒中水的体积(图3)。

|实验|锥形瓶中药品|注射器中药品|
|实验1|0.2g二氧化锰|9.1mL5%过氧化氢溶液|
|实验2|1.41g过碳酸钠 and 0.2g二氧化锰|______mL水|
Ⅲ. 加水量的探究。
向锥形瓶中加入1.41g过碳酸钠、0.2g$MnO_{2}$和9.11mL水,再分别用不同体积的水进行实验。记录并处理20min内数据如图4所示。


(6) 由图4可得出的结论______。
【活动三】制作供氧器______。
(7) 结合图3中数据,制氧剂选择过碳酸钠的依据是______ ______。
(8) 学习小组利用身边物品自制了如图5所示的简易供氧器______ ______ ______。
A. 产氧和洗气装置组合不用一体化

B. 内部气体流向采用高进低出方式
C. 特定需求是选择制氧方法的重要依据______。
答案:
1. B
2.
(1) C
(2) 供给呼吸 B 过氧化氢$\xrightarrow{\text{二氧化锰}}$水+氧气
(3) 质量和化学性质 反应的发生与停止 液面上升
提示:
(1) 氯化钠由钠元素和氯元素组成,不含氧元素,氯化钠发生化学反应后不可能生成氧气。
(2) A装置中虽有分液漏斗,但控制的是水的量,水不参加反应,无法控制反应速率;B装置通过分液漏斗控制加入过氧化氢溶液的量,能够控制反应速率,获得平稳的气流;C装置中长颈漏斗无法控制加入过氧化氢溶液的量,不能获得平稳的气流;D装置中长颈漏斗加水,水不参加反应,无法控制反应速率。
(3) 图中装置内过氧化氢分解生成氧气,使集气瓶中的气体增多,压强变大,过氧化氢溶液被压入安全管中,液面上升。
3.
(1) 观察是否有气泡和产生气体的快慢
(2) 洗气,使氧气具有一定的湿度(合理均可)
(3) ①带火星木条复燃 ②瓶壁发烫
(4) 催化剂
(5) 9.1
(6) 过碳酸钠的产氧速率随加水量的增加而增大
(7) 相同条件下,2 min~20 min,过碳酸钠产氧速率比5%过氧化氢溶液高
(8) A
2.
(1) C
(2) 供给呼吸 B 过氧化氢$\xrightarrow{\text{二氧化锰}}$水+氧气
(3) 质量和化学性质 反应的发生与停止 液面上升
提示:
(1) 氯化钠由钠元素和氯元素组成,不含氧元素,氯化钠发生化学反应后不可能生成氧气。
(2) A装置中虽有分液漏斗,但控制的是水的量,水不参加反应,无法控制反应速率;B装置通过分液漏斗控制加入过氧化氢溶液的量,能够控制反应速率,获得平稳的气流;C装置中长颈漏斗无法控制加入过氧化氢溶液的量,不能获得平稳的气流;D装置中长颈漏斗加水,水不参加反应,无法控制反应速率。
(3) 图中装置内过氧化氢分解生成氧气,使集气瓶中的气体增多,压强变大,过氧化氢溶液被压入安全管中,液面上升。
3.
(1) 观察是否有气泡和产生气体的快慢
(2) 洗气,使氧气具有一定的湿度(合理均可)
(3) ①带火星木条复燃 ②瓶壁发烫
(4) 催化剂
(5) 9.1
(6) 过碳酸钠的产氧速率随加水量的增加而增大
(7) 相同条件下,2 min~20 min,过碳酸钠产氧速率比5%过氧化氢溶液高
(8) A
查看更多完整答案,请扫码查看


