第80页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
7. 为了测定实验室某生锈铁片中铁元素的质量分数,两位同学分别设计了下列甲、乙两个实验方案。
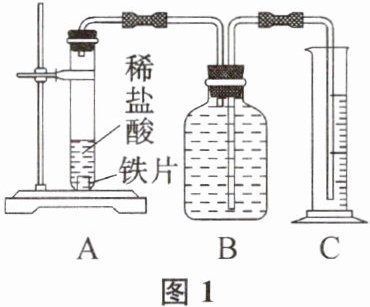
方案甲:称得生锈铁片的质量为$m_{1}g$,按图1所示装置进行实验,完全反应后,测得室温下产生氢气的体积为$V_{1}L$,查得其密度为$ρ_{1}g/L$。
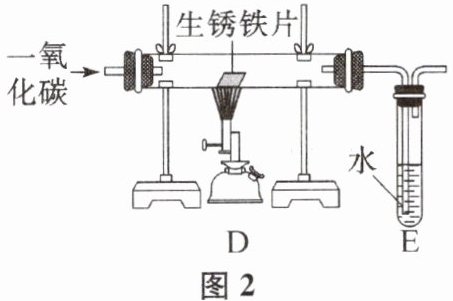
方案乙:称得生锈铁片的质量为$m_{2}g$,先按图2装置进行实验。当生锈铁片完全变成光亮的银白色时,停止加热,继续通入CO至室温。取出铁片,按图1装置继续进行实验。完全反应后,测得室温下产生氢气的体积为$V_{2}L$,查得其密度为$ρ_{2}g/L$。
(1)称量时应将铁片放在托盘天平的
(2)评价交流:上述两个方案中,可行的是
(3)设计实验:方案乙中,同学们设计了如下所示实验报告,请帮助完成。
①
②
(4)提出问题:图2装置是否有可改进之处?请简要叙述具体改进意见或在图2中画出简易装置示意图:
(5)结论:生锈铁片中铁元素的质量分数是

方案甲:称得生锈铁片的质量为$m_{1}g$,按图1所示装置进行实验,完全反应后,测得室温下产生氢气的体积为$V_{1}L$,查得其密度为$ρ_{1}g/L$。
方案乙:称得生锈铁片的质量为$m_{2}g$,先按图2装置进行实验。当生锈铁片完全变成光亮的银白色时,停止加热,继续通入CO至室温。取出铁片,按图1装置继续进行实验。完全反应后,测得室温下产生氢气的体积为$V_{2}L$,查得其密度为$ρ_{2}g/L$。
(1)称量时应将铁片放在托盘天平的
左
(填“左”或“右”)盘;两位同学使用托盘天平,分别称得铁片质量为2.12g、2.1g,其中不合理的数据是2.12g
。(2)评价交流:上述两个方案中,可行的是
乙
(填“甲”或“乙”);分析不可行的方案,其缺陷是不能测出生锈铁片中铁元素的质量
。(3)设计实验:方案乙中,同学们设计了如下所示实验报告,请帮助完成。

①
防止装置E中的水倒吸
Fe₂O₃+3CO$\xlongequal{高温}$2Fe+3CO₂
②
Fe+2HCl=FeCl₂+H₂↑
(4)提出问题:图2装置是否有可改进之处?请简要叙述具体改进意见或在图2中画出简易装置示意图:
将装置E中的水改成澄清石灰水或氢氧化钠溶液,并在装置E的导管口处点燃导出的气体,图略
。(5)结论:生锈铁片中铁元素的质量分数是
(2800ρ₂V₂)/m₂%
(用字母表示)。
答案:
(1)左 2.12g
(2)乙 不能测出生锈铁片中铁元素的质量
(3)①防止装置E中的水倒吸 Fe₂O₃+3CO$\xlongequal{高温}$2Fe+3CO₂ ②Fe+2HCl=FeCl₂+H₂↑
(4)将装置E中的水改成澄清石灰水或氢氧化钠溶液,并在装置E的导管口处点燃导出的气体,图略
(5)(2800ρ₂V₂)/m₂%
提示:
(2)生锈铁片中含有铁、铁的化合物等物质,方案甲只能得出铁片中金属铁的质量,无法知道铁的化合物的质量,而题目要求测定生锈铁片中铁元素的质量分数,方案乙将铁锈的铁先还原出来,可以测出生锈铁片中铁元素的质量,故方案乙可行。
(4)二氧化碳是造成温室效应的主要气体,而一氧化碳有毒,排放到空气中会造成空气污染,因此必须对这两种气体进行处理。
(5)设生锈铁片中铁元素的质量为x。
Fe+2HCl=FeCl₂+H₂↑
56 2
x ρ₂V₂g
56/2=x/ρ₂V₂g
解得:x=28ρ₂V₂g。
则生锈铁片中铁元素的质量分数为(28ρ₂V₂g)/m₂g×100%=(2800ρ₂V₂)/m₂%。
(1)左 2.12g
(2)乙 不能测出生锈铁片中铁元素的质量
(3)①防止装置E中的水倒吸 Fe₂O₃+3CO$\xlongequal{高温}$2Fe+3CO₂ ②Fe+2HCl=FeCl₂+H₂↑
(4)将装置E中的水改成澄清石灰水或氢氧化钠溶液,并在装置E的导管口处点燃导出的气体,图略
(5)(2800ρ₂V₂)/m₂%
提示:
(2)生锈铁片中含有铁、铁的化合物等物质,方案甲只能得出铁片中金属铁的质量,无法知道铁的化合物的质量,而题目要求测定生锈铁片中铁元素的质量分数,方案乙将铁锈的铁先还原出来,可以测出生锈铁片中铁元素的质量,故方案乙可行。
(4)二氧化碳是造成温室效应的主要气体,而一氧化碳有毒,排放到空气中会造成空气污染,因此必须对这两种气体进行处理。
(5)设生锈铁片中铁元素的质量为x。
Fe+2HCl=FeCl₂+H₂↑
56 2
x ρ₂V₂g
56/2=x/ρ₂V₂g
解得:x=28ρ₂V₂g。
则生锈铁片中铁元素的质量分数为(28ρ₂V₂g)/m₂g×100%=(2800ρ₂V₂)/m₂%。
查看更多完整答案,请扫码查看


