第26页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
13. 人类常利用化学反应得到所需要的物质。如图所示为$Mg(OH)_{2}$、$MgCl_{2}$、$Mg(NO_{3})_{2}$三种物质间的转化关系,根据所学知识判断,下列说法中,正确的是(

A.通过加入氯化铜溶液或稀盐酸可实现①的转化
B.通过一步反应无法实现②的转化
C.通过一步反应可实现$Mg(NO_{3})_{2}向MgCl_{2}$的转化
D.通过加入氢氧化钠等可溶性碱可实现③的转化
D
)
A.通过加入氯化铜溶液或稀盐酸可实现①的转化
B.通过一步反应无法实现②的转化
C.通过一步反应可实现$Mg(NO_{3})_{2}向MgCl_{2}$的转化
D.通过加入氢氧化钠等可溶性碱可实现③的转化
答案:
D
14. 小柯为比较$Mg$、$Fe$、$Cu$三种金属的活动性顺序,进行了如图甲所示的实验,实验后把两试管中的物质倒入烧杯中(如图乙所示),发现烧杯内的红色固体明显增多,充分反应后过滤。溶液中含有的金属离子可能的组成是(
①$Mg^{2+}$
②$Mg^{2+}和Fe^{2+}$
③$Mg^{2+}和Cu^{2+}$
④$Mg^{2+}$、$Fe^{2+}和Cu^{2+}$

A.①②
B.①③
C.②④
D.③④
C
)①$Mg^{2+}$
②$Mg^{2+}和Fe^{2+}$
③$Mg^{2+}和Cu^{2+}$
④$Mg^{2+}$、$Fe^{2+}和Cu^{2+}$

A.①②
B.①③
C.②④
D.③④
答案:
C
15. 某溶液含有$Cu(NO_{3})_{2}和AgNO_{3}$,现向其中加入一定量的锌粉,参加反应的锌的质量与溶液中金属离子种类数的关系如图所示。下列说法中,不正确的是(

A.当溶液中溶质仅有1种时,金属单质可能仅有1种
B.从$m_{1}变化到m_{2}$,溶液中$Cu(NO_{3})_{2}$的质量分数变大
C.$Cu的活动性比Ag$强,只用盐酸无法比较两者的活动性强弱
D.$cd$段(不含$c$、$d$两点)溶液中的金属离子为$Cu^{2+}$、$Zn^{2+}$
A
)
A.当溶液中溶质仅有1种时,金属单质可能仅有1种
B.从$m_{1}变化到m_{2}$,溶液中$Cu(NO_{3})_{2}$的质量分数变大
C.$Cu的活动性比Ag$强,只用盐酸无法比较两者的活动性强弱
D.$cd$段(不含$c$、$d$两点)溶液中的金属离子为$Cu^{2+}$、$Zn^{2+}$
答案:
A
16. 金属及金属材料在生产、生活中有广泛的应用。
(1) 钢铁是制造船舶的主要材料,钢铁与纯铁相比,其硬度更
(2) 铝的金属活动性较强,但在空气中却耐锈蚀,其原因是
(3) 铁制品若保管不善,则很容易生锈,请写出一项防锈措施:
(4) 家庭电路中使用的电线是铜芯线,这主要是利用了铜的
(1) 钢铁是制造船舶的主要材料,钢铁与纯铁相比,其硬度更
大
(填“大”或“小”)。(2) 铝的金属活动性较强,但在空气中却耐锈蚀,其原因是
铝在常温下能和氧气反应生成一层致密的氧化铝薄膜,阻止内部的铝进一步反应
。(3) 铁制品若保管不善,则很容易生锈,请写出一项防锈措施:
涂油(或刷漆,保持干燥)
。(4) 家庭电路中使用的电线是铜芯线,这主要是利用了铜的
导电
性。
答案:
(1)大
(2)铝在常温下能和氧气反应生成一层致密的氧化铝薄膜,阻止内部的铝进一步反应
(3)涂油(或刷漆,保持干燥)
(4)导电
(1)大
(2)铝在常温下能和氧气反应生成一层致密的氧化铝薄膜,阻止内部的铝进一步反应
(3)涂油(或刷漆,保持干燥)
(4)导电
17. 氧化还原反应一定会出现得失电子现象,元素的化合价也会改变。金属钠在氯气中点燃生成食盐的化学方程式为$2Na+Cl_{2}\xlongequal{点燃}2NaCl$。此反应过程中,得到电子的元素是
Cl
(填化学符号,下同),化合价升高的元素是Na
,作为氧化剂的物质是Cl₂
,氧化产物是NaCl
。
答案:
Cl Na Cl₂ NaCl
18. 小明学习了物质的性质后,梳理的单质、氧化物、酸、碱、盐与X之间的转化关系如图所示,“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物及反应条件已略去。
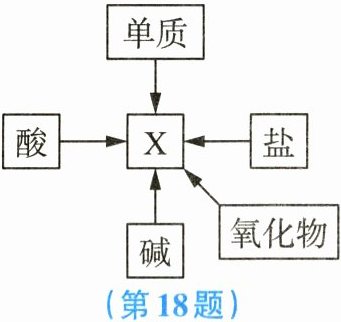
(1) 若X是氯化钠,则酸→X的化学方程式为
(2) 若X是水,则能实现图中物质间转化的基本反应类型有
A. 化合反应
B. 分解反应
C. 置换反应
D. 复分解反应

(1) 若X是氯化钠,则酸→X的化学方程式为
HCl+NaOH===NaCl+H₂O
,图中碱的化学式为NaOH
。(2) 若X是水,则能实现图中物质间转化的基本反应类型有
ABCD
(填字母)。A. 化合反应
B. 分解反应
C. 置换反应
D. 复分解反应
答案:
(1)HCl+NaOH===NaCl+H₂O NaOH
(2)ABCD
(1)HCl+NaOH===NaCl+H₂O NaOH
(2)ABCD
19. 某兴趣小组的同学在探究金属的化学性质时,做了如图所示的两次实验。
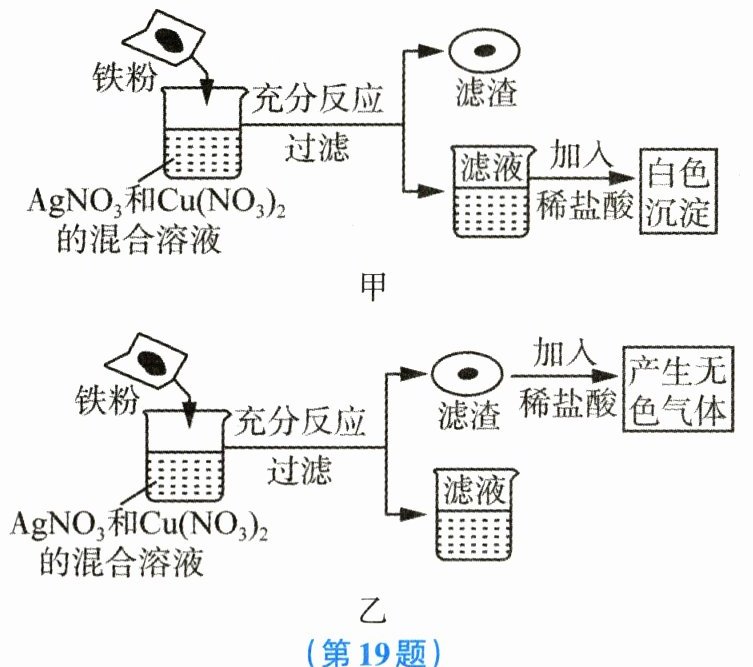
(1) 甲实验中滤渣的成分是
(2) 乙实验中滤液中含有的金属离子为

(1) 甲实验中滤渣的成分是
银
,产生白色沉淀的反应的化学方程式为HCl+AgNO₃===HNO₃+AgCl↓
。(2) 乙实验中滤液中含有的金属离子为
Fe²⁺
(填离子符号)。
答案:
(1)银 HCl+AgNO₃===HNO₃+AgCl↓
(2)Fe²⁺
(1)银 HCl+AgNO₃===HNO₃+AgCl↓
(2)Fe²⁺
20. 某固体粉末可能含有氯化镁、硫酸钠、硝酸钠、硫酸铜和碳酸钙中的一种或几种,为确定其成分,某科学实验小组的同学进行了如图所示的实验。
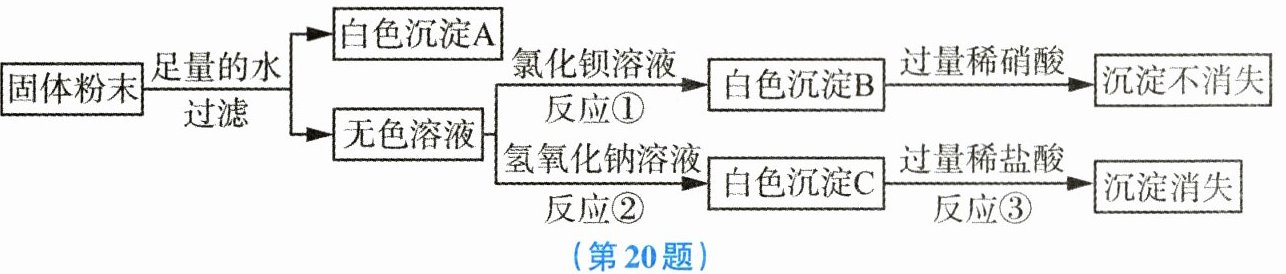
(1) 白色沉淀C是
(2) 反应①的化学方程式为
(3) 原固体粉末中一定含有的物质是

(1) 白色沉淀C是
Mg(OH)₂
(填化学式)。(2) 反应①的化学方程式为
Na₂SO₄+BaCl₂===BaSO₄↓+2NaCl
。(3) 原固体粉末中一定含有的物质是
CaCO₃、Na₂SO₄、MgCl₂
(填化学式,下同),一定不含的物质是CuSO₄
。
答案:
(1)Mg(OH)₂
(2)Na₂SO₄+BaCl₂===BaSO₄↓+2NaCl
(3)CaCO₃、Na₂SO₄、MgCl₂ CuSO₄
(1)Mg(OH)₂
(2)Na₂SO₄+BaCl₂===BaSO₄↓+2NaCl
(3)CaCO₃、Na₂SO₄、MgCl₂ CuSO₄
查看更多完整答案,请扫码查看


