第11页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
21. 叶绿素富含微量元素铁,叶绿素呈绿色,被破坏后变成黄褐色。小金为探究影响叶绿素稳定性的因素,在室温下进行了四组实验,实验记录如下表所示。

(1)请写出用$pH$试纸测定溶液酸碱性的方法:
(2)根据实验结果,小金得出结论:当$pH<7$时,叶绿素被破坏。有同学认为这样得出的结论还不够严谨,理由是

(1)请写出用$pH$试纸测定溶液酸碱性的方法:
用洁净的玻璃棒蘸取待测液,滴在pH试纸上,再将试纸显示的颜色与标准比色卡对照
。(2)根据实验结果,小金得出结论:当$pH<7$时,叶绿素被破坏。有同学认为这样得出的结论还不够严谨,理由是
实验没有以1.0为pH梯度进行,表格中也没有pH等于7时溶液颜色的变化
。
答案:
(1)用洁净的玻璃棒蘸取待测液,滴在pH试纸上,再将试纸显示的颜色与标准比色卡对照
(2)实验没有以1.0为pH梯度进行,表格中也没有pH等于7时溶液颜色的变化
(1)用洁净的玻璃棒蘸取待测液,滴在pH试纸上,再将试纸显示的颜色与标准比色卡对照
(2)实验没有以1.0为pH梯度进行,表格中也没有pH等于7时溶液颜色的变化
22. 如图甲所示,同学们借助传感器监测溶液的$pH$和温度的变化情况来探究稀硫酸和氢氧化钠溶液的反应,图乙为反应过程中溶液的$pH$变化曲线,图丙为反应过程中溶液温度的变化曲线。请回答下列问题:
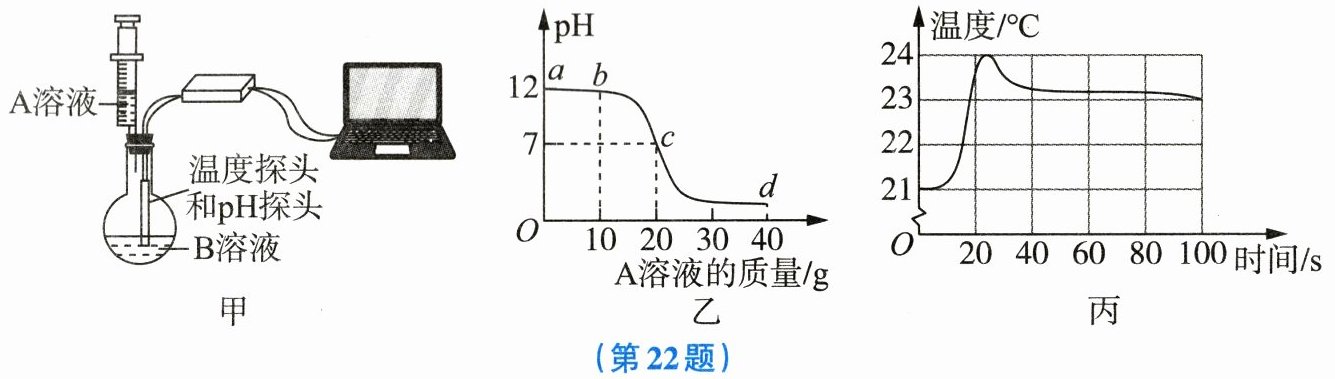
(1)该反应的化学方程式为
(2)小宁取反应后的溶液,加入$Ba(NO_3)_2$后看到白色沉淀。根据此现象,小宁判断该溶液中一定含有$H_2SO_4$。你认为小宁的判断是否正确?请作出判断并说明理由。
(3)图丙中的最高点与图乙中的

(1)该反应的化学方程式为
2NaOH+H₂SO₄=Na₂SO₄+2H₂O
。(2)小宁取反应后的溶液,加入$Ba(NO_3)_2$后看到白色沉淀。根据此现象,小宁判断该溶液中一定含有$H_2SO_4$。你认为小宁的判断是否正确?请作出判断并说明理由。
不正确,H₂SO₄与反应生成的Na₂SO₄都可以和硝酸钡反应生成白色沉淀
。(3)图丙中的最高点与图乙中的
c
(填“$a$”“$b$”“$c$”或“$d$”)点相对应。
答案:
(1)2NaOH+H₂SO₄=Na₂SO₄+2H₂O
(2)不正确,H₂SO₄与反应生成的Na₂SO₄都可以和硝酸钡反应生成白色沉淀
(3)c
(1)2NaOH+H₂SO₄=Na₂SO₄+2H₂O
(2)不正确,H₂SO₄与反应生成的Na₂SO₄都可以和硝酸钡反应生成白色沉淀
(3)c
23. 粗盐中含有难溶性杂质和多种可溶性杂质(氯化镁、氯化钙等)。某同学为了提纯粗盐,设计了如图所示的实验方案:(已知碳酸镁微溶于水)

(1)用化学方程式回答,步骤②的主要目的是
(2)有同学认为只需要用氢氧化钠溶液和碳酸钠溶液中的任意一种就能将这两种可溶性杂质除去,你认为这种方法
(3)有同学认为原实验方案不完善,作出这种评价的依据是

(1)用化学方程式回答,步骤②的主要目的是
MgCl₂+2NaOH=Mg(OH)₂↓+2NaCl
。(2)有同学认为只需要用氢氧化钠溶液和碳酸钠溶液中的任意一种就能将这两种可溶性杂质除去,你认为这种方法
不可行
,理由是碳酸镁或氢氧化钙是微溶的,只用其中一种试剂会生成一种杂质微溶物而不能将杂质全部除去
。(3)有同学认为原实验方案不完善,作出这种评价的依据是
在除去氯化镁和氯化钙的同时又引入了新的杂质氢氧化钠和碳酸钠
。
答案:
(1)MgCl₂+2NaOH=Mg(OH)₂↓+2NaCl
(2)不可行 碳酸镁或氢氧化钙是微溶的,只用其中一种试剂会生成一种杂质微溶物而不能将杂质全部除去
(3)在除去氯化镁和氯化钙的同时又引入了新的杂质氢氧化钠和碳酸钠
(1)MgCl₂+2NaOH=Mg(OH)₂↓+2NaCl
(2)不可行 碳酸镁或氢氧化钙是微溶的,只用其中一种试剂会生成一种杂质微溶物而不能将杂质全部除去
(3)在除去氯化镁和氯化钙的同时又引入了新的杂质氢氧化钠和碳酸钠
24. 一次实验中,同学们发现了一瓶标签受损的无色溶液,如图所示。这瓶溶液是什么呢?同学们进行了以下探究:

【提出猜想】这瓶溶液可能是:①氯化钠溶液;②硝酸钠溶液;③碳酸钠溶液;④氢氧化钠溶液。
【查阅资料】硝酸钠溶液呈中性。
【实验探究】
(1)取少量该溶液于试管中,向其中滴加几滴紫色石蕊试液,若溶液变为蓝色,则猜想______(填序号)不成立。
(2)将该溶液滴加到稀盐酸中,若观察到______(填现象),则猜想③成立。
【反思与评价】有同学指出该结论不够严谨,理由是若该溶液为氢氧化钠溶液,则其发生部分变质后也能产生上述现象。为此,同学们认为,可以往该溶液中加入过量的______(填物质名称)溶液以排除干扰,再检验氢氧化钠即可。
【实验探究】
(1)
(2)

【提出猜想】这瓶溶液可能是:①氯化钠溶液;②硝酸钠溶液;③碳酸钠溶液;④氢氧化钠溶液。
【查阅资料】硝酸钠溶液呈中性。
【实验探究】
(1)取少量该溶液于试管中,向其中滴加几滴紫色石蕊试液,若溶液变为蓝色,则猜想______(填序号)不成立。
(2)将该溶液滴加到稀盐酸中,若观察到______(填现象),则猜想③成立。
【反思与评价】有同学指出该结论不够严谨,理由是若该溶液为氢氧化钠溶液,则其发生部分变质后也能产生上述现象。为此,同学们认为,可以往该溶液中加入过量的______(填物质名称)溶液以排除干扰,再检验氢氧化钠即可。
【实验探究】
(1)
①②
(2)
有气泡产生
【反思与评价】氯化钙(或氯化钡)
答案:
【实验探究】
(1)①②
(2)有气泡产生 【反思与评价】氯化钙(或氯化钡)
(1)①②
(2)有气泡产生 【反思与评价】氯化钙(或氯化钡)
25. 学习了酸雨及酸的性质后,同学们知道了煤(含有$C$、$S$等元素)燃烧产生的二氧化硫是形成酸雨的主要原因之一,并制作了“酸雨形成及危害的研究模型”与评价量表。如图甲所示为小明制作的模型。


(1)根据评价量表,该模型的指标一被评为“优秀”,据此推测图甲中“▲”处的溶液可能是
(2)该模型的指标二被评为“合格”的原因是
(3)该模型的指标三被评为“待改进”,于是小明设计了如图乙、丙所示的两种改进模型。这两种模型中,图


(1)根据评价量表,该模型的指标一被评为“优秀”,据此推测图甲中“▲”处的溶液可能是
氢氧化钠溶液
。(2)该模型的指标二被评为“合格”的原因是
煤中含有碳元素,燃烧还能产生二氧化碳气体,二氧化碳与水反应生成碳酸,碳酸显酸性,也会使紫色石蕊试液变红
。(3)该模型的指标三被评为“待改进”,于是小明设计了如图乙、丙所示的两种改进模型。这两种模型中,图
丙
(填“乙”或“丙”)所示模型的指标三能被评为“合格”。
答案:
(1)氢氧化钠溶液
(2)煤中含有碳元素,燃烧还能产生二氧化碳气体,二氧化碳与水反应生成碳酸,碳酸显酸性,也会使紫色石蕊试液变红
(3)丙
(1)氢氧化钠溶液
(2)煤中含有碳元素,燃烧还能产生二氧化碳气体,二氧化碳与水反应生成碳酸,碳酸显酸性,也会使紫色石蕊试液变红
(3)丙
26. (6分)学习“常见的碱”这节课时,同学们发现氢氧化钠溶液和二氧化碳的反应没有明显现象,为验证两者确实能够发生反应,同学们设计了如图所示的装置进行探究。
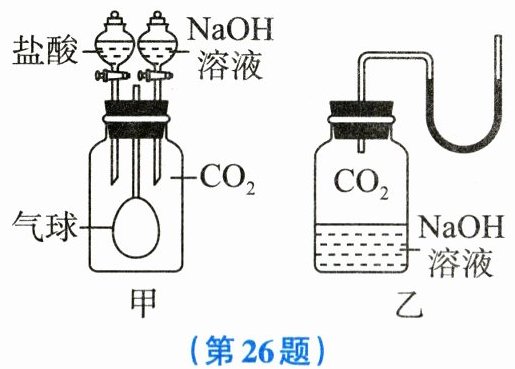
(1)小可设计了如图甲所示的装置,在依次滴加$NaOH$溶液、盐酸的过程中,气球的体积将如何变化?
(2)小雪认为将图甲中的盐酸用氯化钙溶液代替也能达到实验目的,请帮她说明理由:
(3)图乙是小明设计的实验装置,小可认为小明仅利用此装置得出的结论不可靠,需要再设置一个对照组。请你帮他写出对照组的实验过程:

(1)小可设计了如图甲所示的装置,在依次滴加$NaOH$溶液、盐酸的过程中,气球的体积将如何变化?
先变大后变小
。(2)小雪认为将图甲中的盐酸用氯化钙溶液代替也能达到实验目的,请帮她说明理由:
先加入氢氧化钠溶液,后加入氯化钙溶液,氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,会观察到产生白色沉淀,说明二氧化碳和氢氧化钠反应
。(3)图乙是小明设计的实验装置,小可认为小明仅利用此装置得出的结论不可靠,需要再设置一个对照组。请你帮他写出对照组的实验过程:
利用和题图乙相同的装置,把氢氧化钠溶液换成等体积的水,若此时U形管中左侧液面上升的高度小于装置中为氢氧化钠溶液时,则说明氢氧化钠能和二氧化碳反应
。
答案:
(1)先变大后变小
(2)先加入氢氧化钠溶液,后加入氯化钙溶液,氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,会观察到产生白色沉淀,说明二氧化碳和氢氧化钠反应
(3)利用和题图乙相同的装置,把氢氧化钠溶液换成等体积的水,若此时U形管中左侧液面上升的高度小于装置中为氢氧化钠溶液时,则说明氢氧化钠能和二氧化碳反应
(1)先变大后变小
(2)先加入氢氧化钠溶液,后加入氯化钙溶液,氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,会观察到产生白色沉淀,说明二氧化碳和氢氧化钠反应
(3)利用和题图乙相同的装置,把氢氧化钠溶液换成等体积的水,若此时U形管中左侧液面上升的高度小于装置中为氢氧化钠溶液时,则说明氢氧化钠能和二氧化碳反应
查看更多完整答案,请扫码查看


