第101页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
27. (12 分)某科学兴趣小组的同学用实验室常用药品(或溶液)对“NaOH 溶液与稀盐酸是否恰好完全反应”进行探究,该小组设计了两种不同的方案。
【知识卡片】①氯化钠溶液显中性;②氯化铜易溶于水。
【实验探究】
(1)方案一:某同学先向试管中加入 2mL NaOH 溶液,再滴入几滴酚酞试液,溶液变红,然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为无色。
①边滴边振荡的原因是
②写出该反应的化学方程式:
③在滴入稀盐酸的过程中,若观察到有气泡出现,请分析产生气泡的可能原因:
(2)方案二:

【实验反思】
(1)另有同学提出方案二不能证明 NaOH 溶液与稀盐酸恰好完全反应,其原因是
(2)除以上方案外,单独使用下列物质也能探究“NaOH 溶液与稀盐酸是否恰好完全反应”的是(
A. 铜片
B. pH 试纸
C. 氧化铜
D. 紫色石蕊试液
【知识卡片】①氯化钠溶液显中性;②氯化铜易溶于水。
【实验探究】
(1)方案一:某同学先向试管中加入 2mL NaOH 溶液,再滴入几滴酚酞试液,溶液变红,然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为无色。
①边滴边振荡的原因是
使反应物充分接触,加快化学反应的速率
。②写出该反应的化学方程式:
${NaOH + HCl\xlongequal{}NaCl + H_{2}O}$
。③在滴入稀盐酸的过程中,若观察到有气泡出现,请分析产生气泡的可能原因:
${Na_{2}CO_{3} + 2HCl\xlongequal{}2NaCl + H_{2}O + CO_{2}\uparrow}$
(用化学方程式表示)。(2)方案二:

有气泡产生
【实验反思】
(1)另有同学提出方案二不能证明 NaOH 溶液与稀盐酸恰好完全反应,其原因是
如果稀盐酸的量不足,氢氧化钠即使有剩余也没有明显现象
。(2)除以上方案外,单独使用下列物质也能探究“NaOH 溶液与稀盐酸是否恰好完全反应”的是(
BD
)(填字母)。A. 铜片
B. pH 试纸
C. 氧化铜
D. 紫色石蕊试液
答案:
【实验探究】
(1)①使反应物充分接触,加快化学反应的速率
②${NaOH + HCl\xlongequal{}NaCl + H_{2}O}$ ③${Na_{2}CO_{3} + 2HCl\xlongequal{}2NaCl + H_{2}O + CO_{2}\uparrow}$
(2)有气泡产生 【实验反思】
(1)如果稀盐酸的量不足,氢氧化钠即使有剩余也没有明显现象
(2)BD
(1)①使反应物充分接触,加快化学反应的速率
②${NaOH + HCl\xlongequal{}NaCl + H_{2}O}$ ③${Na_{2}CO_{3} + 2HCl\xlongequal{}2NaCl + H_{2}O + CO_{2}\uparrow}$
(2)有气泡产生 【实验反思】
(1)如果稀盐酸的量不足,氢氧化钠即使有剩余也没有明显现象
(2)BD
28. (6 分)同学们通过以下在溶液中进行的实验,探究复分解反应发生的条件:
$①H_2SO_4 + Ba(NO_3)_2 ②H_2SO_4 + NaOH ③H_2SO_4 + Na_2CO_3 ④Ba(NO_3)_2 + NaOH ⑤Ba(NO_3)_2 + Na_2CO_3 ⑥NaOH + Na_2CO_3$
(1)同学们经总结和归纳得出:生成物中有沉淀、气体、水时,复分解反应才可以发生。
(2)同学们将实验后的所有物质倒入实验烧杯中,后续实验及现象如图所示:
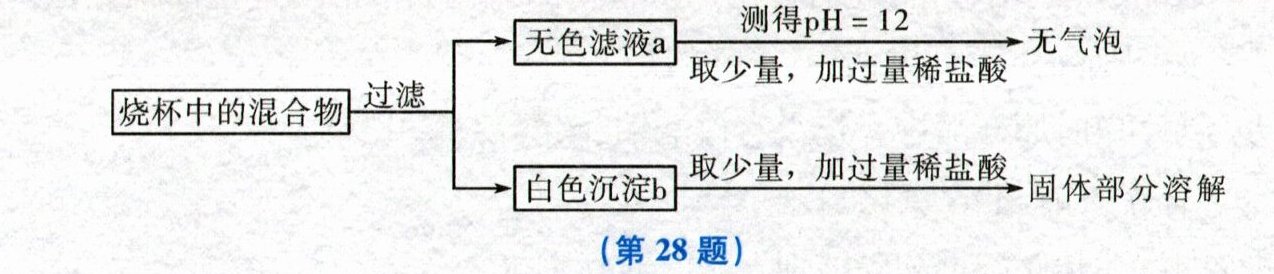
综合分析可知,无色滤液 a 中一定含有的溶质包括
(3)下列有关利用无色滤液 a 和白色沉淀 b 的设想,合理的是
A. 鉴别氯化镁溶液和氯化钡溶液:取样,滴加无色滤液 a
B. 制取硝酸钠溶液:向无色滤液 a 中加入适量的稀硝酸
C. 除去硝酸钡溶液中的硝酸:向其中加入过量的白色沉淀 b,过滤
请你写出认为合理的方案中发生反应的化学方程式:
$①H_2SO_4 + Ba(NO_3)_2 ②H_2SO_4 + NaOH ③H_2SO_4 + Na_2CO_3 ④Ba(NO_3)_2 + NaOH ⑤Ba(NO_3)_2 + Na_2CO_3 ⑥NaOH + Na_2CO_3$
(1)同学们经总结和归纳得出:生成物中有沉淀、气体、水时,复分解反应才可以发生。
(2)同学们将实验后的所有物质倒入实验烧杯中,后续实验及现象如图所示:

综合分析可知,无色滤液 a 中一定含有的溶质包括
NaOH、NaNO₃
。(3)下列有关利用无色滤液 a 和白色沉淀 b 的设想,合理的是
C
(填字母)。A. 鉴别氯化镁溶液和氯化钡溶液:取样,滴加无色滤液 a
B. 制取硝酸钠溶液:向无色滤液 a 中加入适量的稀硝酸
C. 除去硝酸钡溶液中的硝酸:向其中加入过量的白色沉淀 b,过滤
请你写出认为合理的方案中发生反应的化学方程式:
BaCO₃ + 2HNO₃=Ba(NO₃)₂ + H₂O + CO₂↑
。
答案:
(2)${NaOH}$、${NaNO_{3}}$
(3)C ${BaCO_{3} + 2HNO_{3}\xlongequal{}Ba(NO_{3})_{2} + H_{2}O + CO_{2}\uparrow}$
(2)${NaOH}$、${NaNO_{3}}$
(3)C ${BaCO_{3} + 2HNO_{3}\xlongequal{}Ba(NO_{3})_{2} + H_{2}O + CO_{2}\uparrow}$
查看更多完整答案,请扫码查看


