第67页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
1. [2024·湖北,16(2)(3)(4)]铍用于宇航器件的构筑。一种从其铝硅酸盐$[Be_{3}Al_{2}(SiO_{3})_{6}]$中提取铍的路径为
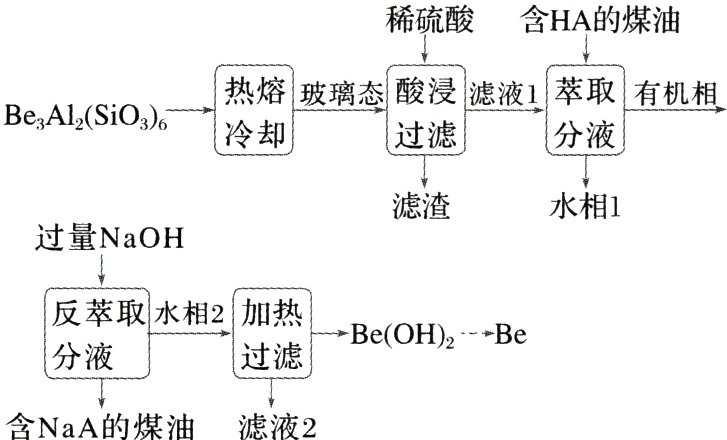
已知:$Be^{2 + }+4HA{<=>}BeA_{2}(HA)_{2}+2H^{ + }$
回答下列问题:
(2)为了从“热熔冷却”步骤得到玻璃态,冷却过程的特点是______________________________。
(3)“萃取分液”的目的是分离$Be^{2 + }$和$Al^{3 + }$,向过量烧碱溶液中逐滴加入少量“水相1”的溶液,观察到的现象是__________________________。
(4)写出反萃取生成$Na_{2}[Be(OH)_{4}]$的化学方程式______________________________。“滤液2”可以进入______________步骤再利用。

已知:$Be^{2 + }+4HA{<=>}BeA_{2}(HA)_{2}+2H^{ + }$
回答下列问题:
(2)为了从“热熔冷却”步骤得到玻璃态,冷却过程的特点是______________________________。
(3)“萃取分液”的目的是分离$Be^{2 + }$和$Al^{3 + }$,向过量烧碱溶液中逐滴加入少量“水相1”的溶液,观察到的现象是__________________________。
(4)写出反萃取生成$Na_{2}[Be(OH)_{4}]$的化学方程式______________________________。“滤液2”可以进入______________步骤再利用。
答案:
(2)快速冷却
(3)先产生白色沉淀,后白色沉淀快速溶解
(4)$BeA_{2}(HA)_{2}+6NaOH=Na_{2}[Be(OH)_{4}]+4NaA + 2H_{2}O$
(5)反萃取
解析 在本流程生产过程中,先将铝硅酸盐加热熔融后快速冷却得到其玻璃态,加入稀硫酸浸得到的滤渣成分为$H_{2}SiO_{3}$;“滤液1”中含有$Be^{2+}$和$Al^{3+}$,加入含HA的煤油后HA与$Be^{2+}$反应生成$BeA_{2}(HA)_{2}$进入有机相中,$Al^{3+}$进入水相1中;在有机相中加入过量氢氧化钠后$BeA_{2}(HA)_{2}$转化为$Na_{2}[Be(OH)_{4}]$进入水相2中,分离出含NaA的煤油;对水相2加热,$Na_{2}[Be(OH)_{4}]$转化为$Be(OH)_{2}$,通过过滤分离出来,最后通过一系列操作得到金属铍。
(2)熔融态物质冷却凝固时,若缓慢冷却则会形成晶体,若快速冷却则会形成非晶态,即玻璃态。
(3)“滤液1”中有$Be^{2+}$和$Al^{3+}$,加入含HA的煤油后HA将$Be^{2+}$萃取到有机相中,则水相1中含有$Al^{3+}$;若向过量烧碱的溶液中逐滴加入少量水相1的溶液,可观察到的现象为:先产生白色沉淀,后白色沉淀快速溶解。
(4)反萃取过程中$BeA_{2}(HA)_{2}$与烧碱反应生成$Na_{2}[Be(OH)_{4}]$,化学方程式为$BeA_{2}(HA)_{2}+6NaOH=Na_{2}[Be(OH)_{4}]+4NaA + 2H_{2}O$;滤液2的主要成分为NaOH,可进入反萃取步骤再利用。
(2)快速冷却
(3)先产生白色沉淀,后白色沉淀快速溶解
(4)$BeA_{2}(HA)_{2}+6NaOH=Na_{2}[Be(OH)_{4}]+4NaA + 2H_{2}O$
(5)反萃取
解析 在本流程生产过程中,先将铝硅酸盐加热熔融后快速冷却得到其玻璃态,加入稀硫酸浸得到的滤渣成分为$H_{2}SiO_{3}$;“滤液1”中含有$Be^{2+}$和$Al^{3+}$,加入含HA的煤油后HA与$Be^{2+}$反应生成$BeA_{2}(HA)_{2}$进入有机相中,$Al^{3+}$进入水相1中;在有机相中加入过量氢氧化钠后$BeA_{2}(HA)_{2}$转化为$Na_{2}[Be(OH)_{4}]$进入水相2中,分离出含NaA的煤油;对水相2加热,$Na_{2}[Be(OH)_{4}]$转化为$Be(OH)_{2}$,通过过滤分离出来,最后通过一系列操作得到金属铍。
(2)熔融态物质冷却凝固时,若缓慢冷却则会形成晶体,若快速冷却则会形成非晶态,即玻璃态。
(3)“滤液1”中有$Be^{2+}$和$Al^{3+}$,加入含HA的煤油后HA将$Be^{2+}$萃取到有机相中,则水相1中含有$Al^{3+}$;若向过量烧碱的溶液中逐滴加入少量水相1的溶液,可观察到的现象为:先产生白色沉淀,后白色沉淀快速溶解。
(4)反萃取过程中$BeA_{2}(HA)_{2}$与烧碱反应生成$Na_{2}[Be(OH)_{4}]$,化学方程式为$BeA_{2}(HA)_{2}+6NaOH=Na_{2}[Be(OH)_{4}]+4NaA + 2H_{2}O$;滤液2的主要成分为NaOH,可进入反萃取步骤再利用。
2. [2017·全国卷Ⅲ,27(4)]重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为$FeO\cdot Cr_{2}O_{3}$,还含有硅、铝等杂质。制备流程如图所示:
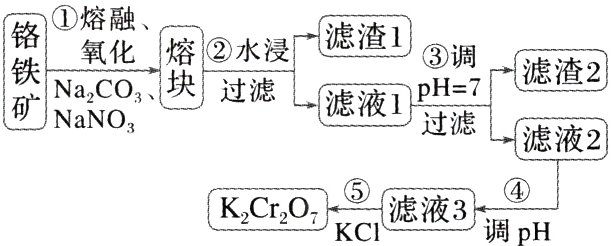
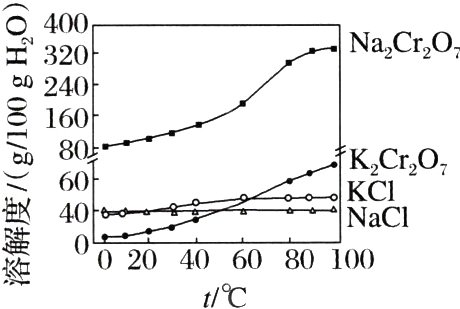
有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到$K_{2}Cr_{2}O_{7}$固体。冷却到__________(填字母)得到的$K_{2}Cr_{2}O_{7}$固体产品最多。
a. $80^{\circ}C$ b. $60^{\circ}C$ c. $40^{\circ}C$ d. $10^{\circ}C$
步骤⑤的反应类型是__________________。

有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到$K_{2}Cr_{2}O_{7}$固体。冷却到__________(填字母)得到的$K_{2}Cr_{2}O_{7}$固体产品最多。
a. $80^{\circ}C$ b. $60^{\circ}C$ c. $40^{\circ}C$ d. $10^{\circ}C$

步骤⑤的反应类型是__________________。
答案:
d 复分解反应
1. [2024·全国甲卷,26(3)]钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、铁、钴、锰的+2价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
炼锌废渣$\xrightarrow{稀H_{2}SO_{4}}酸浸\xrightarrow{H_{2}S}沉铜\xrightarrow{Na_{2}S_{2}O_{8}}沉锰\xrightarrow{NaOH调pH=4}沉淀\xrightarrow{NaClO}沉钴\xrightarrow{}滤液$
浸渣 CuS $MnO_{2}$ 滤渣 $Co(OH)_{3}$
注:加沉淀剂使一种金属离子浓度小于等于$10^{-5}mol\cdot L^{-1}$,其他金属离子不沉淀,即认为完全分离。
已知:①$K_{sp}(CuS)=6.3\times10^{-36}$,$K_{sp}(ZnS)=2.5\times10^{-22}$,$K_{sp}(CoS)=4.0\times10^{-21}$。
②以氢氧化物形式沉淀时,$\lg[c(M)/(mol\cdot L^{-1})]$和溶液pH的关系如图所示。

假设“沉铜”后得到的滤液中$c(Zn^{2+})$和$c(Co^{2+})$均为$0.10mol\cdot L^{-1}$,向其中加入$Na_{2}S$至$Zn^{2+}$沉淀完全,此时溶液中$c(Co^{2+})=$________$mol\cdot L^{-1}$,据此判断能否实现$Zn^{2+}$和$Co^{2+}$的完全分离?________(填“能”或“不能”)。
炼锌废渣$\xrightarrow{稀H_{2}SO_{4}}酸浸\xrightarrow{H_{2}S}沉铜\xrightarrow{Na_{2}S_{2}O_{8}}沉锰\xrightarrow{NaOH调pH=4}沉淀\xrightarrow{NaClO}沉钴\xrightarrow{}滤液$
浸渣 CuS $MnO_{2}$ 滤渣 $Co(OH)_{3}$
注:加沉淀剂使一种金属离子浓度小于等于$10^{-5}mol\cdot L^{-1}$,其他金属离子不沉淀,即认为完全分离。
已知:①$K_{sp}(CuS)=6.3\times10^{-36}$,$K_{sp}(ZnS)=2.5\times10^{-22}$,$K_{sp}(CoS)=4.0\times10^{-21}$。
②以氢氧化物形式沉淀时,$\lg[c(M)/(mol\cdot L^{-1})]$和溶液pH的关系如图所示。

假设“沉铜”后得到的滤液中$c(Zn^{2+})$和$c(Co^{2+})$均为$0.10mol\cdot L^{-1}$,向其中加入$Na_{2}S$至$Zn^{2+}$沉淀完全,此时溶液中$c(Co^{2+})=$________$mol\cdot L^{-1}$,据此判断能否实现$Zn^{2+}$和$Co^{2+}$的完全分离?________(填“能”或“不能”)。
答案:
$1.6×10^{-4}$ 不能
解析 假设“沉铜”后得到的滤液中$c(Zn^{2 + })$和$c(Co^{2 + })$均为$0.10\ mol\cdot L^{-1}$,向其中加入$Na_{2}S$至$Zn^{2 + }$沉淀完全,此时溶液中$c(S^{2 - })=\frac{2.5×10^{-22}}{10^{-5}}\ mol\cdot L^{-1}=2.5×10^{-17}\ mol\cdot L^{-1}$,则$c(Co^{2 + })=\frac{4.0×10^{-21}}{2.5×10^{-17}}\ mol\cdot L^{-1}=1.6×10^{-4}\ mol\cdot L^{-1}$,说明大部分$Co^{2 + }$也转化为硫化物沉淀,不能实现$Zn^{2 + }$和$Co^{2 + }$的完全分离。
解析 假设“沉铜”后得到的滤液中$c(Zn^{2 + })$和$c(Co^{2 + })$均为$0.10\ mol\cdot L^{-1}$,向其中加入$Na_{2}S$至$Zn^{2 + }$沉淀完全,此时溶液中$c(S^{2 - })=\frac{2.5×10^{-22}}{10^{-5}}\ mol\cdot L^{-1}=2.5×10^{-17}\ mol\cdot L^{-1}$,则$c(Co^{2 + })=\frac{4.0×10^{-21}}{2.5×10^{-17}}\ mol\cdot L^{-1}=1.6×10^{-4}\ mol\cdot L^{-1}$,说明大部分$Co^{2 + }$也转化为硫化物沉淀,不能实现$Zn^{2 + }$和$Co^{2 + }$的完全分离。
查看更多完整答案,请扫码查看


