第37页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
3. [2023·北京,16(3)]近年研究发现,电催化$CO_{2}$和含氮物质($NO_{3}^{-}$等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的$KNO_{3}$溶液通$CO_{2}$至饱和,在电极上反应生成$CO(NH_{2})_{2}$,电解原理如图所示。

①电极b是电解池的____________极。
②电解过程中生成尿素的电极反应式是
______________________________。

①电极b是电解池的____________极。
②电解过程中生成尿素的电极反应式是
______________________________。
答案:
①阳 ②$2NO_{3}^{-} + 16e^{-} + CO_{2} + 18H^{+} = CO(NH_{2})_{2} + 7H_{2}O$
解析 ①电极 b 上发生$H_{2}O$失电子生成$O_{2}$的氧化反应,是电解池的阳极。②a 极硝酸根离子得电子转化为尿素,再结合酸性环境可分析出电极反应式。
解析 ①电极 b 上发生$H_{2}O$失电子生成$O_{2}$的氧化反应,是电解池的阳极。②a 极硝酸根离子得电子转化为尿素,再结合酸性环境可分析出电极反应式。
4. [2023·湖南,17(2)]工业上以粗镓为原料,制备超纯$Ga(CH_{3})_{3}$的工艺流程如下:

已知:金属Ga的化学性质和Al相似,Ga的熔点为29.8 ℃。
“电解精炼”装置如图所示,电解池温度控制在40~45 ℃的原因是____________________________,阴极的电极反应式为______________________________。

已知:金属Ga的化学性质和Al相似,Ga的熔点为29.8 ℃。
“电解精炼”装置如图所示,电解池温度控制在40~45 ℃的原因是____________________________,阴极的电极反应式为______________________________。
答案:
确保生成的 Ga 为液体,便于从出料口流出 $[Ga(OH)_{4}]^{-} + 3e^{-} = Ga + 4OH^{-}$
解析 镓的熔点为 29.8℃,电解精炼温度需高于镓的熔点,因此电解池温度控制在 40~45℃。Ga 和 Al 性质相似,电解精炼过程中粗镓在阳极失电子产生的$Ga^{3+}$在$NaOH$溶液中形成$[Ga(OH)_{4}]^{-}$,$[Ga(OH)_{4}]^{-}$在阴极得电子被还原为 Ga,故阴极反应为$[Ga(OH)_{4}]^{-} + 3e^{-} = Ga + 4OH^{-}$。
解析 镓的熔点为 29.8℃,电解精炼温度需高于镓的熔点,因此电解池温度控制在 40~45℃。Ga 和 Al 性质相似,电解精炼过程中粗镓在阳极失电子产生的$Ga^{3+}$在$NaOH$溶液中形成$[Ga(OH)_{4}]^{-}$,$[Ga(OH)_{4}]^{-}$在阴极得电子被还原为 Ga,故阴极反应为$[Ga(OH)_{4}]^{-} + 3e^{-} = Ga + 4OH^{-}$。
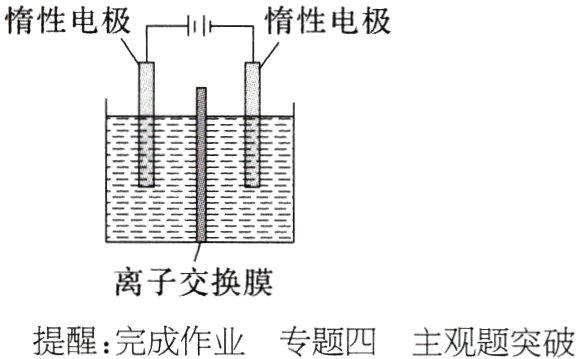
5. [2021·山东,17(4)]利用膜电解技术(装置如图所示),以$Na_{2}CrO_{4}$为主要原料制备$Na_{2}Cr_{2}O_{7}$的总反应的化学方程式为$4Na_{2}CrO_{4}$
$+ 4H_{2}O$ $\xlongequal[]{电解}$ $2Na_{2}Cr_{2}O_{7}$ + 4NaOH + $2H_{2}$↑ + $O_{2}$↑。则$Na_{2}Cr_{2}O_{7}$在__________(填“阴”或“阳”)极室制得,电解时通过膜的离子主要为__________。
$+ 4H_{2}O$ $\xlongequal[]{电解}$ $2Na_{2}Cr_{2}O_{7}$ + 4NaOH + $2H_{2}$↑ + $O_{2}$↑。则$Na_{2}Cr_{2}O_{7}$在__________(填“阴”或“阳”)极室制得,电解时通过膜的离子主要为__________。

答案:
阳 $Na^{+}$
查看更多完整答案,请扫码查看


