第40页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
4. (2023·浙江1月选考,14)标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知$O_{2}(g)$和$Cl_{2}(g)$的相对能量为0],下列说法不正确的是 ( )
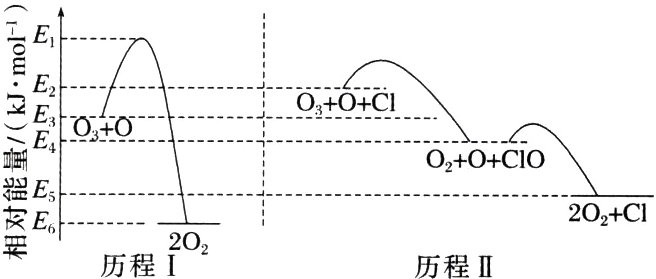
A. $E_{6}-E_{3}=E_{5}-E_{2}$
B. 可计算$Cl—Cl$键能为$2(E_{2}-E_{3})\ kJ\cdot mol^{-1}$
C. 相同条件下,$O_{3}$的平衡转化率:历程Ⅱ>历程I
D. 历程I、历程Ⅱ中速率最快的一步反应的热化学方程式为$ClO(g)+O(g)\xlongequal{\;\;}O_{2}(g)+Cl(g)$ $\Delta H=(E_{5}-E_{4})\ kJ\cdot mol^{-1}$

A. $E_{6}-E_{3}=E_{5}-E_{2}$
B. 可计算$Cl—Cl$键能为$2(E_{2}-E_{3})\ kJ\cdot mol^{-1}$
C. 相同条件下,$O_{3}$的平衡转化率:历程Ⅱ>历程I
D. 历程I、历程Ⅱ中速率最快的一步反应的热化学方程式为$ClO(g)+O(g)\xlongequal{\;\;}O_{2}(g)+Cl(g)$ $\Delta H=(E_{5}-E_{4})\ kJ\cdot mol^{-1}$
答案:
4. C [对比两个历程可知,历程Ⅱ中增加了催化剂,降低了反应的活化能,加快了反应速率。催化剂能降低活化能,但是不能改变反应的焓变,因此$E_{6}-E_{3}=E_{5}-E_{2}$,A正确;已知$Cl_{2}(g)$的相对能量为0,对比两个历程可知,$Cl(g)$的相对能量为$(E_{2}-E_{3})\ kJ\cdot mol^{-1}$,则$Cl - Cl$键能为$2(E_{2}-E_{3})\ kJ\cdot mol^{-1}$,B正确;催化剂不能改变反应的平衡转化率,因此相同条件下,$O_{3}$的平衡转化率:历程Ⅱ = 历程Ⅰ,C错误;活化能越低,反应速率越快,由图像可知,历程Ⅱ中第二步反应的活化能最低,所以速率最快的一步反应的热化学方程式为$ClO(g)+O(g)\xlongequal{\;\;}O_{2}(g)+Cl(g)$ $\Delta H=(E_{5}-E_{4})\ kJ\cdot mol^{-1}$,D正确。
查看更多完整答案,请扫码查看


