2026年薪火金卷高考仿真模拟卷化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年薪火金卷高考仿真模拟卷化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
7. 由含硒废料(主要含$S$、$Se$、${Fe2O3}$、${CuO}$、${ZnO}$、${SiO2}$等)在实验室中制取硒的流程如图:
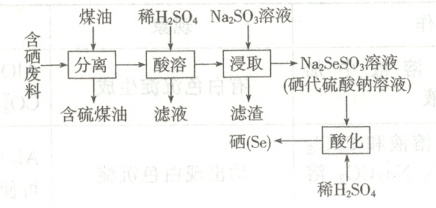
下列说法错误的是(
A.“分离”时得到含硫煤油的方法是分液
B.“酸溶”操作的目的是除去废料中的金属氧化物
C.“浸取”后的分离操作用玻璃仪器为烧杯、漏斗、玻璃棒
D.“酸化”时发生反应的离子方程式:${SeSO^{2-}_{3} + 2H^+ \xlongequal{} Se \downarrow + SO2 \uparrow + H2O}$

下列说法错误的是(
A
)A.“分离”时得到含硫煤油的方法是分液
B.“酸溶”操作的目的是除去废料中的金属氧化物
C.“浸取”后的分离操作用玻璃仪器为烧杯、漏斗、玻璃棒
D.“酸化”时发生反应的离子方程式:${SeSO^{2-}_{3} + 2H^+ \xlongequal{} Se \downarrow + SO2 \uparrow + H2O}$
答案:
7. A ["分离"时得到含硫煤油为分离固液的操作,方法是过滤,A错误;金属氧化物能和酸反应,"酸溶"操作的目的是除去废料中的金属氧化物,B正确;"浸取"后分离固液的操作为过滤,所用玻璃仪器为烧杯、漏斗、玻璃棒,C正确;"酸化"时${SeSO^{2-}_{3}}$转化为Se和二氧化硫,发生反应的离子方程式:${SeSO^{2-}_{3} + 2H^{+}\xlongequal{}Se\downarrow + SO_{2}\uparrow + H_{2}O}$,D正确。]
8. $25\ {^{\circ}C}$下,在含一定质量${Mg(OH)2}$的悬浊液中,分$6$次快速注入等量盐酸,体系$pH$变化曲线如图。下列说法不正确的是(

A.由图可知,酸碱中和反应速率大于${Mg(OH)2}$沉淀溶解速率
B.第$6$次加入盐酸时,${Mg(OH)2}$沉淀消耗完全
C.由图可知$K_{sp}[{Mg(OH)2}]=5× 10^{-32.8}$
D.上述过程中${Mg(OH)2}$的沉淀溶解平衡常数保持不变
C
)
A.由图可知,酸碱中和反应速率大于${Mg(OH)2}$沉淀溶解速率
B.第$6$次加入盐酸时,${Mg(OH)2}$沉淀消耗完全
C.由图可知$K_{sp}[{Mg(OH)2}]=5× 10^{-32.8}$
D.上述过程中${Mg(OH)2}$的沉淀溶解平衡常数保持不变
答案:
8. C [中和反应是一个进行极快的反应,瞬间就可完成,A正确;由图可知第6次加入盐酸后,溶液最终显酸性且pH不变,${Mg(OH)_{2}}$沉淀消耗完全,B正确;由图可知未加入稀盐酸时溶液的${pH = 10.6}$,$c{(H^{+})}=1× 10^{-10.6}$,则$c{(OH^{-})}=1× 10^{-3.4}$,$c{(Mg^{2+})}=\dfrac{1}{2}× 10^{-3.4}$,$K_{sp}{[Mg(OH)_{2}]}=c{(Mg^{2+})}· c^{2}{(OH^{-})}=\dfrac{1}{2}× 10^{-3.4}× (1× 10^{-3.4})^{2}=5× 10^{-11.2}$,C错误;沉淀溶解平衡常数只与温度有关,温度不变,沉淀溶解平衡常数保持不变,D正确。]
9. 电池中一种常用电解质的阴离子结构如图所示。$M$、$W$、$X$、$Y$、$Z$为原子序数依次增大的短周期元素,$X$和$Z$同族。下列说法正确的是(

A.$W$的氧化物的水化物是强酸
B.简单氢化物沸点:$Y>X>W$
C.${MZ2}$为极性分子
D.此阴离子中$M$和$W$的杂化方式相同
D
)
A.$W$的氧化物的水化物是强酸
B.简单氢化物沸点:$Y>X>W$
C.${MZ2}$为极性分子
D.此阴离子中$M$和$W$的杂化方式相同
答案:
9. D [M原子序数最小,且形成4条键,则M为C,X形成2条键,X和Z同族,则X为O,Z为S,由原子序数关系知,W为N,Y形成1条键,为F。${HNO_{3}}$为强酸,${HNO_{2}}$是弱酸,A错误;${H_{2}O}$常温下为液态,HF常温下为气态,${H_{2}O}$的沸点高于HF,B错误;${CS_{2}}$的结构与${CO_{2}}$相似(直线形:${S\xlongequal{}C\xlongequal{}S}$),正负电荷中心重合,为非极性分子,C错误;该阴离子中,C原子和N原子杂化方式均为${sp^{3}}$,D正确。]
10. 工业上煅烧含硫矿物产生的${SO2}$可以按如图流程脱除或利用。

已知:途径Ⅰ、Ⅱ、Ⅲ中均有空气参与;硫酸的结构简式为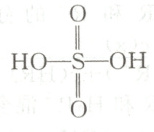
下列说法错误的是(
A.含硫矿物粉碎有利于提高“煅烧”效率
B.途径Ⅱ发生的反应为${2SO2 + O2 + 2CaCO3 \xlongequal{高温} 2CaSO4 + 2CO2}$
C.途径Ⅲ产生的${SO3}$也可以用浓硫酸吸收
D.$1\ mol\ X$最多可以与$1\ mol\ {NaOH}$反应

已知:途径Ⅰ、Ⅱ、Ⅲ中均有空气参与;硫酸的结构简式为

下列说法错误的是(
D
)A.含硫矿物粉碎有利于提高“煅烧”效率
B.途径Ⅱ发生的反应为${2SO2 + O2 + 2CaCO3 \xlongequal{高温} 2CaSO4 + 2CO2}$
C.途径Ⅲ产生的${SO3}$也可以用浓硫酸吸收
D.$1\ mol\ X$最多可以与$1\ mol\ {NaOH}$反应
答案:
10. D [含硫矿物粉碎有利于提高"煅烧"效率,A正确;途径Ⅱ发生的反应为${2SO_{2} + O_{2} + 2CaCO_{3}\xlongequal{高温}2CaSO_{4} + 2CO_{2}}$,B正确;途径Ⅲ产生的${SO_{3}}$也可以用浓硫酸吸收得到焦硫酸,再稀释转化为浓硫酸,可以避免三氧化硫与水反应形成大量酸雾,C正确;X经水解可到硫酸和甲醇,故$1\ mol$X最多可以与$2\ mol\ {NaOH}$反应得到$1\ mol$硫酸钠和$1\ mol$甲醇,D错误。]
查看更多完整答案,请扫码查看


