2026年薪火金卷高考仿真模拟卷化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年薪火金卷高考仿真模拟卷化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
1. 下列文物不属于传统无机非金属材料的是(

C
)
答案:
1. C [皇后玉玺通常由玉石制成,玉石主要成分为硅酸盐类矿物,属于传统无机非金属材料,A不符合题意;青瓷属于陶瓷,陶瓷是典型的传统无机非金属材料,B不符合题意;四羊青铜方尊的材料为青铜,青铜是铜锡合金,属于金属材料,而非传统无机非金属材料,C符合题意;击鼓陶俑为陶器,陶器属于陶瓷范畴,是传统无机非金属材料,D不符合题意。]
2. $N_A$是阿伏加德罗常数的值。下列说法正确的是(
A.$1\ mol$重水比$1\ mol$水多$N_A$个质子
B.${CH4}$和${C2H4}$混合气体$2.24\ L$(标准状况)下充分燃烧,则消耗${O2}$分子数目为$0.25N_A$
C.$1\ mol$甲基含有的电子数为$10N_A$
D.$1\ L\ 0.1\ mol·L^{-1}\ {FeCl3}$溶液制成胶体,含有${Fe(OH)3}$胶粒数一定小于$0.1N_A$
D
)A.$1\ mol$重水比$1\ mol$水多$N_A$个质子
B.${CH4}$和${C2H4}$混合气体$2.24\ L$(标准状况)下充分燃烧,则消耗${O2}$分子数目为$0.25N_A$
C.$1\ mol$甲基含有的电子数为$10N_A$
D.$1\ L\ 0.1\ mol·L^{-1}\ {FeCl3}$溶液制成胶体,含有${Fe(OH)3}$胶粒数一定小于$0.1N_A$
答案:
2. D [重水中的氢为${^2_1H}$,因此重水分子比水分子多2个中子,质子数相同,即$1\ mol$重水比$1\ mol$水多$2N_{A}$个中子,A错误;已知${CH_{4} + 2O_{2}\xlongequal{点燃}CO_{2} + 2H_{2}O}$、${C_{2}H_{4} + 3O_{2}\xlongequal{点燃}2CO_{2} + 2H_{2}O}$,混合气体$n=\dfrac{V}{V_{m}}=\dfrac{2.24\ L}{22.4\ L· mol^{-1}}=0.1\ mol$,若全部是${CH_{4}}$,则消耗$0.2\ mol\ {O_{2}}$,若全部是${C_{2}H_{4}}$,则消耗$0.3\ mol\ {O_{2}}$,因此消耗${O_{2}}$分子数目应在$0.2N_{A}~0.3N_{A}$之间,无法确定具体数值,B错误;$1\ mol$甲基${(\underset{· ·}{\overset{· ·}{H}} \overset{}{\underset{H}{\overset{H}{C}}} : H)}$含有电子$9\ mol$,电子数为$9N_{A}$,C错误;因为${Fe(OH)_{3}}$胶粒由很多个${Fe(OH)_{3}}$构成,$1\ L\ 0.1\ mol· L^{-1}\ {FeCl_{3}}$溶液制成胶体,含有${Fe(OH)_{3}}$胶粒数一定小于$0.1N_{A}$,D正确。]
3. 下列实验室中的做法错误的是(
A.液溴保存在磨口玻璃塞的棕色瓶中,并加少量水液封
B.酸碱中和滴定接近滴定终点时,用蒸馏水冲洗锥形瓶内壁
C.向氨水中逐滴加入硝酸银溶液制备银氨溶液
D.乙醇和浓硫酸制备乙烯时,温度计水银球插入液面以下
C
)A.液溴保存在磨口玻璃塞的棕色瓶中,并加少量水液封
B.酸碱中和滴定接近滴定终点时,用蒸馏水冲洗锥形瓶内壁
C.向氨水中逐滴加入硝酸银溶液制备银氨溶液
D.乙醇和浓硫酸制备乙烯时,温度计水银球插入液面以下
答案:
3. C [溴单质易挥发,${Br_{2}}$可以腐蚀橡胶,因此液溴保存在磨口玻璃塞的棕色瓶中,并加少量水液封,A正确;酸碱中和滴定接近滴定终点时,为使待测液充分反应,应用蒸馏水冲洗锥形瓶内壁,以使粘在内壁的待测液完全反应,B正确;向硝酸银溶液中逐滴加入氨水,至产生的沉淀恰好溶解,即可得到银氨溶液,C错误;乙醇和浓硫酸制备乙烯时,为控制反应温度迅速升温至$170\ ^{\circ}C$,温度计水银球插入液面以下,D正确。]
4. 化合物$R$是一种用于有机合成的催化剂,其网状结构片段如图。$X$、$Y$、$Z$、$W$为原子序数依次增大的短周期主族元素,四种元素原子序数之和为$29$,$W$的第一电离能大于同周期相邻元素。下列说法正确的是(

A.电负性:$W>Y>X$
B.${YF3}$中各原子均满足$8$电子稳定结构
C.同周期元素形成的单质中,$Z$的氧化性最强
D.化合物$R$中$Y$、$Z$、$W$原子的杂化类型相同
D
)
A.电负性:$W>Y>X$
B.${YF3}$中各原子均满足$8$电子稳定结构
C.同周期元素形成的单质中,$Z$的氧化性最强
D.化合物$R$中$Y$、$Z$、$W$原子的杂化类型相同
答案:
4. D [X、Y、Z、W为原子序数依次增大的短周期主族元素,X原子序数最小,形成1个共价键,X为氢;Z形成2个共价键,为氧;W的第一电离能大于同周期相邻元素,且原子序数大于氧,为磷;四种元素原子序数之和为29,则Y为硼。同周期元素从左到右金属性减弱,非金属性变强,元素的电负性增强;同主族元素由上而下金属性增强,非金属性逐渐减弱,元素电负性减弱;H的电负性强于B,故电负性:$W>X>Y$,A错误。${BF_{3}}$中B不是8电子结构,B错误。同周期元素从左到右,金属性减弱,非金属性增强;氧元素所在的同周期元素形成的单质中,氟单质的氧化性最强,C错误。化合物R中Y、W均形成4个共价键,为${sp^{3}}$杂化,氧形成2个共价键,还有2对孤电子对,也为${sp^{3}}$杂化,Y、Z、W原子的杂化类型相同,D正确。]
5. 含有未成对电子的物质具有顺磁性。下列物质一定具有顺磁性的是(
A.$[{Cu(NH3)4}]{SO4}$
B.${TiCl4}$
C.$[{Cu(NH3)2}]{Cl}$
D.${K4[Fe(CN)6]}$
A
)A.$[{Cu(NH3)4}]{SO4}$
B.${TiCl4}$
C.$[{Cu(NH3)2}]{Cl}$
D.${K4[Fe(CN)6]}$
答案:
5. A ${[[Cu(NH_{3})_{4}]SO_{4}}$中${Cu^{2+}}$的价电子排布式为${3d^{9}}$,含有未成对电子,属于顺磁性物质,A正确;${TiCl_{4}}$中${Ti^{4+}}$价电子排布式为${3s^{2}3p^{6}}$,整个结构中不含未成对电子,不属于顺磁性物质,B错误;${[Cu(NH_{3})_{2}]Cl}$中,${Cu^{+}}$价电子排布式为${3d^{10}}$,整个结构中不含未成对电子,不属于顺磁性物质,C错误;${K_{4}[Fe(CN)_{6}]}$中${Fe^{2+}}$价电子排布式为${3d^{6}}$,含有4个未成对电子,但4个K原子可提供4个电子,整个结构中不含未成对电子,不属于顺磁性物质,D错误。]
6. 化学用语可表示物质的组成和形成过程。下列化学用语表述错误的是(
A.中子数是$18$的硫的一种核素为${^{34}_{16}S}$
B.过氧化氢的电子式为 ,但${H2O2}$为极性分子
,但${H2O2}$为极性分子
C.聚对苯二甲酸对苯二酚酯的结构简式为
D.${MgBr2}$的形成过程可表示为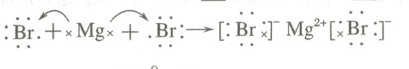
C
)A.中子数是$18$的硫的一种核素为${^{34}_{16}S}$
B.过氧化氢的电子式为
 ,但${H2O2}$为极性分子
,但${H2O2}$为极性分子C.聚对苯二甲酸对苯二酚酯的结构简式为

D.${MgBr2}$的形成过程可表示为
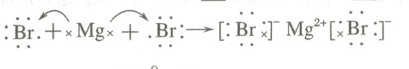
答案:
6. C
查看更多完整答案,请扫码查看


