2026年薪火金卷高考仿真模拟卷化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年薪火金卷高考仿真模拟卷化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
14. 已知 $MR$ 为易溶的弱酸弱碱盐,常温下,调节 $0.1\ mol· L^{-1}$ 的 $MR$ 溶液的 $pH$(忽略温度和溶液体积变化),溶液 $pH$ 与 $\lg X$ [$X$ 表示 $\frac{c(R^-)}{c(HR)}$ 或 $\frac{c(M^+)}{c(MOH)}$]变化情况如图所示。

下列说法正确的是(
A.$L_2$ 表示 $\lg\frac{c(R^-)}{c(HR)}$
B.$MR+H_2O\rightleftharpoons MOH+HR$ 的水解平衡常数 $K_h=10^{-2}$
C.$b$ 点溶液中:$c(HR)+c(MOH)=10c(R^-)+10c(M^+)$
D.两条直线上任意点均满足:$c(M^+)+c(MOH)=c(HR)+2c(R^-)$

下列说法正确的是(
B
)A.$L_2$ 表示 $\lg\frac{c(R^-)}{c(HR)}$
B.$MR+H_2O\rightleftharpoons MOH+HR$ 的水解平衡常数 $K_h=10^{-2}$
C.$b$ 点溶液中:$c(HR)+c(MOH)=10c(R^-)+10c(M^+)$
D.两条直线上任意点均满足:$c(M^+)+c(MOH)=c(HR)+2c(R^-)$
答案:
14. B [$\lg \frac{c(R^{-})}{c(HR)} = \lg \frac{c(R^{-})· c(H^{+})}{c(HR)· c(H^{+})} = \lg \frac{K_a}{c(H^{+})} = \lg K_a - \lg c(H^{+}) = \lg K_a + pH$,$\lg \frac{c(M^{+})}{c(MOH)} = \lg \frac{c(M^{+})· c(OH^{-})}{c(MOH)· c(OH^{-})} = \lg \frac{K_b}{c(OH^{-})} = \lg \frac{K_b}{\frac{K_w}{c(H^{+})}} = \lg K_b + 14 - pH$,根据图像曲线趋势,可知 $L_1$ 表示 $\lg \frac{c(R^{-})}{c(HR)}$,$L_2$ 表示 $\lg \frac{c(M^{+})}{c(MOH)}$。根据 $b$ 点进行计算,$\lg K_a + 6 = 1$,$K_a = 1× 10^{-5}\ mol· L^{-1}$,$\lg K_b + 14 - 6 = 1$,$K_b = 1× 10^{-7}\ mol· L^{-1}$。
由以上分析可知,$L_1$ 表示 $\lg \frac{c(R^{-})}{c(HR)}$,A 错误;$MR + H_2O\rightleftharpoons MOH + HR$ 的水解平衡常数 $K_h = \frac{c(MOH)· c(HR)}{c(M^{+})· c(R^{-})} = \frac{c(H^{+})· c(OH^{-})}{K_a· K_b} = 10^{-2}$,B 正确;$b$ 点溶液中 $\lg \frac{c(R^{-})}{c(HR)} = 1$,所以 $\frac{c(R^{-})}{c(HR)} = 10$,$c(R^{-}) = 10c(HR)$,$\lg \frac{c(M^{+})}{c(MOH)} = 1$,$\frac{c(M^{+})}{c(MOH)} = 10$,$c(M^{+}) = 10c(MOH)$,所以 $10c(HR) + 10c(MOH) = c(R^{-}) + c(M^{+})$,C 错误;$MR$ 为易溶的弱酸弱碱盐,结合溶液中存在的物料守恒,两条直线上任意点均满足:$c(M^{+}) + c(MOH) = c(HR) + c(R^{-})$,D 错误。]
由以上分析可知,$L_1$ 表示 $\lg \frac{c(R^{-})}{c(HR)}$,A 错误;$MR + H_2O\rightleftharpoons MOH + HR$ 的水解平衡常数 $K_h = \frac{c(MOH)· c(HR)}{c(M^{+})· c(R^{-})} = \frac{c(H^{+})· c(OH^{-})}{K_a· K_b} = 10^{-2}$,B 正确;$b$ 点溶液中 $\lg \frac{c(R^{-})}{c(HR)} = 1$,所以 $\frac{c(R^{-})}{c(HR)} = 10$,$c(R^{-}) = 10c(HR)$,$\lg \frac{c(M^{+})}{c(MOH)} = 1$,$\frac{c(M^{+})}{c(MOH)} = 10$,$c(M^{+}) = 10c(MOH)$,所以 $10c(HR) + 10c(MOH) = c(R^{-}) + c(M^{+})$,C 错误;$MR$ 为易溶的弱酸弱碱盐,结合溶液中存在的物料守恒,两条直线上任意点均满足:$c(M^{+}) + c(MOH) = c(HR) + c(R^{-})$,D 错误。]
15. (16 分)铌($Nb$)、钽($Ta$)为同族元素,在航空航天、武器装备等领域发挥着重要作用。以含铌、钽的尾矿(主要成分 $Nb_2O_5$、$Ta_2O_5$、$Al_2O_3$、$SiO_2$、$MgO$、$Fe_2O_3$ 等)为原料制备 $Nb_2O_5$、$Ta_2O_5$ 的工艺流程如下:
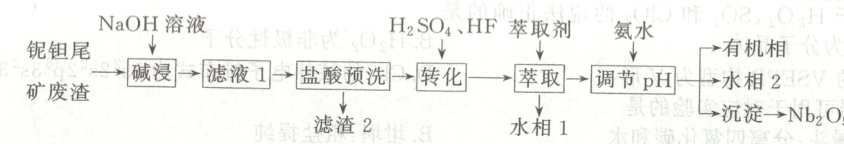
已知:①“碱浸”步骤中铌、钽发生的反应为 $Nb_2O_5+2NaOH=2NaNbO_3+H_2O$;$Ta_2O_5+2NaOH=2NaTaO_3+H_2O$。
②“转化”步骤中 $NaNbO_3$、$NaTaO_3$ 分别转化成氟铌酸根($NbF_7^{2-}$)、氟钽酸根($TaF_7^{2-}$)。
请回答下列问题:
(1)“滤液 1”中的主要成分为
(2)“盐酸预洗”的目的是
(3)①“转化”步骤中 $NaNbO_3$ 转化为 $NbF_7^{2-}$ 的离子方程式为 。
②“转化”步骤在 $90^{\circ}C$、硫酸酸化下完成,反应速率方程为:$v=kc^{1.2}(H^+)c^{1.1}(F^-)$。$H_2SO_4$ 的作用是
(4)$NbF_7^{2-}$、$TaF_7^{2-}$ 能被不同的有机溶剂选择性地萃取而与杂质分离,水相 1 和水相 2 中加入硫酸可以回收利用

已知:①“碱浸”步骤中铌、钽发生的反应为 $Nb_2O_5+2NaOH=2NaNbO_3+H_2O$;$Ta_2O_5+2NaOH=2NaTaO_3+H_2O$。
②“转化”步骤中 $NaNbO_3$、$NaTaO_3$ 分别转化成氟铌酸根($NbF_7^{2-}$)、氟钽酸根($TaF_7^{2-}$)。
请回答下列问题:
(1)“滤液 1”中的主要成分为
$Na[Al(OH)_4]$、$Na_2SiO_3$、$NaNbO_3$、$NaTaO_3$
(填化学式)。(2)“盐酸预洗”的目的是
将 $[Al(OH)_4]^{-}$ 转化为 $Al(OH)_3$ 沉淀,$SiO^{2-}_3$ 转化为 $H_2SiO_3$ 沉淀,过滤除去
。(3)①“转化”步骤中 $NaNbO_3$ 转化为 $NbF_7^{2-}$ 的离子方程式为 。
$NbO^{-}_3 + 7HF = NbF^{2-}_7 + 3H_2O + H^{+}$
②“转化”步骤在 $90^{\circ}C$、硫酸酸化下完成,反应速率方程为:$v=kc^{1.2}(H^+)c^{1.1}(F^-)$。$H_2SO_4$ 的作用是
增大 $H^{+}$ 浓度,加快反应速率
;不能用盐酸代替 $H_2SO_4$ 的理由是$Cl^{-}$ 会被 $NbO^{-}_3$、$TaO^{-}_3$ 氧化
。(4)$NbF_7^{2-}$、$TaF_7^{2-}$ 能被不同的有机溶剂选择性地萃取而与杂质分离,水相 1 和水相 2 中加入硫酸可以回收利用
$HF$
(填化学式),“调节 $pH$”步骤得到的沉淀是铌、钽的氢氧化物,煅烧氢氧化钽发生的化学方程式为$2Ta(OH)_5\xlongequal{煅烧}Ta_2O_5 + 5H_2O$
。
答案:
15. 解析 含铌、钽的尾矿(主要成分 ${Nb_{2}O_{5}}$、${Ta_{2}O_{5}}$、${Al_{2}O_{3}}$、${SiO_{2}}$、${MgO}$、${Fe_{2}O_{3}}$ 等)用 ${NaOH}$ 溶液碱浸,“碱浸”步骤中铌、钽发生的反应为 ${Nb_{2}O_{5} + 2NaOH = 2NaNbO_{3} + H_{2}O}$,${Ta_{2}O_{5} + 2NaOH = 2NaTaO_{3} + H_{2}O}$,${Al_{2}O_{3}}$ 转化为 ${Na[Al(OH)_{4}]}$,${SiO_{2}}$ 转化为 ${Na_{2}SiO_{3}}$,${MgO}$、${Fe_{2}O_{3}}$ 不和 ${NaOH}$ 溶液反应存在于滤渣中,向滤液中加入盐酸预洗,${[Al(OH)_{4}]^{-}}$ 转化为 ${Al(OH)_{3}}$ 沉淀,${SiO^{2-}_{3}}$ 转化为 ${H_{2}SiO_{3}}$ 沉淀,“转化”步骤中 ${NaNbO_{3}}$、${NaTaO_{3}}$ 分别转化成氟铌酸根(${NbF^{2-}_{7}}$)、氟钽酸根(${TaF^{2-}_{7}}$),加入萃取剂分离出氟铌酸根(${NbF^{2-}_{7}}$)、氟钽酸根(${TaF^{2-}_{7}}$),加入氨水调节 $pH$ 分离出的沉淀煅烧得到 ${Nb_{2}O_{5}}$、${Ta_{2}O_{5}}$。
(1)由分析可知,“滤液 1”中的主要成分为 ${Na[Al(OH)_{4}]}$、${Na_{2}SiO_{3}}$、${NaNbO_{3}}$、${NaTaO_{3}}$。
(2)“盐酸预洗”的目的是将 ${[Al(OH)_{4}]^{-}}$ 转化为 ${Al(OH)_{3}}$ 沉淀,${SiO^{2-}_{3}}$ 转化为 ${H_{2}SiO_{3}}$ 沉淀,过滤除去。
(3)①“转化”步骤中 ${NaNbO_{3}}$ 转化为 ${NbF^{2-}_{7}}$ 的离子方程式为 ${NbO^{-}_{3} + 7HF = NbF^{2-}_{7} + 3H_{2}O + H^{+}}$;②“转化”步骤在 $90\ ^{\circ}C$、硫酸酸化下完成,反应速率方程为:$v = kc^{1.2}({H^{+}})c^{1.1}({F^{-}})$。${H_{2}SO_{4}}$ 的作用是增大 ${H^{+}}$ 浓度,加快反应速率;不能用盐酸代替 ${H_{2}SO_{4}}$ 的理由是:${Cl^{-}}$ 会被 ${NbO^{-}_{3}}$、${TaO^{-}_{3}}$ 氧化。
(4)水相 1 和水相 2 中含有 ${F^{-}}$,根据强酸制取弱酸的原理,加入硫酸可以回收利用 ${HF}$,“调节 $pH$”步骤得到的沉淀是铌、钽的氢氧化物,煅烧氢氧化钽发生的反应方程式为 ${2Ta(OH)_{5}\xlongequal{煅烧}Ta_{2}O_{5} + 5H_{2}O}$。
答案 (1)${Na[Al(OH)_{4}]}$、${Na_{2}SiO_{3}}$、${NaNbO_{3}}$、${NaTaO_{3}}$
(2)将 ${[Al(OH)_{4}]^{-}}$ 转化为 ${Al(OH)_{3}}$ 沉淀,${SiO^{2-}_{3}}$ 转化为 ${H_{2}SiO_{3}}$ 沉淀,过滤除去
(3)①${NbO^{-}_{3} + 7HF = NbF^{2-}_{7} + 3H_{2}O + H^{+}}$ ②增大 ${H^{+}}$ 浓度,加快反应速率 ${Cl^{-}}$ 会被 ${NbO^{-}_{3}}$、${TaO^{-}_{3}}$ 氧化
(4)${HF}$ ${2Ta(OH)_{5}\xlongequal{煅烧}Ta_{2}O_{5} + 5H_{2}O}$
(1)由分析可知,“滤液 1”中的主要成分为 ${Na[Al(OH)_{4}]}$、${Na_{2}SiO_{3}}$、${NaNbO_{3}}$、${NaTaO_{3}}$。
(2)“盐酸预洗”的目的是将 ${[Al(OH)_{4}]^{-}}$ 转化为 ${Al(OH)_{3}}$ 沉淀,${SiO^{2-}_{3}}$ 转化为 ${H_{2}SiO_{3}}$ 沉淀,过滤除去。
(3)①“转化”步骤中 ${NaNbO_{3}}$ 转化为 ${NbF^{2-}_{7}}$ 的离子方程式为 ${NbO^{-}_{3} + 7HF = NbF^{2-}_{7} + 3H_{2}O + H^{+}}$;②“转化”步骤在 $90\ ^{\circ}C$、硫酸酸化下完成,反应速率方程为:$v = kc^{1.2}({H^{+}})c^{1.1}({F^{-}})$。${H_{2}SO_{4}}$ 的作用是增大 ${H^{+}}$ 浓度,加快反应速率;不能用盐酸代替 ${H_{2}SO_{4}}$ 的理由是:${Cl^{-}}$ 会被 ${NbO^{-}_{3}}$、${TaO^{-}_{3}}$ 氧化。
(4)水相 1 和水相 2 中含有 ${F^{-}}$,根据强酸制取弱酸的原理,加入硫酸可以回收利用 ${HF}$,“调节 $pH$”步骤得到的沉淀是铌、钽的氢氧化物,煅烧氢氧化钽发生的反应方程式为 ${2Ta(OH)_{5}\xlongequal{煅烧}Ta_{2}O_{5} + 5H_{2}O}$。
答案 (1)${Na[Al(OH)_{4}]}$、${Na_{2}SiO_{3}}$、${NaNbO_{3}}$、${NaTaO_{3}}$
(2)将 ${[Al(OH)_{4}]^{-}}$ 转化为 ${Al(OH)_{3}}$ 沉淀,${SiO^{2-}_{3}}$ 转化为 ${H_{2}SiO_{3}}$ 沉淀,过滤除去
(3)①${NbO^{-}_{3} + 7HF = NbF^{2-}_{7} + 3H_{2}O + H^{+}}$ ②增大 ${H^{+}}$ 浓度,加快反应速率 ${Cl^{-}}$ 会被 ${NbO^{-}_{3}}$、${TaO^{-}_{3}}$ 氧化
(4)${HF}$ ${2Ta(OH)_{5}\xlongequal{煅烧}Ta_{2}O_{5} + 5H_{2}O}$
查看更多完整答案,请扫码查看


