2026年薪火金卷高考仿真模拟卷化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年薪火金卷高考仿真模拟卷化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
6. 溴苯可用于生产镇痛解热药和止咳药,其制备、纯化流程如图。下列说法错误的是(
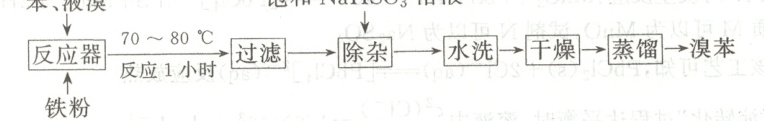
A.“过滤”可除去未反应的铁粉
B.“除杂”使用饱和${NaHSO_{3}}$溶液可除去剩余的溴单质
C.“干燥”时可使用浓硫酸作为干燥剂
D.“蒸馏”的目的是分离苯和溴苯
C
)
A.“过滤”可除去未反应的铁粉
B.“除杂”使用饱和${NaHSO_{3}}$溶液可除去剩余的溴单质
C.“干燥”时可使用浓硫酸作为干燥剂
D.“蒸馏”的目的是分离苯和溴苯
答案:
6.C [苯与液溴反应后剩余铁粉,不溶于苯,“过滤”可除去未反应的铁粉,A正确;${NaHSO_{3}}$可与${Br_{2}}$发生氧化还原反应,故使用饱和${NaHSO_{3}}$溶液可除去剩余的溴单质,B正确;水洗后须加入固体干燥剂${P_{2}O_{5}}$后蒸馏,不可用浓硫酸作为干燥剂,以防止蒸馏过程发生副反应,C错误;经过过滤、水洗、干燥后得到的是苯和溴苯的混合物,故蒸馏的主要目的是分离苯和溴苯,D正确。]
7. 下列有关物质结构和性质的比较中,逻辑推理关系与结论均正确的是(
A.根据${O}$与${N}$的电负性大小,推知羟胺(${NH_{2}OH}$)中分子间氢键强弱:${O-H·s O}>{N-H·s N}$
B.根据孤电子对与成键电子对之间斥力大小,推知${CO_{2}}$、${HCHO}$、${CCl_{4}}$键角依次减小
C.根据非金属性的大小,推知酸性:${HClO_{4}}>{H_{3}AsO_{4}}>{H_{2}SO_{4}}$
D.根据原子半径大小,推知第一电离能:${O}<{N}$
A
)A.根据${O}$与${N}$的电负性大小,推知羟胺(${NH_{2}OH}$)中分子间氢键强弱:${O-H·s O}>{N-H·s N}$
B.根据孤电子对与成键电子对之间斥力大小,推知${CO_{2}}$、${HCHO}$、${CCl_{4}}$键角依次减小
C.根据非金属性的大小,推知酸性:${HClO_{4}}>{H_{3}AsO_{4}}>{H_{2}SO_{4}}$
D.根据原子半径大小,推知第一电离能:${O}<{N}$
答案:
7.A [${O}$的电负性大于${N}$,因此羟胺中${O—H}$的氢键强度大于${N—H}$的氢键,A正确;${CO_{2}}$、${HCHO}$、${CCl_{4}}$的键角差异由杂化方式不同(键角:$\mathrm{sp}>\mathrm{sp}^{2}>\mathrm{sp}^{3}$)决定,推理错误,B错误;非金属性:${Cl}>{S}>{As}$,酸性${HClO_{4}}>{H_{2}SO_{4}}>{H_{3}AsO_{4}}$,C错误;${O}$的第一电离能小于${N}$的原因是${N}$的最高能级电子半满排布更稳定,与原子半径无关,D错误。]
8. 短周期主族元素${X}$、${Y}$、${Z}$、${W}$原子序数依次增大,${Y}$比${X}$原子的核外电子数多$1$个,${X}$与${Z}$原子最外层电子数之比为$2:3$。下列说法错误的是(
A.${X}$、${Y}$一定位于同一周期,${Y}$、${Z}$可能不位于同一周期
B.${X}$气态氢化物分子的空间构型一定是正四面体
C.${Y}$最高价氧化物对应的水化物可能是强电解质
D.若${Y}$、${Z}$、${W}$位于同一周期,则电负性:${W}>{Z}>{Y}$
B
)A.${X}$、${Y}$一定位于同一周期,${Y}$、${Z}$可能不位于同一周期
B.${X}$气态氢化物分子的空间构型一定是正四面体
C.${Y}$最高价氧化物对应的水化物可能是强电解质
D.若${Y}$、${Z}$、${W}$位于同一周期,则电负性:${W}>{Z}>{Y}$
答案:
8.B [${X}$、${Y}$一定位于同一周期,若二者位于第二周期,则${X}$为${C}$、${Y}$为${N}$,${Z}$可能为${O}$或${S}$,即${Y}$、${Z}$可能不位于同一周期,也可能位于同一周期,故A正确;${X}$为${C}$或${Si}$,其气态氢化物分子如${CH_{4}}$、${SiH_{4}}$的空间构型是四面体,若为乙烷、乙烯、丙烯等则不为正四面体,故B错误;${Y}$如果是${N}$,其最高价氧化物对应的水化物为硝酸,是强电解质,故C正确;若${Y}$、${Z}$、${W}$位于同一周期,则原子序数:${Y}<{Z}<{W}$,则电负性:${W}>{Z}>{Y}$,故D正确。]
9. 某化学小组探究二氧化碳与过氧化钠的反应。取适量${Na_{2}O_{2}}$粉末放入燃烧匙中,伸入充满${SO_{2}}$气体的集气瓶中,${SO_{2}}$气体与${Na_{2}O_{2}}$粉末接触时剧烈反应,淡黄色粉末变成白色粉末,并放出大量的热。根据反应现象,作如下假设:假设一:发生反应${2Na_{2}O_{2} + 2SO_{2}\xlongequal{}2Na_{2}SO_{3} + O_{2}}$;假设二:发生反应${Na_{2}O_{2} + SO_{2}\xlongequal{}Na_{2}SO_{4}}$;假设三:同时发生以上两个反应。该小组同学用一定量脱脂棉包裹少量${Na_{2}O_{2}}$粉末,放入充满${SO_{2}}$的圆底烧瓶中充分反应,圆底烧瓶中${O_{2}}$含量变化曲线如图所示。已知${Na_{2}SO_{3}}$比${SO_{2}}$更易被${O_{2}}$氧化。下列说法错误的是(
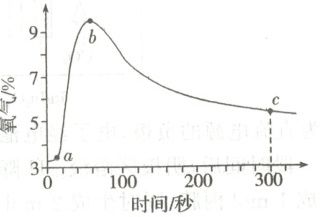
A.$ab$段发生的主要反应为${2Na_{2}O_{2} + 2SO_{2}\xlongequal{}2Na_{2}SO_{3} + O_{2}}$
B.$bc$段发生的主要反应为${2Na_{2}SO_{3} + O_{2}\xlongequal{}2Na_{2}SO_{4}}$
C.取$c$点固体加水溶解,静置,滴加${BaCl_{2}}$溶液产生白色沉淀,说明假设二成立
D.相同条件下,将${SO_{2}}$换成${CO_{2}}$后,重复上述操作,$300$秒时${O_{2}}$含量高于$c$点
C
)
A.$ab$段发生的主要反应为${2Na_{2}O_{2} + 2SO_{2}\xlongequal{}2Na_{2}SO_{3} + O_{2}}$
B.$bc$段发生的主要反应为${2Na_{2}SO_{3} + O_{2}\xlongequal{}2Na_{2}SO_{4}}$
C.取$c$点固体加水溶解,静置,滴加${BaCl_{2}}$溶液产生白色沉淀,说明假设二成立
D.相同条件下,将${SO_{2}}$换成${CO_{2}}$后,重复上述操作,$300$秒时${O_{2}}$含量高于$c$点
答案:
9.C [$ab$段${O_{2}}$含量增加,故存在${2Na_{2}O_{2} + 2SO_{2}\xlongequal{}2Na_{2}SO_{3} + O_{2}}$,A正确;$bc$段${O_{2}}$含量缓慢降低的可能原因:${2Na_{2}SO_{3} + O_{2}\xlongequal{}2Na_{2}SO_{4}}$,B正确;取$c$点固体加水溶解,静置,滴加${BaCl_{2}}$溶液产生白色沉淀,说明溶液中存在${Na_{2}SO_{4}}$,可能只发生反应②,也可能两反应均发生,即假设二或假设三成立均可能,C错误;相同条件下,将${SO_{2}}$换成${CO_{2}}$后,重复上述操作,只发生反应${2Na_{2}O_{2} + 2CO_{2}\xlongequal{}2Na_{2}CO_{3} + O_{2}}$,300秒时${O_{2}}$含量高于$c$点,D正确。]
10. 工业生产中利用方铅矿(主要成分为${PbS}$,含有${FeS_{2}}$等杂质)制备${PbSO_{4}}$晶体的工艺流程如图:
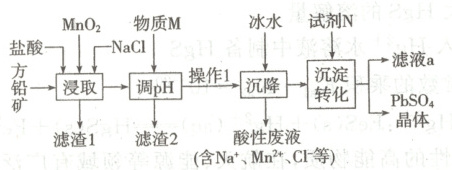
已知:${PbCl_{2}(s) + 2Cl^{-}(aq){<=>[][]}[PbCl_{4}]^{2-}(aq)}$;$K_{sp}({PbSO_{4}})=1×10^{-8}\ {mol^{2}· L^{-2}}$;$K_{sp}({PbCl_{2}})=1.6×10^{-5}\ {mol^{3}· L^{-3}}$。
下列说法错误的是(
A.“浸取”时发生反应:${MnO_{2} + PbS + 4H^{+} + 4Cl^{-}\xlongequal{}[PbCl_{4}]^{2-} + S + Mn^{2+} + 2H_{2}O}$
B.物质${M}$可以为${MnO}$,试剂${N}$可以为${Na_{2}SO_{4}}$
C.由该工艺可知,${PbCl_{2}(s) + 2Cl^{-}(aq){<=>[][]}[PbCl_{4}]^{2-}(aq)}$反应放热
D.“沉淀转化”过程达平衡时,溶液中$\dfrac{c^{2}({Cl^{-}})}{c({SO^{2-}_{4}})}=1.6×10^{3}\ {mol· L^{-1}}$

已知:${PbCl_{2}(s) + 2Cl^{-}(aq){<=>[][]}[PbCl_{4}]^{2-}(aq)}$;$K_{sp}({PbSO_{4}})=1×10^{-8}\ {mol^{2}· L^{-2}}$;$K_{sp}({PbCl_{2}})=1.6×10^{-5}\ {mol^{3}· L^{-3}}$。
下列说法错误的是(
C
)A.“浸取”时发生反应:${MnO_{2} + PbS + 4H^{+} + 4Cl^{-}\xlongequal{}[PbCl_{4}]^{2-} + S + Mn^{2+} + 2H_{2}O}$
B.物质${M}$可以为${MnO}$,试剂${N}$可以为${Na_{2}SO_{4}}$
C.由该工艺可知,${PbCl_{2}(s) + 2Cl^{-}(aq){<=>[][]}[PbCl_{4}]^{2-}(aq)}$反应放热
D.“沉淀转化”过程达平衡时,溶液中$\dfrac{c^{2}({Cl^{-}})}{c({SO^{2-}_{4}})}=1.6×10^{3}\ {mol· L^{-1}}$
答案:
10.C [“浸取”时盐酸与${MnO_{2}}$、${PbS}$发生反应生成${PbCl_{2}}$和${S}$,${MnO_{2}}$被还原成${Mn^{2+}}$,加入的${NaCl}$可促进反应${PbCl_{2}(s) + 2Cl^{-}(aq)⇌ [PbCl_{4}]^{2-}(aq)}$平衡正向移动,使更多的${Pb}$元素存在于溶液中,离子方程式为${MnO_{2} + PbS + 4H^{+} + 4Cl^{-}\xlongequal{}[PbCl_{4}]^{2-} + S + Mn^{2+} + 2H_{2}O}$,A正确;调${pH}$的目的是消耗溶液中的${H^{+}}$,促进${Fe^{3+}}$水解转化成${Fe(OH)_{3}}$除去,可选用${MnO}$、${Mn(OH)_{2}}$等,滤液${a}$中含有大量的${NaCl}$,但为确保${PbSO_{4}}$的产量,需加入过量的试剂${N(Na_{2}SO_{4})}$,B正确;${PbCl_{2}(s) + 2Cl^{-}(aq)⇌ [PbCl_{4}]^{2-}(aq)}$,温度降低,反应逆向移动,即平衡向左移,有利于${PbCl_{2}}$沉淀更完全,反应为吸热反应,C错误;“沉淀转化”过程中,沉淀的转化方程式为${PbCl_{2}(s) + SO^{2-}_{4}(aq)⇌ PbSO_{4}(s) + 2Cl^{-}(aq)}$,溶液中达到平衡时溶液中$\dfrac{c^{2}({Cl^{-}})}{c({SO^{2-}_{4}})}=\dfrac{\dfrac{c^{2}({Cl^{-}})· c({Pb^{2+}})}{c({SO^{2-}_{4}})· c({Pb^{2+}})}}{}=\dfrac{K_{sp}({PbCl_{2}})}{K_{sp}({PbSO_{4}})}=\dfrac{1.6× 10^{-5}}{1× 10^{-8}}\ \mathrm{mol· L^{-1}}=1.6× 10^{3}\ \mathrm{mol· L^{-1}}$,D正确。]
查看更多完整答案,请扫码查看


