2026年薪火金卷高考仿真模拟卷化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年薪火金卷高考仿真模拟卷化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
7. 关于非金属含氧酸及其盐的性质,下列说法正确的是(
A.Ag 与浓硝酸反应比与稀硝酸反应快,所以实验室通常用浓硝酸洗涤附着在试管内壁上的银镜
B.加热浓硫酸与 NaCl 固体的混合物可制备 HCl,说明浓硫酸酸性强于 HCl
C.将 CO₂通入 Ba(NO₃)₂溶液无明显现象,则将 SO₂通入 Ba(NO₃)₂溶液也无明显现象
D.向 NaClO 溶液中滴加酚酞试剂,先变红后褪色,证明 NaClO 在溶液中发生了水解反应
D
)A.Ag 与浓硝酸反应比与稀硝酸反应快,所以实验室通常用浓硝酸洗涤附着在试管内壁上的银镜
B.加热浓硫酸与 NaCl 固体的混合物可制备 HCl,说明浓硫酸酸性强于 HCl
C.将 CO₂通入 Ba(NO₃)₂溶液无明显现象,则将 SO₂通入 Ba(NO₃)₂溶液也无明显现象
D.向 NaClO 溶液中滴加酚酞试剂,先变红后褪色,证明 NaClO 在溶液中发生了水解反应
答案:
7.D [实验室通常用稀硝酸清洗银镜,稀硝酸成本更低,A错误;加热浓硫酸与${NaCl}$固体的化学方程式为${H_{2}SO_{4} + 2NaCl\xlongequal{\triangle}2HCl\uparrow + Na_{2}SO_{4}}$,反应能发生,是由于浓硫酸的沸点高于${HCl}$的沸点,${HCl}$不断离开反应体系,反应得以进行,与浓硫酸和${HCl}$的酸性大小无关,B错误;${SO_{2}}$通入${Ba(NO_{3})_{2}}$溶液中,${SO_{2}}$被氧化为硫酸根,会生成${BaSO_{4}}$白色沉淀,C错误;向${NaClO}$溶液中滴加酚酞试剂,先变红后褪色,是由于次氯酸根水解${ClO^{-} + H_{2}O⇌ HClO + OH^{-}}$,使溶液呈碱性,溶液变红由于生成의次氯酸具有漂白性,使得变红后的溶液褪色,D正确。]
8. 葡萄糖酸锌[Zn(C₆H₁₁O₇)₂]是一种常见的补锌药物。某研究小组使用葡萄糖酸钙制备葡萄糖酸锌的流程如下。下列有关说法不正确的是(
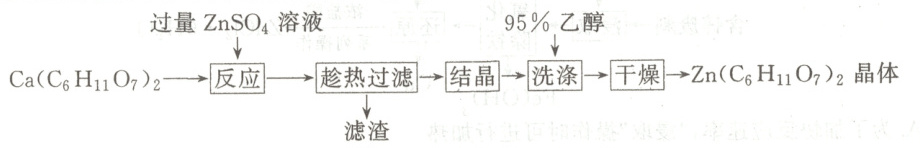
已知:葡萄糖酸钙和葡萄糖酸锌均可溶于冷水,易溶于热水,难溶于乙醇。
A.适当控制反应温度并不断搅拌有利于提高反应速率
B.趁热过滤后的滤液中存在的离子只有 Zn²⁺、C₆H₁₁O₇⁻
C.趁热过滤的目的是防止葡萄糖酸锌析出
D.使用 95%乙醇洗涤的目的是减少葡萄糖酸锌溶解
B
)
已知:葡萄糖酸钙和葡萄糖酸锌均可溶于冷水,易溶于热水,难溶于乙醇。
A.适当控制反应温度并不断搅拌有利于提高反应速率
B.趁热过滤后的滤液中存在的离子只有 Zn²⁺、C₆H₁₁O₇⁻
C.趁热过滤的目的是防止葡萄糖酸锌析出
D.使用 95%乙醇洗涤的目的是减少葡萄糖酸锌溶解
答案:
8.B [适当控制反应温度并不断搅拌,增加反应物接触的机会,有利于提高反应速率,A正确;趁热过滤后的滤液中存在的离子有${Zn^{2+}}$、${C_{6}H_{11}O^{-}_{7}}$、${SO^{2-}_{4}}$、${Ca^{2+}}$,B错误;趁热过滤的目的是防止葡萄糖酸锌析出,产品产率降低,C正确;使用$95\%$乙醇洗涤的目的是减少葡萄糖酸锌溶解,减少产物的损失,D正确。]
9. 已知 PbO₂受热分解为 Pb 的 +4 价和 +2 价的混合氧化物(+4 价的 Pb 能氧化浓盐酸生成 Cl₂)。1 mol PbO₂受热分解得到固体和 a mol 氧气,固体与足量的浓盐酸反应得氯气 b mol,若 a : b 为 3 : 2,则分解所得固体的成分及物质的量之比可能是(
①PbO₂、PbO:1 : 2
②PbO₂、Pb₃O₄:1 : 3
③Pb₃O₄,PbO:1 : 1
④PbO₂、Pb₃O₄、PbO:1 : 1 : 4
A.③④
B.②③
C.①②
D.①④
A
)①PbO₂、PbO:1 : 2
②PbO₂、Pb₃O₄:1 : 3
③Pb₃O₄,PbO:1 : 1
④PbO₂、Pb₃O₄、PbO:1 : 1 : 4
A.③④
B.②③
C.①②
D.①④
答案:
9.A [${PbO_{2}}$受热分解得到氧气和铅的氧化物的混合物(${Pb}$为$+4$、$+2$价),铅的氧化物的混合物再与浓盐酸作用,$+4$价${Pb}$被还原为$+2$价,${Cl^{-}}$被氧化为${Cl_{2}}$,此时得到${PbCl_{2}}$溶液,根据化合价变化可知,$1\ mol\ {PbO_{2}}$在上述转化过程中共转移$2\ mol\ {e^{-}}$,设该过程得到${O_{2}}$的物质的量为$a = 3x\ mol$,则${Cl_{2}}$的物质的量为$b = 2x\ mol$,利用得失电子守恒可得:$3x× 4 + 2x× 2 = 2$,解得$x = 0.125$,故知$1\ mol\ {PbO_{2}}$在受热分解过程中产生$0.375\ mol\ {O_{2}}$,利用原子守恒可知受热后的剩余固体中$n{(Pb)}:n{(O)} = 4:5$,结合选项可知只有③、④项满足$n{(Pb)}:n{(O)} = 4:5$,A正确。]
10. 选用下列装置制备磺酰胺[SO₂(NH₂)₂],原理为 SO₂Cl₂ + 4NH₃ = SO₂(NH₂)₂ + 2NH₄Cl。已知 SO₂Cl₂熔点为 -54.1℃,遇潮湿空气产生酸雾。下列说法正确的是(
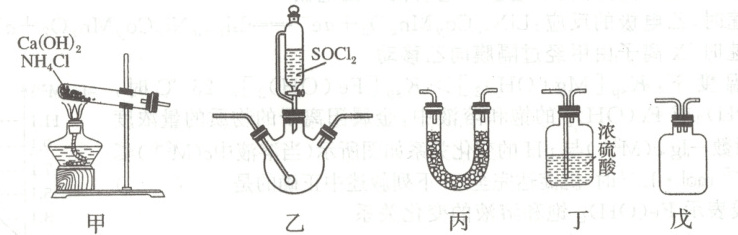
A.依次选用的装置为甲→丁→戊→乙→丙
B.实验开始前应先点燃酒精灯一段时间后再加入 SO₂Cl₂
C.装置丙内的试剂为 P₂O₅
D.装置乙内多孔球泡的作用是防倒吸
B
)
A.依次选用的装置为甲→丁→戊→乙→丙
B.实验开始前应先点燃酒精灯一段时间后再加入 SO₂Cl₂
C.装置丙内的试剂为 P₂O₅
D.装置乙内多孔球泡的作用是防倒吸
答案:
10.B [${SO_{2}Cl_{2}}$遇潮湿空气产生酸雾,需对通入的氨气进行干燥,氨气可与浓硫酸反应,不可用其进行干燥,可用浓硫酸处理尾气并吸收空气中水蒸气,故依次选取的装置为甲$\to$丙$\to$乙$\to$戊$\to$丁,A错误;实验开始前先点燃甲中酒精灯排尽装置内原有空气后再加入${SO_{2}Cl_{2}}$,防止${SO_{2}Cl_{2}}$遇潮湿空气产生酸雾,B正确;丙内试剂应不与氨气反应,为碱性干燥剂,如碱石灰等,不可使用酸性干燥剂${P_{2}O_{5}}$,C错误;乙中多孔球泡的作用是增大气液接触面积,使氨气与${SO_{2}Cl_{2}}$反应更充分,而非防倒吸,D错误。]
查看更多完整答案,请扫码查看


