2026年薪火金卷高考仿真模拟卷化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年薪火金卷高考仿真模拟卷化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
9. 具有抗菌、抗病毒活性的吡喃萘醌类有机物 $M$ 的结构简式如图。下列说法错误的是(
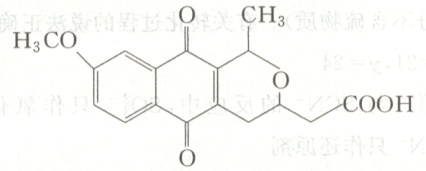
A.$M$ 的分子式为 $C_{17} H_{16} O_{6}$
B.$1 ~mol M$ 最多可与 $7 ~mol H_{2}$ 加成
C.$M$ 能与 $Na 、 NaOH$ 溶液和 $Na_{2} CO_{3}$ 溶液反应
D.$M$ 既能形成分子内氢键又能形成分子间氢键
B
)
A.$M$ 的分子式为 $C_{17} H_{16} O_{6}$
B.$1 ~mol M$ 最多可与 $7 ~mol H_{2}$ 加成
C.$M$ 能与 $Na 、 NaOH$ 溶液和 $Na_{2} CO_{3}$ 溶液反应
D.$M$ 既能形成分子内氢键又能形成分子间氢键
答案:
9.B [M的分子式为C17H16O6,A正确;根据1mol苯环需要3molH2,2mol羰基需要2molH2,1mol碳碳双键需要1molH2,则1molM最多可与6mol H2加成,B错误;M含有的官能团中羧基,能够与Na、NaOH溶液和Na2CO3溶液反应,C正确;两分子的M能够形成分子间氢键,M分子内部的羧基能够与相邻醚键上的氧原子形成分子内氢键,D正确。]
10. 工业上利用某炼铁废渣 (含 $Fe$ 和 $Cu$, 少量的油污、 $Fe_{2} O_{3} 、 CuS 、 CuO 、 CuCO_{3}$ ) 为原料生产 $CuCl_{2} · 2 H_{2} O$ 的工艺流程如图所示。下列有关该工艺的说法正确的是(
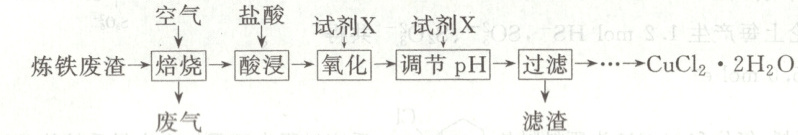
已知: 常温下 $Cu^{2+} 、 Fe^{2+} 、 Fe^{3+}$ 在碱性条件下沉淀的 $pH$ 如下表:

A.“焙烧”的目的是除掉少量的油污
B.“酸浸”过程中溶解 $Fe_{2} O_{3} 、 CuO$ 和 $CuCO_{3}$
C.“氧化”流程中, 试剂 $X$ 可为氯水且“调节 $pH$”范围是 $3.2 \leqslant pH<4.7$
D.“过滤”得到的滤液经过蒸发、干燥即可得到 $CuCl_{2} · 2 H_{2} O$
C
)
已知: 常温下 $Cu^{2+} 、 Fe^{2+} 、 Fe^{3+}$ 在碱性条件下沉淀的 $pH$ 如下表:

A.“焙烧”的目的是除掉少量的油污
B.“酸浸”过程中溶解 $Fe_{2} O_{3} 、 CuO$ 和 $CuCO_{3}$
C.“氧化”流程中, 试剂 $X$ 可为氯水且“调节 $pH$”范围是 $3.2 \leqslant pH<4.7$
D.“过滤”得到的滤液经过蒸发、干燥即可得到 $CuCl_{2} · 2 H_{2} O$
答案:
10.C [焙烧时通入空气,目的不仅是除去油污(油污燃烧),还包括将CuS氧化为CuO(便于酸浸),CuCO3分解为CuO等,Cu转化为CuO,Fe转化为Fe2O3,故A错误;焙烧时CuCO3会分解为CuO和CO2,因此酸浸时不存在CuCO3,溶解的是CuO(来自原CuO、CuS氧化及CuCO3分解),而非CuCO3本身,故B错误;氧化步骤需将Fe2+氧化为Fe3+以便除杂,氯水可作氧化剂,调节pH需使Fe3+完全沉淀(pH≥3.2)且Cu2+不沉淀(pH<4.7),范围为3.2≤pH<4.7,故C正确;CuCl2溶液蒸发干燥时会因水解生成Cu(OH)2或CuO,应通过蒸发浓缩、冷却结晶、过滤洗涤得到CuCl2·2H2O,故D错误。]
11. 某溶液可能含有等浓度的下列某些离子: $Na^{+} 、 Mg^{2+} 、 NH_{4}^{+} 、 H^{+} 、 Cl^{-} 、 SO_{3}^{2-} 、 SO_{4}^{2-} 、 NO_{3}^{-}$, 取溶液分别进行如下实验:
(1)加人 $HNO_{3}$ 酸化的 $Ba(NO_{3})_{2}$ 溶液产生白色沉淀;
(2)加人淀粉 $-KI$ 溶液, 呈蓝色;
(3)加人 $NaOH$ 溶液产生白色沉淀, 加热后产生有刺激性气味的气体。
下列说法错误的是(
A. 由(1)(2)可知一定有 $H^{+} 、 NO_{3}^{-} 、 SO_{4}^{2-}$
B. 若将(1)中的试剂换成盐酸酸化的 $BaCl_{2}$ 溶液, 不影响成分的判断
C. 实验(3)发生的反应为 $Mg^{2+}+NH_{4}^{+}+3 OH^{-} \stackrel{\triangle}{=} Mg(OH)_{2} \downarrow+NH_{3} \uparrow+H_{2} O$
D. 不能确定有无 $Cl^{-}$
(1)加人 $HNO_{3}$ 酸化的 $Ba(NO_{3})_{2}$ 溶液产生白色沉淀;
(2)加人淀粉 $-KI$ 溶液, 呈蓝色;
(3)加人 $NaOH$ 溶液产生白色沉淀, 加热后产生有刺激性气味的气体。
下列说法错误的是(
D
)A. 由(1)(2)可知一定有 $H^{+} 、 NO_{3}^{-} 、 SO_{4}^{2-}$
B. 若将(1)中的试剂换成盐酸酸化的 $BaCl_{2}$ 溶液, 不影响成分的判断
C. 实验(3)发生的反应为 $Mg^{2+}+NH_{4}^{+}+3 OH^{-} \stackrel{\triangle}{=} Mg(OH)_{2} \downarrow+NH_{3} \uparrow+H_{2} O$
D. 不能确定有无 $Cl^{-}$
答案:
11.D [①加入HNO3酸化的Ba(NO3)2溶液产生白色沉淀,则该白色沉淀为硫酸钡,原溶液中可能含有的SO42−,也可能含有的SO32−被硝酸氧化生成SO42−导致;②加入淀粉−KI溶液,呈蓝色,说明溶液中存在强氧化性离子,能将KI氧化成碘单质,则应一定含有H+、NO3−,从而排除SO32−,则原溶液中肯定存在SO42−;③加入NaOH溶液产生白色沉淀,可知一定有Mg2+,加热后产生有刺激性气味的气体,则一定有NH4+;又因各离子浓度相同,结合电荷守恒可知溶液中一定有Cl−,则一定没有Na+。由②可推知溶液中存在氧化性离子,则一定有H+、NO3−,从而排除SO32−,再结合①中白色沉淀现象,可知一定有SO42−,A正确;若将①中的试剂换成盐酸酸化的BaCl2溶液,则可通过白色沉淀现象直接确定SO42−存在,对最终成分的判断无影响,B正确;加入NaOH溶液产生白色沉淀,可知存在Mg2+,加热后产生有刺激性气味的气体,则存在NH4+,反应为Mg2++NH4++3OH−△Mg(OH)2↓+NH3↑+H2O,C正确;由以上分析可知溶液中一定有Cl−,D错误。]
12. $Au_{n}$ 纳米团簇能催化水煤气变换反应, 其微观反应机理如图 1 所示, 反应过程中相对能量的变化如图 2 所示。已知图 2 中 TS 表示过渡态, FS 表示稳定的共吸附。下列说法错误的是(
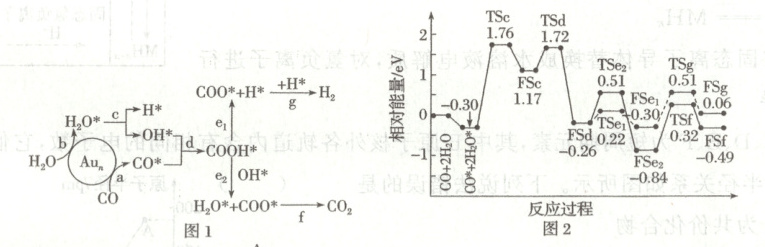
A.水煤气变换反应为 $H_{2} O+CO \stackrel{Au_{n}}{=} CO_{2}+H_{2}$
B.稳定性: $FSe_{2}$ 大于 $FSe_{1}$
C.水煤气变换反应的 $\Delta H<0$
D.制约总反应速率的反应为 $CO^{*}+OH^{*}=COOH^{*}$
D
)
A.水煤气变换反应为 $H_{2} O+CO \stackrel{Au_{n}}{=} CO_{2}+H_{2}$
B.稳定性: $FSe_{2}$ 大于 $FSe_{1}$
C.水煤气变换反应的 $\Delta H<0$
D.制约总反应速率的反应为 $CO^{*}+OH^{*}=COOH^{*}$
答案:
12.D [由图1可知,反应物为H2O和CO,生成物为CO2和H2,故水煤气变换反应为H2O+COAu CO2+H2,A正确;物质的能量越低越稳定,FSe2的能量比FSe1的低,故稳定性:FSe2大于FSe1,B正确;由图2可知,反应物总能量高于生成物总能量,故水煤气变换反应的△H<0,C正确;制约总反应速率的反应为活化能最大的反应,由图1、2可知,活化能最大的反应为H2O*=OH*+H*,D错误。]
查看更多完整答案,请扫码查看


