2025年非常学案高中化学选择性必修第一册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年非常学案高中化学选择性必修第一册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第80页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
1. 用$0.1000mol· L^{-1}HCl$溶液滴定未知浓度的$NaOH$溶液。有关该实验说法不正确的是 (
A.本实验可选用酚酞作指示剂
B.用酸式滴定管盛装$0.1000mol· L^{-1}HCl$溶液
C.用未知浓度的$NaOH$溶液润洗锥形瓶$2\sim3$次
D.滴定结束时俯视酸式滴定管读数,测量结果偏低
C
)A.本实验可选用酚酞作指示剂
B.用酸式滴定管盛装$0.1000mol· L^{-1}HCl$溶液
C.用未知浓度的$NaOH$溶液润洗锥形瓶$2\sim3$次
D.滴定结束时俯视酸式滴定管读数,测量结果偏低
答案:
1.C [中和滴定时锥形瓶不能润洗,C错误。]
2. 常温下,用$0.1000mol· L^{-1}$的$NaOH$溶液分别滴定$20.00mL$浓度均为$0.1000mol· L^{-1}$的盐酸和醋酸,得到两条滴定曲线,如图所示(已知醋酸钠溶液显碱性)。下列说法正确的是 (
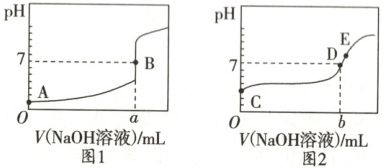
A.滴定前$CH_{3}COOH$的电离度约为$0.1\%$
B.图1表示醋酸的滴定曲线
C.达到B、D状态时,反应消耗的$NaOH$溶液的体积:$a>b$
D.滴定两种溶液时都可以用甲基橙作为指示剂
C
)
A.滴定前$CH_{3}COOH$的电离度约为$0.1\%$
B.图1表示醋酸的滴定曲线
C.达到B、D状态时,反应消耗的$NaOH$溶液的体积:$a>b$
D.滴定两种溶液时都可以用甲基橙作为指示剂
答案:
2.C [盐酸与醋酸的浓度均为$0.100\ 0\ mol·L^{-1}$,图1溶液起始${pH}=1$,表示盐酸的滴定曲线,图2溶液起始${pH}=3$,表示醋酸的滴定曲线。$0.100\ 0\ mol·L^{-1}$醋酸的${pH}=3$,即$c{(H^{+})}=1.0×10^{-3}\ mol·L^{-1}$,${CH_{3}COOH}$的电离度为$\frac{1.0×10^{-3}\ mol·L^{-1}}{0.100\ 0\ mol·L^{-1}}×100\%=1\%$,故A错误;图1表示盐酸的滴定曲线,故B错误;达到B状态时,$a=20.00$,若$b=20.00$,则恰好完全反应生成醋酸钠,溶液显碱性,而D状态溶液显中性,因此达到D状态时,$b<20.00$,故C正确;滴定${CH_{3}COOH}$溶液达到滴定终点时溶液呈碱性,不能用甲基橙作为指示剂,故D错误。]
3. 用标准盐酸滴定待测碱溶液时,下列操作会引起碱溶液浓度的测定值偏大的是 (
A.锥形瓶内的溶液在滴定过程中溅出
B.滴定前俯视读数,滴定后仰视读数
C.指示剂变色15s后又恢复为原来的颜色便停止滴定
D.滴定过程中锥形瓶内加少量蒸馏水
B
)A.锥形瓶内的溶液在滴定过程中溅出
B.滴定前俯视读数,滴定后仰视读数
C.指示剂变色15s后又恢复为原来的颜色便停止滴定
D.滴定过程中锥形瓶内加少量蒸馏水
答案:
3.B [根据$c(待测)=\frac{c(标准)· V(标准)}{V(待测)}$判断。A项,$V$(待测)的实际量减小,导致$V$(标准)偏小,测定值偏小;B项,滴定前俯视读数,滴定后仰视读数,导致$V$(标准)偏大,测定值偏大;C项,未达到滴定终点便停止滴定,导致$V$(标准)偏小,测定值偏小;D项,不影响测定结果。]
4. (教材互鉴:改编自苏教版教材)某同学用中和滴定法测定某烧碱溶液的浓度。
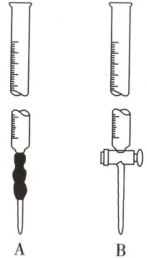
Ⅰ. 实验步骤:
(1)
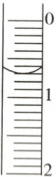
(2) 记录盛装$0.1000mol· L^{-1}$标准盐酸的酸式滴定管的初始读数。如果某时刻液面位置如图所示,则此时的读数为______。
(3) 滴定。滴定过程中,眼睛应始终注视____________。
(4) 滴定终点的现象是_______________。
Ⅱ. 数据记录:
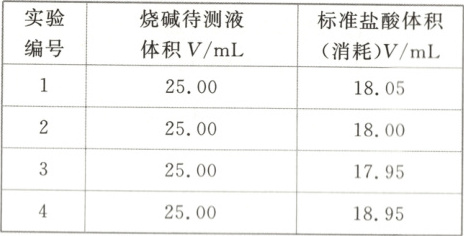
Ⅲ. 数据处理:
计算该烧碱溶液的浓度$c(NaOH)=__________mol·$$L^{-1}$(精确到小数点后4位)。
Ⅳ. 误差分析:
以下操作会导致测定结果偏高的是$\underline{AC}$(填字母)。
A. 未用盐酸标准溶液润洗滴定管
B. 装待测液前,锥形瓶中有少量蒸馏水
C. 滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D. 读数时,滴定前仰视,滴定后俯视

Ⅰ. 实验步骤:
(1)
A
用仪器$\underline{A}$(填“A”或“B”)量取待测烧碱溶液$25.00mL$于锥形瓶中,滴加2滴酚酞溶液作指示剂。(2) 记录盛装$0.1000mol· L^{-1}$标准盐酸的酸式滴定管的初始读数。如果某时刻液面位置如图所示,则此时的读数为______。

(3) 滴定。滴定过程中,眼睛应始终注视____________。
(4) 滴定终点的现象是_______________。
Ⅱ. 数据记录:

Ⅲ. 数据处理:
计算该烧碱溶液的浓度$c(NaOH)=__________mol·$$L^{-1}$(精确到小数点后4位)。
Ⅳ. 误差分析:
以下操作会导致测定结果偏高的是$\underline{AC}$(填字母)。
A. 未用盐酸标准溶液润洗滴定管
B. 装待测液前,锥形瓶中有少量蒸馏水
C. 滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D. 读数时,滴定前仰视,滴定后俯视
答案:
解析:Ⅲ.在四组数据中,第4组数据有明显误差,故舍弃。$\overline{V}=\frac{18.05+18.00+17.95}{3}\ mL=18.00\ mL$,$c{(NaOH)}=\frac{0.100\ 0\ mol·L^{-1}×0.018\ 00\ L}{0.025\ 00\ L}=0.072\ 0\ mol·L^{-1}$。Ⅳ.A项,未用盐酸标准溶液润洗滴定管,造成盐酸浓度偏小,所用盐酸体积偏大,测定结果偏高;B项,装待测液前,锥形瓶中有少量蒸馏水,无影响;C项,滴定前滴定管尖嘴部分有气泡,滴定后气泡消失,所用盐酸体积偏大,测定结果偏高;D项,读数时,滴定前仰视,滴定后俯视,造成盐酸读数偏小,结果偏低。
答案:Ⅰ.
(1)A
(2)$0.70$
(3)锥形瓶中溶液的颜色变化
(4)滴入最后半滴标准溶液后,溶液由红色恰好变为无色,且半分钟内不恢复原色 Ⅲ.$0.072\ 0$ Ⅳ.AC
答案:Ⅰ.
(1)A
(2)$0.70$
(3)锥形瓶中溶液的颜色变化
(4)滴入最后半滴标准溶液后,溶液由红色恰好变为无色,且半分钟内不恢复原色 Ⅲ.$0.072\ 0$ Ⅳ.AC
查看更多完整答案,请扫码查看


