第97页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
|类型|图像|分析|
|产生氢气速率—反应时间||0~t₀段:因为反应
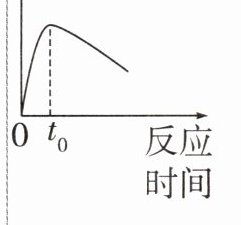
|压强—反应时间||密闭容器中:0~t₀段:反应有气体产生,且反应放热,导致压强
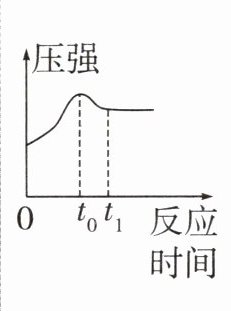
|温度—反应时间||0~t₀段:该反应为
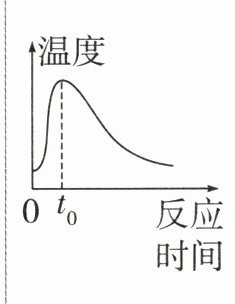
|产生氢气速率—反应时间||0~t₀段:因为反应
放热
(填"吸热"或"放热"),温度升高,反应速率加快;t₀之后:酸的浓度逐渐减小,反应速率逐渐减慢|
|压强—反应时间||密闭容器中:0~t₀段:反应有气体产生,且反应放热,导致压强
增大
(填"增大"或"减小",后同);t₀时:反应结束$;t₀~t_1$段:温度恢复至室温,导致压强减小
;但因为反应产生了气体,最终压强大于初始压强|
|温度—反应时间||0~t₀段:该反应为
放热
(填"吸热"或"放热")反应,温度逐渐升高
(填"升高"或"降低");t₀时:反应结束,温度达到最高值;t₀之后:温度逐渐恢复至室温|
答案:
放热 增大 减小 放热 升高
1. (黑白卷改编)铝是目前使用比较广泛的材料之一。如图是未经打磨的铝片与稀盐酸在密闭容器中反应时,用传感器测得反应容器内的压强随时间变化的情况。下列说法正确的是(
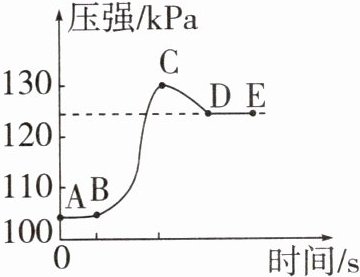
A.AB段容器中未发生化学反应
B.B点时,容器内的物质成分只有$AlCl_3$和水
C.压强增大是因为铝与稀盐酸反应
D.由图像推知,D点时容器内反应刚结束
C
)
A.AB段容器中未发生化学反应
B.B点时,容器内的物质成分只有$AlCl_3$和水
C.压强增大是因为铝与稀盐酸反应
D.由图像推知,D点时容器内反应刚结束
答案:
C
2. 分别取足量的表面积相同且打磨光亮的镁片、铁片与等体积、等浓度的稀盐酸反应,用数字化传感器测得压强随时间变化曲线如图所示。
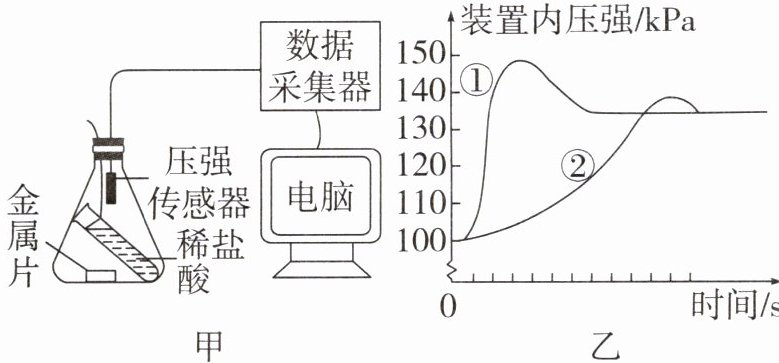
(1)反应结束,消耗镁片的质量
(2)曲线①对应的金属是
(3)曲线②对应反应的化学方程式为

(1)反应结束,消耗镁片的质量
<
(填">" "<"或"= ")铁片的质量。(2)曲线①对应的金属是
Mg
,判断依据是单位时间内曲线①对应反应产生氢气的体积多,反应速率快
。(3)曲线②对应反应的化学方程式为
Fe+2HCl=FeCl₂+H₂↑
,曲线上压强达到最高点后又略微下降的原因是反应结束,温度恢复至室温,压强减小
。
答案:
(1)<
(2)Mg 单位时间内曲线①对应反应产生氢气的体积多,反应速率快
(3)Fe+2HCl=FeCl₂+H₂↑ 反应结束,温度恢复至室温,压强减小
(1)<
(2)Mg 单位时间内曲线①对应反应产生氢气的体积多,反应速率快
(3)Fe+2HCl=FeCl₂+H₂↑ 反应结束,温度恢复至室温,压强减小
3. 镁与稀盐酸、稀硫酸均能发生反应。如图一是未经打磨过的镁条与少量稀盐酸反应时产生氢气的速率随时间的变化关系图。
图一
图二
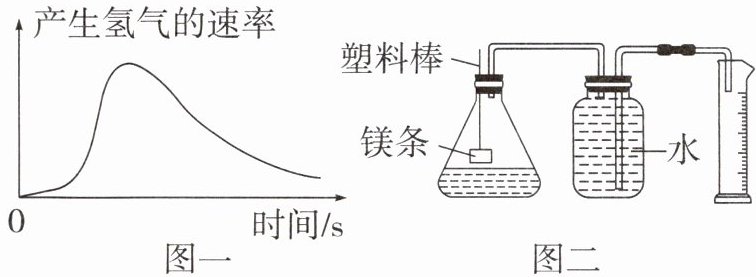
(1)反应刚开始时产生氢气的速率几乎为零,该过程主要发生反应的化学方程式为
(2)请根据所学知识解释产生氢气的速率到达最高点后下降的原因是
(3)为了比较镁与稀盐酸和稀硫酸的反应速率,利用图二装置将塑料棒向下移动,使等质量打磨过的镁条分别与等质量的相同溶质质量分数的稀盐酸和稀硫酸完全反应(酸足量),应记录的实验数据是
图一
图二

(1)反应刚开始时产生氢气的速率几乎为零,该过程主要发生反应的化学方程式为
MgO+2HCl=MgCl₂+H₂O
。(2)请根据所学知识解释产生氢气的速率到达最高点后下降的原因是
随着反应的进行,稀盐酸的浓度减小,反应速率逐渐降低
。(3)为了比较镁与稀盐酸和稀硫酸的反应速率,利用图二装置将塑料棒向下移动,使等质量打磨过的镁条分别与等质量的相同溶质质量分数的稀盐酸和稀硫酸完全反应(酸足量),应记录的实验数据是
相同时间内量筒内收集水的体积(或量筒内收集相同体积水所需要的时间)
。
答案:
(1)MgO+2HCl=MgCl₂+H₂O
(2)随着反应的进行,稀盐酸的浓度减小,反应速率逐渐降低
(3)相同时间内量筒内收集水的体积(或量筒内收集相同体积水所需要的时间)
(1)MgO+2HCl=MgCl₂+H₂O
(2)随着反应的进行,稀盐酸的浓度减小,反应速率逐渐降低
(3)相同时间内量筒内收集水的体积(或量筒内收集相同体积水所需要的时间)
查看更多完整答案,请扫码查看


