第117页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
4. 日常生活情境 融雪剂 氯盐融雪剂的种类繁多,其成分主要是氯化钠、氯化钙、氯化镁中的一种或多种。下表是这三种物质在不同温度时的溶解度,请回答下列问题。
|温度/℃|0|10|20|30|
|----|----|----|----|----|
|溶解度/g|NaCl|35.7|35.8|36.0|36.3|氯化钙|59.5|65.0|74.5|100|氯化镁|52.9|53.8|54.6|56.0|
(1)在通常情况下,纯水的冰点为0℃,20%的氯化钠溶液的冰点为-10℃,因此铺撒氯化钠可快速融雪的原因是
(2)同学们想要了解相同温度的条件下,等质量的三种物质饱和溶液的融雪效果,现要在20℃时配制符合要求的这三种溶液,则需要固体质量最小的是
(3)将(2)中配制好的三种溶液分别升温至30℃,溶液的溶质质量分数由大到小的关系为
|温度/℃|0|10|20|30|
|----|----|----|----|----|
|溶解度/g|NaCl|35.7|35.8|36.0|36.3|氯化钙|59.5|65.0|74.5|100|氯化镁|52.9|53.8|54.6|56.0|
(1)在通常情况下,纯水的冰点为0℃,20%的氯化钠溶液的冰点为-10℃,因此铺撒氯化钠可快速融雪的原因是
氯化钠溶于水形成氯化钠溶液后冰点降低
。(2)同学们想要了解相同温度的条件下,等质量的三种物质饱和溶液的融雪效果,现要在20℃时配制符合要求的这三种溶液,则需要固体质量最小的是
NaCl(或氯化钠)
。(3)将(2)中配制好的三种溶液分别升温至30℃,溶液的溶质质量分数由大到小的关系为
CaCl₂>MgCl₂>NaCl(或氯化钙>氯化镁>氯化钠)
。
答案:
(1)氯化钠溶于水形成氯化钠溶液后冰点降低
(2)NaCl(或氯化钠)
(3)CaCl₂>MgCl₂>NaCl(或氯化钙>氯化镁>氯化钠) 【解析】
(1)氯化钠溶于水形成氯化钠溶液后冰点降低,因此铺撒氯化钠可快速融雪。
(2)分析表格数据可知,在$20\;^{\circ}\text{C}$时三种物质的溶解度大小关系为氯化钙>氯化镁>氯化钠,因此要在$20\;^{\circ}\text{C}$时配制符合要求的这三种饱和溶液,需要固体质量最小的是氯化钠。
(3)三种物质的溶解度均随温度升高而增大,将$20\;^{\circ}\text{C}$时等质量的三种物质的饱和溶液分别升温至$30\;^{\circ}\text{C}$,溶质质量分数不变,与最初$20\;^{\circ}\text{C}$时三种物质饱和溶液的溶质质量分数相等,根据饱和溶液溶质质量分数计算公式$\frac{S}{100\;\text{g}+S}×100\%$,以及$20\;^{\circ}\text{C}$时三种物质的溶解度:氯化钙>氯化镁>氯化钠可知,所得溶液的溶质质量分数由大到小的关系为氯化钙>氯化镁>氯化钠。
(1)氯化钠溶于水形成氯化钠溶液后冰点降低
(2)NaCl(或氯化钠)
(3)CaCl₂>MgCl₂>NaCl(或氯化钙>氯化镁>氯化钠) 【解析】
(1)氯化钠溶于水形成氯化钠溶液后冰点降低,因此铺撒氯化钠可快速融雪。
(2)分析表格数据可知,在$20\;^{\circ}\text{C}$时三种物质的溶解度大小关系为氯化钙>氯化镁>氯化钠,因此要在$20\;^{\circ}\text{C}$时配制符合要求的这三种饱和溶液,需要固体质量最小的是氯化钠。
(3)三种物质的溶解度均随温度升高而增大,将$20\;^{\circ}\text{C}$时等质量的三种物质的饱和溶液分别升温至$30\;^{\circ}\text{C}$,溶质质量分数不变,与最初$20\;^{\circ}\text{C}$时三种物质饱和溶液的溶质质量分数相等,根据饱和溶液溶质质量分数计算公式$\frac{S}{100\;\text{g}+S}×100\%$,以及$20\;^{\circ}\text{C}$时三种物质的溶解度:氯化钙>氯化镁>氯化钠可知,所得溶液的溶质质量分数由大到小的关系为氯化钙>氯化镁>氯化钠。
5. 传统文化情境 其他文化遗产 古代中国的“五步产盐法”被列入国家级非物质文化遗产目录,该法又名“垦畦浇晒”产盐法,通过如图1所示过程从盐湖水中制得粗盐。
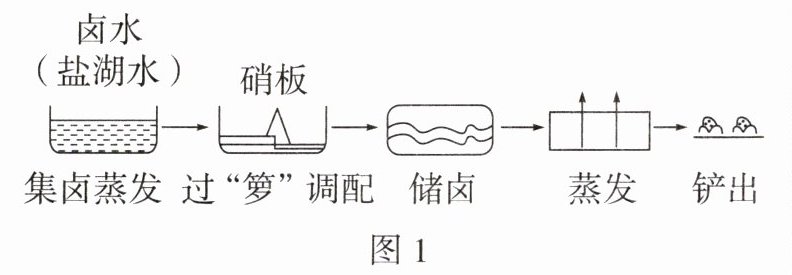
(1)集卤蒸发是将不同浓度的盐湖水引入垦畦地,借助风吹日晒使水分蒸发(溶质未结晶析出),在这个过程中,____(填“溶质质量”“溶剂质量”或“溶质质量分数”)不变。
(2)“蒸发”过程中析出氯化钠晶体利用的是蒸发结晶而不是降温结晶的主要原因为____。
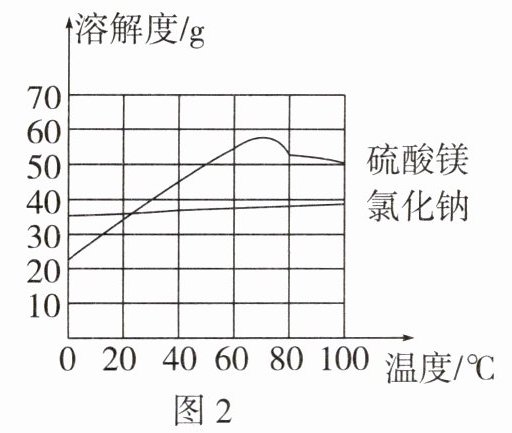
(3)铲出的盐中含有氯化钠和硫酸镁等,氯化钠和硫酸镁的溶解度曲线如图2所示①20℃时氯化钠的溶解度为36g,当“蒸发”过程中有氯化钠晶体析出时,剩余溶液中溶质氯化钠和水的质量比为____(填最简整数比)。
②刮湿热的南风凝结的盐没有苦味,而刮寒冷干燥的西北风凝结的盐会带有苦味结合溶解度曲线,请你解释风向不同,池盐成分不同的原因:____。
(4)请你就传承与保护传统制盐技艺提出你的方法:____。


(1)集卤蒸发是将不同浓度的盐湖水引入垦畦地,借助风吹日晒使水分蒸发(溶质未结晶析出),在这个过程中,____(填“溶质质量”“溶剂质量”或“溶质质量分数”)不变。
(2)“蒸发”过程中析出氯化钠晶体利用的是蒸发结晶而不是降温结晶的主要原因为____。
(3)铲出的盐中含有氯化钠和硫酸镁等,氯化钠和硫酸镁的溶解度曲线如图2所示①20℃时氯化钠的溶解度为36g,当“蒸发”过程中有氯化钠晶体析出时,剩余溶液中溶质氯化钠和水的质量比为____(填最简整数比)。
②刮湿热的南风凝结的盐没有苦味,而刮寒冷干燥的西北风凝结的盐会带有苦味结合溶解度曲线,请你解释风向不同,池盐成分不同的原因:____。
(4)请你就传承与保护传统制盐技艺提出你的方法:____。
答案:
(1)溶质质量
(2)氯化钠的溶解度受温度变化影响不大
(3)①9:25 ②氯化钠的溶解度受温度影响不大,刮南风(湿热)时,气温较高,水分蒸发快,氯化钠易结晶析出,硫酸镁的溶解度受温度影响变化较大,刮西北风(寒冷干燥)时,气温下降,硫酸镁易结晶析出
(4)利用电视媒体以创新的方式讲解“五步产盐法”的过程(合理即可)
(1)溶质质量
(2)氯化钠的溶解度受温度变化影响不大
(3)①9:25 ②氯化钠的溶解度受温度影响不大,刮南风(湿热)时,气温较高,水分蒸发快,氯化钠易结晶析出,硫酸镁的溶解度受温度影响变化较大,刮西北风(寒冷干燥)时,气温下降,硫酸镁易结晶析出
(4)利用电视媒体以创新的方式讲解“五步产盐法”的过程(合理即可)
6. 日常生活情境 自制冰棍 小明和小亮在家里配制蔗糖溶液,用于自制冰棍,结合蔗糖的溶解度表,回答下列问题。
|温度/℃|0|10|20|
|----|----|----|----|
|溶解度/g|182|191|204|
(1)20℃时,为了得到最甜的蔗糖溶液,二人决定配制100g饱和蔗糖溶液,该温度下蔗糖的溶解度为
(2)(黑白卷改编)取少量配好的饱和溶液进行品尝,小明认为溶液过甜,小亮仍坚持做最甜的冰棍。于是二人分别取30g饱和溶液,各自按如图方案(部分流程省略)制作冰棍。
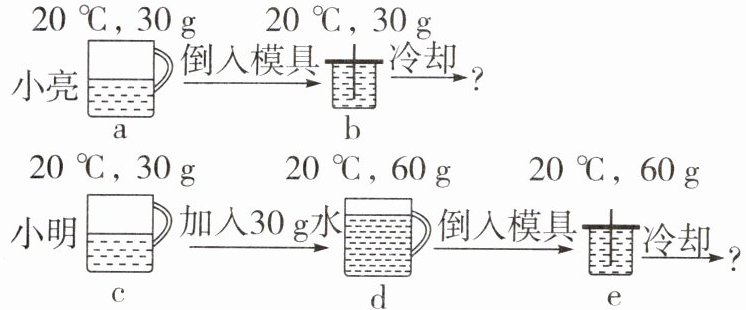
①c水杯中溶液的甜度
②冷却至0℃后,两个方案中模具
|温度/℃|0|10|20|
|----|----|----|----|
|溶解度/g|182|191|204|
(1)20℃时,为了得到最甜的蔗糖溶液,二人决定配制100g饱和蔗糖溶液,该温度下蔗糖的溶解度为
204
g,则需要取用蔗糖的质量最少为68
g(计算结果取整数)。(2)(黑白卷改编)取少量配好的饱和溶液进行品尝,小明认为溶液过甜,小亮仍坚持做最甜的冰棍。于是二人分别取30g饱和溶液,各自按如图方案(部分流程省略)制作冰棍。

①c水杯中溶液的甜度
>
(填“>”“=”或“<”)d水杯中溶液的甜度。②冷却至0℃后,两个方案中模具
b
(填“b”或“e”)内会有蔗糖晶体析出。
答案:
(1)204 68
(2)①> ②b
(1)204 68
(2)①> ②b
查看更多完整答案,请扫码查看


