第61页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
例 1 传统文化情境 科技成就 火药是我国古代四大发明之一,向火药中加入硝酸铜,其爆炸时会产生绿色火焰,发生的反应为$2\mathrm{C}\mathrm{u}(\mathrm{N}{\mathrm{O}}_{3}{)}_{2}\xlongequal{\triangle }2\mathrm{C}\mathrm{u}\mathrm{O}+{\mathrm{O}}_{2}\uparrow +4\mathrm{X}\uparrow$,其中 X 的化学式为 (
A. NO
B. $\mathrm{N}{\mathrm{O}}_{2}$
C. ${\mathrm{N}}_{2}$
D. Cu
【方法指导】
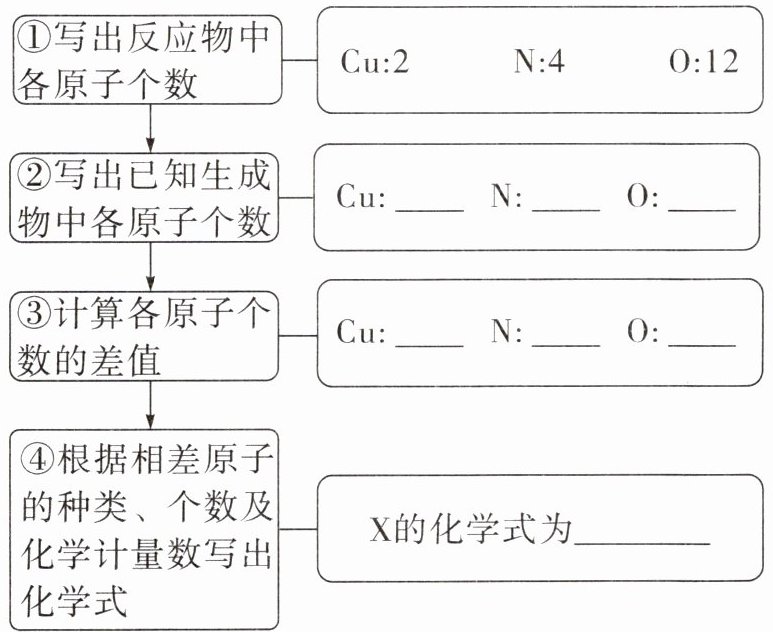
①写出反应物中各原子个数 Cu:2 N:4 O:12
②写出已知生成物中各原子个数 Cu:
③计算各原子个数的差值 Cu:
④根据相差原子的种类、个数及化学计量数写出化学式 X的化学式为
B
)A. NO
B. $\mathrm{N}{\mathrm{O}}_{2}$
C. ${\mathrm{N}}_{2}$
D. Cu
【方法指导】
①写出反应物中各原子个数 Cu:2 N:4 O:12
②写出已知生成物中各原子个数 Cu:
2
N:0
O:4
③计算各原子个数的差值 Cu:
0
N:4
O:8
④根据相差原子的种类、个数及化学计量数写出化学式 X的化学式为
NO₂

答案:
B 【方法指导】②2 0 4 ③0 4 8 ④NO₂
1. 科技前沿情境 航空航天 我国空间站的运转需要强大的能源供应,其发电担当是天和核心舱上的柔性太阳能电池翼。电池翼材料的生产过程中涉及化学反应:${\mathrm{A}\mathrm{s}}_{2}{\mathrm{O}}_{3}+3\mathrm{C}\xlongequal{\text{高温}}2\mathrm{A}\mathrm{s}+x\mathrm{C}\mathrm{O}\uparrow$,据此可推断 x 的值为 (
A.2
B.4
C.3
D.1
C
)A.2
B.4
C.3
D.1
答案:
C
2. 早在 3000 多年前,我国古代劳动人民就开始炼铜。火法炼铜的反应之一是${\mathrm{C}\mathrm{u}}_{\mathit{x}}\mathrm{S}+{\mathrm{O}}_{2}\xlongequal{\text{高温}}2\mathrm{C}\mathrm{u}+\mathrm{S}{\mathrm{O}}_{2}$,其中 x 为 (
A.1
B.2
C.3
D.4
B
)A.1
B.2
C.3
D.4
答案:
B
例 2 日常生活情境 生活用品 “84”消毒液是家庭常用消毒液,能够有效地杀灭多种细菌病毒,其有效成分主要是次氯酸钠($\mathrm{N}\mathrm{a}\mathrm{C}\mathrm{l}\mathrm{O}$)。工业上常用氢氧化钠($\mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}$)溶液和一种气体反应制备次氯酸钠,同时生成氯化钠和水,则该气体可能是 (
A. 二氧化硫
B. 二氧化氮
C. 氯气
D. 氮气
【方法指导】
①写出已知反应物和生成物的元素组成 已知反应物中的元素组成:
②根据化学反应前后元素种类不变判断一定含有的元素 该气体的组成元素中一定含有
C
)A. 二氧化硫
B. 二氧化氮
C. 氯气
D. 氮气
【方法指导】
①写出已知反应物和生成物的元素组成 已知反应物中的元素组成:
Na、O、H
生成物中的元素组成:Na、Cl、O、H
②根据化学反应前后元素种类不变判断一定含有的元素 该气体的组成元素中一定含有
Cl
,故选项中符合条件的气体是氯气
答案:
C 【方法指导】①Na、O、H Na、Cl、O、H ②Cl 氯气
3. 举重运动员举重前用白色的“镁粉”[有效成分是${\mathrm{M}\mathrm{g}}_{5}(\mathrm{O}\mathrm{H}{)}_{2}(\mathrm{C}{\mathrm{O}}_{3}{)}_{4}$]搓手,是因为“镁粉”质轻、吸水性好,可做防滑剂。“镁粉”$300^{\circ }C$即可以分解,其分解产物
A.$\mathrm{M}\mathrm{g}\mathrm{O}$
B.$\mathrm{C}{\mathrm{O}}_{2}$
C.${\mathrm{H}}_{2}\mathrm{O}$
D.$\mathrm{C}\mathrm{a}\mathrm{O}$
不
可
能
是 (D
)A.$\mathrm{M}\mathrm{g}\mathrm{O}$
B.$\mathrm{C}{\mathrm{O}}_{2}$
C.${\mathrm{H}}_{2}\mathrm{O}$
D.$\mathrm{C}\mathrm{a}\mathrm{O}$
答案:
D
4. 氯乙烷是赛场上的“化学大夫”,能迅速治疗伤痛。已知氯乙烷在氧气中完全燃烧生成二氧化碳、水和氯化氢,下列有关氯乙烷组成的说法正确的是 (
A.一定含有碳、氢、氯元素
B.一定含有氧、氢元素,可能含有氯元素
C.一定含有碳、氯元素,可能含有氢元素
D.一定含有氢、氯元素,可能含有碳元素
A
)A.一定含有碳、氢、氯元素
B.一定含有氧、氢元素,可能含有氯元素
C.一定含有碳、氯元素,可能含有氢元素
D.一定含有氢、氯元素,可能含有碳元素
答案:
A
例 3 柠檬醛是中国规定允许使用的食用香料,常存在于枫茅油和山苍子油中。现从山苍子油中提取7.6 g 柠檬醛,使其在空气中完全燃烧,生成 22 g 二氧化碳和 7.2 g 水,则柠檬醛中 (
A. 只含有碳、氢元素
B. 一定含碳、氢、氧元素
C. 一定含有碳、氢元素,可能含有氧元素
D. 碳、氢元素的原子个数比为$8:5$
【方法指导】
第1步:找出反应物与生成物及各自的质量。
反应物:7.6 g 柠檬醛、x g 氧气;生成物:22 g 二氧化碳、7.2 g 水。
第2步:定性推断物质所含元素。根据“化学反应前后元素种类不变”推出柠檬醛中一定含有____碳、氢____元素,可能含有氧元素。
第3步:定量计算物质所含元素。通过计算判断柠檬醛中是否含有氧元素。
①若柠檬醛中碳元素质量+氢元素质量= 柠檬醛的质量→____不含____氧元素;
②若柠檬醛中碳元素质量+氢元素质量<柠檬醛的质量→____含有____氧元素。
柠檬醛中碳元素的质量= 二氧化碳中碳元素的质量= $22\mathrm{g}× (\frac{12}{44}× 100\%)= 6\mathrm{g}$,柠檬醛中氢元素的质量= 水中氢元素的质量= $7.2\mathrm{g}× (\frac{2}{18}× 100\%)= 0.8\mathrm{g}$;$6\mathrm{g}+0.8\mathrm{g}= 6.8\mathrm{g}<7.6\mathrm{g}$,则柠檬醛中含有氧元素,氧元素的质量为____0.8 g____。
第4步:确定物质中各元素的原子个数比。柠檬醛中碳、氢、氧原子的个数比= $\frac{\text{碳元素质量}}{\text{碳的相对原子质量}}\colon \frac{\text{氢元素质量}}{\text{氢的相对原子质量}}\colon \frac{\text{氧元素质量}}{\text{氧的相对原子质量}}$= ____10:16:1____。
B
)A. 只含有碳、氢元素
B. 一定含碳、氢、氧元素
C. 一定含有碳、氢元素,可能含有氧元素
D. 碳、氢元素的原子个数比为$8:5$
【方法指导】
第1步:找出反应物与生成物及各自的质量。
反应物:7.6 g 柠檬醛、x g 氧气;生成物:22 g 二氧化碳、7.2 g 水。
第2步:定性推断物质所含元素。根据“化学反应前后元素种类不变”推出柠檬醛中一定含有____碳、氢____元素,可能含有氧元素。
第3步:定量计算物质所含元素。通过计算判断柠檬醛中是否含有氧元素。
①若柠檬醛中碳元素质量+氢元素质量= 柠檬醛的质量→____不含____氧元素;
②若柠檬醛中碳元素质量+氢元素质量<柠檬醛的质量→____含有____氧元素。
柠檬醛中碳元素的质量= 二氧化碳中碳元素的质量= $22\mathrm{g}× (\frac{12}{44}× 100\%)= 6\mathrm{g}$,柠檬醛中氢元素的质量= 水中氢元素的质量= $7.2\mathrm{g}× (\frac{2}{18}× 100\%)= 0.8\mathrm{g}$;$6\mathrm{g}+0.8\mathrm{g}= 6.8\mathrm{g}<7.6\mathrm{g}$,则柠檬醛中含有氧元素,氧元素的质量为____0.8 g____。
第4步:确定物质中各元素的原子个数比。柠檬醛中碳、氢、氧原子的个数比= $\frac{\text{碳元素质量}}{\text{碳的相对原子质量}}\colon \frac{\text{氢元素质量}}{\text{氢的相对原子质量}}\colon \frac{\text{氧元素质量}}{\text{氧的相对原子质量}}$= ____10:16:1____。
答案:
B 【方法指导】第2步:碳、氢 第3步:①不含 ②含有 0.8 g 第4步:10:16:1
查看更多完整答案,请扫码查看


