第60页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
7. (教材习题改编)如果采用以下物质分解的方法制取氧气,消耗相同质量的原料,得到氧气质量最多的是(
$A. H_2O_2$
$B. KMnO_4$
C. HgO
$D. H_2O$
D
)$A. H_2O_2$
$B. KMnO_4$
C. HgO
$D. H_2O$
答案:
D
8. 西晋张华著作《博物志》中记载:“烧白石$(CaCO_3)$作石灰(CaO)……”,某小组利用上述原理制备生石灰,记录剩余固体质量与反应时间的关系如图所示,计算理论上制得生石灰的质量。


答案:
解:25g石灰石高温完全分解产生二氧化碳的质量为$25g - 16.2g = 8.8g$ 设25g石灰石理论上制得生石灰的质量为x ${CaCO_{3}\xlongequal{\text{高温}}CaO + CO_{2}\uparrow }$
56 44
x 8.8g
$\frac {56}{44}=\frac {x}{8.8g}$
$x=11.2g$
答:25g石灰石理论上可制得生石灰的质量为11.2g。
56 44
x 8.8g
$\frac {56}{44}=\frac {x}{8.8g}$
$x=11.2g$
答:25g石灰石理论上可制得生石灰的质量为11.2g。
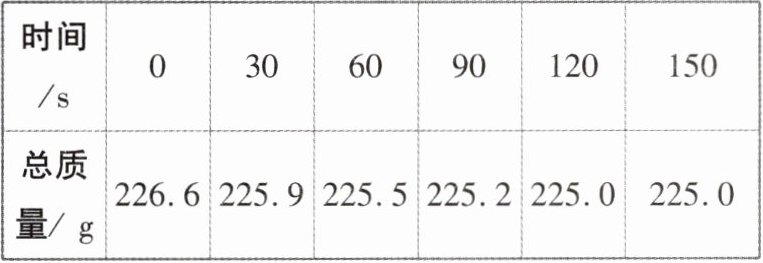
9. 日常生活情境 医疗用品 医学上常用双氧水(过氧化氢的水溶液)来清洗创口和局部抗菌,小明同学取120.0g某医用双氧水于烧杯中,向其中加入少量二氧化锰,每隔30s记录反应过程中装置(烧杯+试剂)的质量,记录结果如下表,计算120.0g该医用双氧水中过氧化氢的质量。
|时间/s|0|30|60|90|120|150|
|总质量/g|226.6|225.9|225.5|225.2|225.0|225.0|
|时间/s|0|30|60|90|120|150|
|总质量/g|226.6|225.9|225.5|225.2|225.0|225.0|

答案:
解:根据表格信息知,完全反应后产生氧气的质量为$226.6g - 225.0g = 1.6g$ 设120.0g该医用双氧水中过氧化氢的质量为x ${2H_{2}O_{2}\xlongequal{\text{MnO}_{2}}2H_{2}O + O_{2}\uparrow }$
68 32
x 1.6g
$\frac {68}{32}=\frac {x}{1.6g}$
$x=3.4g$
答:120.0g该医用双氧水中过氧化氢的质量为3.4g。
68 32
x 1.6g
$\frac {68}{32}=\frac {x}{1.6g}$
$x=3.4g$
答:120.0g该医用双氧水中过氧化氢的质量为3.4g。
10. 汽车安全气囊中叠氮化钠(NaN_3)受撞击时发生反应2NaN_3$\frac{\underline{\;撞击\;}}{}$2Na+3N_2↑,生成的氮气快速充满气囊以保护驾驶员安全,已知驾驶员的安全气囊充满需要氮气质量约为91.12g,则理论上130gNaN_3受撞击时产生的氮气能否充满驾驶员安全气囊?(写出计算过程)
答案:
解:设130g${NaN_{3}}$受撞击时产生氮气的质量为x ${2NaN_{3}\xlongequal{\text{撞击}}2Na + 3N_{2}\uparrow }$
130 84
130g x
$\frac {84}{130}=\frac {x}{130g}$
$x=84g$
$84g < 91.12g$,故130g${NaN_{3}}$受撞击时产生的氮气不能充满安全气囊
答:理论上130g${NaN_{3}}$受撞击时产生84g氮气,不能充满驾驶员安全气囊。
130 84
130g x
$\frac {84}{130}=\frac {x}{130g}$
$x=84g$
$84g < 91.12g$,故130g${NaN_{3}}$受撞击时产生的氮气不能充满安全气囊
答:理论上130g${NaN_{3}}$受撞击时产生84g氮气,不能充满驾驶员安全气囊。
11. 过氧化钠$(Na_2O_2)$是一种常见的供氧剂,常用在矿井、潜水等缺氧的场合,过氧化钠和水反应生成氧气的化学方程式为$2Na_2O_2+2H_2O= 4NaOH+O_2↑,$回答下列问题。
(1)用156g过氧化钠样品制取氧气,请计算所制取的氧气的质量是多少?
(2)(中考新考法·作坐标曲线图)向156g过氧化钠样品中逐渐加入水至过量,请在图中画出加入水的质量与产生氧气的质量曲线。
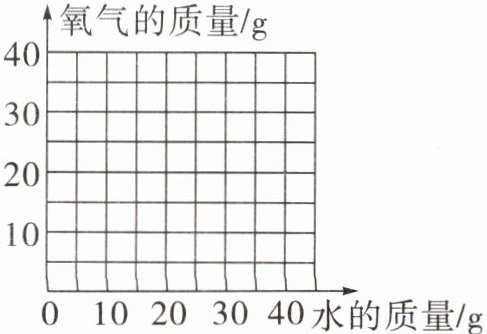
(1)用156g过氧化钠样品制取氧气,请计算所制取的氧气的质量是多少?
(2)(中考新考法·作坐标曲线图)向156g过氧化钠样品中逐渐加入水至过量,请在图中画出加入水的质量与产生氧气的质量曲线。

答案:
(1)解:设156g过氧化钠样品所制取的氧气的质量为x ${2Na_{2}O_{2} + 2H_{2}O = 4NaOH + O_{2}\uparrow }$
156 32
156g x
$\frac {32}{156}=\frac {x}{156g}$
$x=32g$
答:156g过氧化钠样品所制取的氧气的质量为32g。
(2)
【解析】
(2)由
(1)可知,156g过氧化钠样品完全反应产生氧气的质量是32g,题目中所给坐标图的横坐标为水的质量,纵坐标为氧气的质量,因此作出图示需要计算156g过氧化钠样品完全反应时需要水的质量,设156g过氧化钠样品完全反应时需要水的质量为y ${2Na_{2}O_{2} + 2H_{2}O = 4NaOH + O_{2}\uparrow }$
156 36
156g y
$\frac {36}{156}=\frac {y}{156g}$
$y=36g$
故156g过氧化钠样品完全反应需要水的质量为36g,产生氧气的质量为32g,据此作图。
(1)解:设156g过氧化钠样品所制取的氧气的质量为x ${2Na_{2}O_{2} + 2H_{2}O = 4NaOH + O_{2}\uparrow }$
156 32
156g x
$\frac {32}{156}=\frac {x}{156g}$
$x=32g$
答:156g过氧化钠样品所制取的氧气的质量为32g。
(2)

【解析】
(2)由
(1)可知,156g过氧化钠样品完全反应产生氧气的质量是32g,题目中所给坐标图的横坐标为水的质量,纵坐标为氧气的质量,因此作出图示需要计算156g过氧化钠样品完全反应时需要水的质量,设156g过氧化钠样品完全反应时需要水的质量为y ${2Na_{2}O_{2} + 2H_{2}O = 4NaOH + O_{2}\uparrow }$
156 36
156g y
$\frac {36}{156}=\frac {y}{156g}$
$y=36g$
故156g过氧化钠样品完全反应需要水的质量为36g,产生氧气的质量为32g,据此作图。
查看更多完整答案,请扫码查看


