第33页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
18. 实验Ⅰ:剪去易拉罐的盖子,在中间吊一根棉线作烛芯,将其置于盛有冷水的水槽中,向易拉罐中倒入液态石蜡并添加少量硬脂酸。充分冷却,从易拉罐中取出蜡烛。
实验Ⅱ:点燃蜡烛,火焰明亮,烛芯周围有液体产生。
实验Ⅲ:在燃着的蜡烛上方扣一个干燥的烧杯,烧杯内壁出现水雾。
关于上述实验的说法错误的是(
A.实验Ⅰ中的自制蜡烛为混合物
B.实验Ⅱ中烛芯周围产生的液体是水
C.实验Ⅱ能说明蜡烛燃烧时放出热量
D.实验Ⅲ说明蜡烛中含有氢元素
实验Ⅱ:点燃蜡烛,火焰明亮,烛芯周围有液体产生。
实验Ⅲ:在燃着的蜡烛上方扣一个干燥的烧杯,烧杯内壁出现水雾。
关于上述实验的说法错误的是(
B
)A.实验Ⅰ中的自制蜡烛为混合物
B.实验Ⅱ中烛芯周围产生的液体是水
C.实验Ⅱ能说明蜡烛燃烧时放出热量
D.实验Ⅲ说明蜡烛中含有氢元素
答案:
B 解析:根据“向易拉罐中倒入液态石蜡并添加少量硬脂酸”可知,自制蜡烛中含有多种物质,属于混合物,A正确;石蜡受热熔化,实验Ⅱ中烛芯周围产生的液体不是水,而是液体石蜡,B错误;石蜡受热熔化,实验Ⅱ点燃蜡烛,火焰明亮,烛芯周围有液体产生,说明蜡烛燃烧时放出热量,C正确;根据“在燃着的蜡烛上方扣一个干燥的烧杯,烧杯内壁出现水雾”可知,自制蜡烛燃烧生成了水,水是由氢、氧两种元素组成的,根据化学反应前后元素种类不变可知,蜡烛中含有氢元素,D正确。
19. 某同学学习了元素和物质的知识后,对其进行了梳理,其中不正确的是(
A.铁元素的质量分数由大到小:$Fe_3O_4>Fe_2O_3>FeS$
B.钙的化合物的相对分子质量由大到小:$CaCO_3>CaCl_2>Ca(OH)_2$
C.地壳中元素的含量由高到低:O>Si>Al
D.锰元素的化合价由高到低:$KMnO_4>K_2MnO_4>MnO_2$
B
)A.铁元素的质量分数由大到小:$Fe_3O_4>Fe_2O_3>FeS$
B.钙的化合物的相对分子质量由大到小:$CaCO_3>CaCl_2>Ca(OH)_2$
C.地壳中元素的含量由高到低:O>Si>Al
D.锰元素的化合价由高到低:$KMnO_4>K_2MnO_4>MnO_2$
答案:
B 解析:要比较Fe₃O₄、Fe₂O₃、FeS三种物质中铁元素的质量分数的大小,可以将这三种物质的化学式分别改写为Fe₆O₈、Fe₆O₉、Fe₆S₆,因为硫原子的相对原子质量是氧原子的2倍,所以Fe₆S₆还可以改写为Fe₆O₁₂;当三种物质中铁元素对应的原子数量相同时,氧元素对应的原子数量越少,物质中铁元素的质量分数越大,故铁元素的质量分数由大到小:Fe₃O₄>Fe₂O₃>FeS,A正确。CaCO₃的相对分子质量为100,CaCl₂的相对分子质量为111,Ca(OH)₂的相对分子质量为74,故钙的化合物的相对分子质量由大到小:CaCl₂>CaCO₃>Ca(OH)₂,B不正确。地壳中元素的含量由高到低:O>Si>Al,C正确。KMnO₄中锰元素显+7价,K₂MnO₄中锰元素显+6价,MnO₂中锰元素显+4价,故锰元素的化合价由高到低:KMnO₄>K₂MnO₄>MnO₂,D正确。
20.(2024·淮南期中)下列四个图像中,能正确反映对应关系的是(
A.图甲:加热一定量的高锰酸钾固体
B.图乙:过氧化氢溶液制取氧气
C.图丙:加热一定量的高锰酸钾
D.图丁:过氧化氢溶液在不同条件下制氧气
D
)A.图甲:加热一定量的高锰酸钾固体
B.图乙:过氧化氢溶液制取氧气
C.图丙:加热一定量的高锰酸钾
D.图丁:过氧化氢溶液在不同条件下制氧气
答案:
D 解析:高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰和氧气,加热到一定温度时高锰酸钾才能分解,随着反应的进行,二氧化锰的质量分数从0开始逐渐增大,完全反应后不再发生改变,A错误。过氧化氢在二氧化锰的催化作用下分解生成水和氧气,随着反应的进行,氧气逸出,试管中氧原子的个数逐渐减少,至完全反应不再发生改变,由于水分子中也含有氧原子,所以最终试管中仍含有氧原子,不会减少至0,B错误。加热高锰酸钾时,随着反应的进行,剩余固体的质量不断减小,当反应完全后,质量不再减小,因为生成物有锰酸钾和二氧化锰固体,所以剩余固体的质量不会减小到0,C错误。催化剂只能改变反应速率,不影响产生氧气的质量,有催化剂的反应速率大,至完全反应所需时间短,D正确。
21.(6分)(2025·苏州期中)如图,小徐用手掌总结氧气的化学性质,手指上的物质能与掌心的氧气反应。
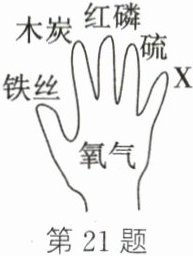
(1)铁丝在氧气中燃烧,铁丝盘成螺旋状的原因是
(2)木炭在氧气中燃烧,为了检验所产生的气体,可向集气瓶中倒入
(3)从微观的角度分析,红磷燃烧前后不发生改变的粒子是
(4)硫燃烧时需要在集气瓶底留有少量水的原因是
(5)若物质X是氢气,在氧气中燃烧产生

(1)铁丝在氧气中燃烧,铁丝盘成螺旋状的原因是
增大铁丝的受热面积,有利于铁丝持续燃烧
。(2)木炭在氧气中燃烧,为了检验所产生的气体,可向集气瓶中倒入
澄清石灰水
。(3)从微观的角度分析,红磷燃烧前后不发生改变的粒子是
磷原子和氧原子
。(4)硫燃烧时需要在集气瓶底留有少量水的原因是
吸收二氧化硫,防止其污染空气
。(5)若物质X是氢气,在氧气中燃烧产生
淡蓝
色火焰,在火焰上方罩一个干燥的烧杯,烧杯内壁有水雾,写出这个反应的文字表达式:氢气+氧气$\xrightarrow{点燃}$水
。
答案:
(1)增大铁丝的受热面积,有利于铁丝持续燃烧 (2)澄清石灰水 (3)磷原子和氧原子 (4)吸收二氧化硫,防止其污染空气 (5)淡蓝 氢气+氧气$\xrightarrow{点燃}$水
22.(8分)新情境 社会热点 氢气的制取与储存是氢能源利用领域的研究热点。
Ⅰ. 制取氢气。
(1)高温下C与水蒸气能产生$H_2。$反应后的气体中含有$H_2、$CO、$CO_2$及水蒸气,向其中加入一定量的干燥剂可提高$H_2$在混合气体中的百分含量,原因是
(2)利用太阳能电厂富余电力电解水制氢,电极上微观粒子的变化情况如图所示。B电极表面生成$H_2$的过程可描述为

Ⅱ. 储存氢气。
(3)碳纳米管与活性炭均具有疏松多孔的结构,研究表明碳纳米管吸附储氢的能力是活性炭的10倍。碳纳米管吸附储氢属于
$(4)Mg_2Cu$是一种储氢合金。350℃时$,Mg_2Cu$与$H_2$反应生成MgHₙ,MgHₙ中Mg与H的质量比为12∶1,则n=
Ⅰ. 制取氢气。
(1)高温下C与水蒸气能产生$H_2。$反应后的气体中含有$H_2、$CO、$CO_2$及水蒸气,向其中加入一定量的干燥剂可提高$H_2$在混合气体中的百分含量,原因是
干燥剂吸收掉水蒸气,使得混合气体的总体积减小
。(2)利用太阳能电厂富余电力电解水制氢,电极上微观粒子的变化情况如图所示。B电极表面生成$H_2$的过程可描述为
每个氢离子在B电极表面得到1个电子变成氢原子,2个氢原子结合成1个氢分子,许多氢分子聚集成氢气
。
Ⅱ. 储存氢气。
(3)碳纳米管与活性炭均具有疏松多孔的结构,研究表明碳纳米管吸附储氢的能力是活性炭的10倍。碳纳米管吸附储氢属于
物理
变化。$(4)Mg_2Cu$是一种储氢合金。350℃时$,Mg_2Cu$与$H_2$反应生成MgHₙ,MgHₙ中Mg与H的质量比为12∶1,则n=
2
。
答案:
(1)干燥剂吸收掉水蒸气,使得混合气体的总体积减小 (2)每个氢离子在B电极表面得到1个电子变成氢原子,2个氢原子结合成1个氢分子,许多氢分子聚集成氢气 (3)物理 (4)2 解析:
(4)在MgHₙ中,镁(Mg)与氢(H)的质量比为12:1,MgHₙ中镁与氢的质量比可以表示为24:n,则24:n=12:1,n=2。
(4)在MgHₙ中,镁(Mg)与氢(H)的质量比为12:1,MgHₙ中镁与氢的质量比可以表示为24:n,则24:n=12:1,n=2。
查看更多完整答案,请扫码查看


