第45页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
15.(2024·乌海海勃湾模拟)用氯酸钾和二氧化锰的混合物制取氧气,混合物的质量变化情况如图所示。下列说法中正确的是 (
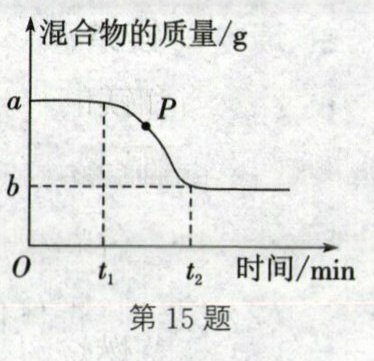
A.反应结束时能生成$(a-b)\ g$氧气
B.P点处混合物的成分是氯酸钾和氯化钾
C.$t_{1}~t_{2}\ min$内,混合物中氯化钾的质量分数不断减小
D.$0~t_{1}\ min$内,$\mathrm{MnO}_{2}$在混合物中的质量分数不断增大
A
)
A.反应结束时能生成$(a-b)\ g$氧气
B.P点处混合物的成分是氯酸钾和氯化钾
C.$t_{1}~t_{2}\ min$内,混合物中氯化钾的质量分数不断减小
D.$0~t_{1}\ min$内,$\mathrm{MnO}_{2}$在混合物中的质量分数不断增大
答案:
A 解析:氯酸钾在二氧化锰的催化作用下受热分解生成氯化钾和氧气,所以反应中混合物减少的质量就是反应生成的氧气质量,故反应结束时能生成(a-b)g氧气,A正确;P点表示氯酸钾部分分解,此时混合物中含有未分解的氯酸钾和生成的氯化钾,还有作为催化剂的二氧化锰,B不正确;在反应过程中,混合物质量逐渐减少,而生成的氯化钾的质量逐渐增加,因此t₁~t₂min内,混合物中氯化钾的质量分数逐渐增大,C不正确;在该反应中二氧化锰是反应的催化剂,质量不变,0~t₁min内,混合物未减少,因此MnO₂在混合物中的质量分数没有改变,D不正确。
16.(2024·安徽模拟改编)用图甲装置探究物质燃烧。点燃蜡烛后立即伸入集气瓶中并塞紧橡皮塞,待蜡烛熄灭后,在$t_{1}$时刻,将滴管中的水全部滴入集气瓶中,铝盒中的白磷燃烧。图乙是集气瓶内$\mathrm{O}_{2}$浓度随时间变化的图像。已知:生石灰与水反应放热。下列说法不正确的是 (
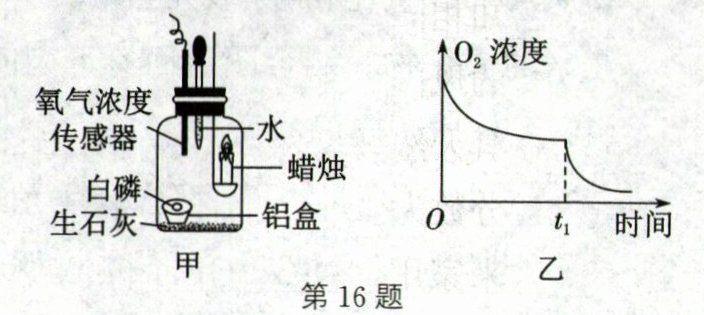
A.$0~t_{1}$时刻内,$\mathrm{O}_{2}$浓度下降与蜡烛燃烧有关
B.生石灰的作用是与水反应放热,引燃白磷
C.该实验证明白磷和蜡烛燃烧需要的最低$\mathrm{O}_{2}$浓度相同
D.白磷燃烧会产生白烟
C
)
A.$0~t_{1}$时刻内,$\mathrm{O}_{2}$浓度下降与蜡烛燃烧有关
B.生石灰的作用是与水反应放热,引燃白磷
C.该实验证明白磷和蜡烛燃烧需要的最低$\mathrm{O}_{2}$浓度相同
D.白磷燃烧会产生白烟
答案:
C 解析:根据题给信息可知,0~t₁时刻内,集气瓶内只有蜡烛在燃烧,故O₂浓度下降与蜡烛燃烧有关,A正确;滴管中的水滴入集气瓶,生石灰与水反应生成氢氧化钙,并放出大量的热,引燃白磷,B正确;通过图乙中氧气浓度的变化可知,白磷燃烧需要的最低O₂浓度比蜡烛燃烧需要的最低O₂浓度低,C错误;白磷燃烧会产生白烟,D正确。
17.(2024·镇江句容期中)已知:$2\mathrm{NaHCO}_{3}\xlongequal{\triangle}\mathrm{Na}_{2}\mathrm{CO}_{3}+\mathrm{CO}_{2}\uparrow+\mathrm{H}_{2}\mathrm{O}$,将8.4 g $\mathrm{NaHCO}_{3}$固体加热到质量不再改变。下列说法正确的是 (
A.固体加热时共生成4.4 g $\mathrm{CO}_{2}$
B.热稳定性:$\mathrm{NaHCO}_{3}>\mathrm{Na}_{2}\mathrm{CO}_{3}$
C.固体加热时共生成0.9 g $\mathrm{H}_{2}\mathrm{O}$
D.加热后,固体中钠元素的质量分数减小
C
)A.固体加热时共生成4.4 g $\mathrm{CO}_{2}$
B.热稳定性:$\mathrm{NaHCO}_{3}>\mathrm{Na}_{2}\mathrm{CO}_{3}$
C.固体加热时共生成0.9 g $\mathrm{H}_{2}\mathrm{O}$
D.加热后,固体中钠元素的质量分数减小
答案:
C 解析:碳酸氢钠在加热条件下分解生成碳酸钠、水和二氧化碳,将8.4gNaHCO₃固体加热到质量不再改变,最终得到的固体为碳酸钠。设反应生成二氧化碳的质量为x,水的质量为y。2NaHCO₃$\xlongequal{\triangle }$Na₂CO₃+CO₂↑+H₂O168 44 188.4g x y$\frac{168}{44}=\frac{8.4\mathrm{g}}{x}$ x=2.2g$\frac{168}{18}=\frac{8.4\mathrm{g}}{y}$ y=0.9g即固体加热时共生成2.2g二氧化碳,A错误。碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,故碳酸钠的热稳定性强于碳酸氢钠,B错误。由上述分析可知,固体加热时共生成0.9gH₂O,C正确。根据质量守恒定律,化学反应前后物质的总质量不变,反应后有气体生成,则反应后固体的质量减小,固体中钠元素的质量分数增大,D错误。
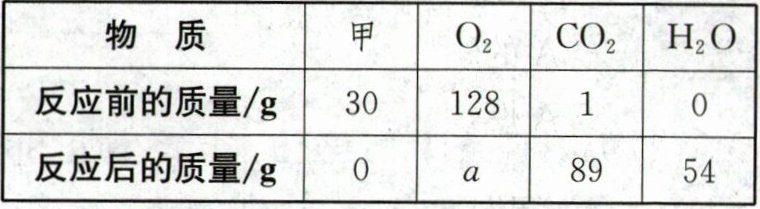
18.(2024·天津红桥模拟)一个密闭容器内有甲、氧气、二氧化碳三种物质,在一定条件下充分反应,反应前后各物质的质量如表所示。下列说法不正确的是 (
|物质|甲|$\mathrm{O}_{2}$|$\mathrm{CO}_{2}$|$\mathrm{H}_{2}\mathrm{O}$|
|反应前的质量/g|30|128|1|0|
|反应后的质量/g|0|a|89|54|
A.甲不充分燃烧会产生有毒的气体
B.甲中一定含氧元素
C.充分反应后剩余氧气的质量是16 g
D.生成$\mathrm{CO}_{2}和\mathrm{H}_{2}\mathrm{O}$的质量比是88∶54
B
)|物质|甲|$\mathrm{O}_{2}$|$\mathrm{CO}_{2}$|$\mathrm{H}_{2}\mathrm{O}$|
|反应前的质量/g|30|128|1|0|
|反应后的质量/g|0|a|89|54|

A.甲不充分燃烧会产生有毒的气体
B.甲中一定含氧元素
C.充分反应后剩余氧气的质量是16 g
D.生成$\mathrm{CO}_{2}和\mathrm{H}_{2}\mathrm{O}$的质量比是88∶54
答案:
B 解析:由题意可知,甲中一定含有碳元素,甲不充分燃烧会产生有毒的一氧化碳气体,A选项正确。a=30+128+1-54-89=16,甲中氧元素的质量为(89g-1g)×$(\frac{32}{44}× 100\%)$+54g×$(\frac{16}{18}× 100\%)$+16g-128g=0,说明甲中不含有氧元素,B选项不正确。充分反应后剩余氧气的质量是16g,C选项正确。生成CO₂和H₂O的质量比为(89g-1g):54g=88:54,D选项正确。
19.(2025·泰州海陵期末)一种提纯白磷($\mathrm{P}_{4}$)样品的工艺流程如图(杂质不参与反应)。下列说法错误的是 (
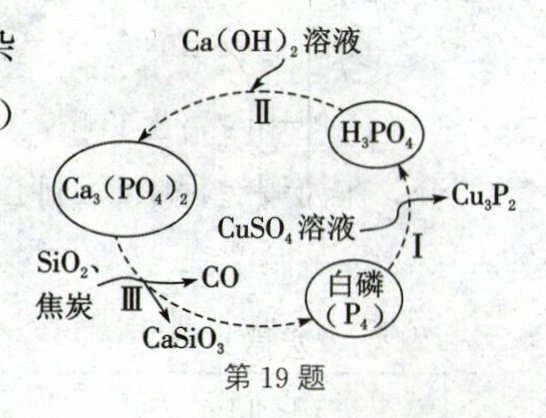
A.过程Ⅰ中,P元素的化合价既升高又降低
B.过程Ⅱ中,发生的反应不属于化合反应
C.过程Ⅲ中,需要进行尾气处理
D.过程Ⅰ中,理论上每生成98 kg的$\mathrm{H}_{3}\mathrm{PO}_{4}$需要消耗31 kg的$\mathrm{P}_{4}$
D
)
A.过程Ⅰ中,P元素的化合价既升高又降低
B.过程Ⅱ中,发生的反应不属于化合反应
C.过程Ⅲ中,需要进行尾气处理
D.过程Ⅰ中,理论上每生成98 kg的$\mathrm{H}_{3}\mathrm{PO}_{4}$需要消耗31 kg的$\mathrm{P}_{4}$
答案:
D 解析:单质中元素的化合价为0,H₃PO₄中P元素的化合价为+5,Cu₃P中P元素的化合价为-3,过程Ⅰ中,P元素的化合价由0变为+5、-3,既升高又降低,A正确;过程Ⅱ为磷酸与氢氧化钙反应,除Ca₃(PO₄)₂外,还有H₂O生成,不符合“多变一”的形式,不属于化合反应,B正确;过程Ⅲ中,有一氧化碳产生,直接排放会污染空气,故需要进行尾气处理,C正确;过程Ⅰ中,每生成98kg的H₃PO₄中含有磷元素的质量为98kg×$(\frac{31}{98}× 100\%)$=31kg,由于过程Ⅰ中还有磷化铜生成,根据质量守恒定律可知,需要消耗的P₄的质量大于31kg,D错误。
20.(2024·常州期末)取10.8 g过氧化钙晶体,对其进行热分解实验,并绘制固体质量与温度的关系如图所示。过氧化钙晶体受热时先失去结晶水:$\mathrm{CaO}_{2}\cdot x\mathrm{H}_{2}\mathrm{O}\xlongequal{\triangle}\mathrm{CaO}_{2}+x\mathrm{H}_{2}\mathrm{O}$,加热时固体中钙元素质量保持不变。下列说法正确的是 (
A.x= 6
B.a点对应的物质属于混合物
C.生成水的质量为8.0 g
D.b点对应固体的化学式为$\mathrm{CaO}$
D
)A.x= 6
B.a点对应的物质属于混合物
C.生成水的质量为8.0 g
D.b点对应固体的化学式为$\mathrm{CaO}$
答案:
D 解析:由图像可知,10.8gCaO₂·xH₂O中结晶水的质量为10.8g-3.6g=7.2g,分解生成的CaO₂的质量为3.6g。则CaO₂·xH₂O$\xlongequal{\triangle }$CaO₂+xH₂O72 18x3.6g 7.2g$\frac{72}{18x}=\frac{3.6\mathrm{g}}{7.2\mathrm{g}}$ x=8A错误。CaO₂·xH₂O加热可分解,而0~150℃时固体质量不发生改变,其原因是没有达到它的分解温度,因此a点对应的物质仍为纯净物,B错误。10.8gCaO₂·xH₂O中结晶水的质量为7.2g,即生成水的质量也为7.2g,C错误。由图像可知,150~350℃时发生反应的化学方程式为CaO₂·8H₂O$\xlongequal{\triangle }$CaO₂+8H₂O,超过350℃时CaO₂可继续分解,过氧化钙受热分解后剩余固体的质量为2.8g,则固体减少的质量为3.6g-2.8g=0.8g,假设过氧化钙分解生成氧化钙和氧气,则反应的化学方程式为2CaO₂$\xlongequal{\triangle }$2CaO+O₂↑,此时生成的氧化钙与氧气的质量比为(56×2):32=7:2,题中剩余固体质量与固体减少的质量比为2.8g:0.8g=7:2,符合上述假设,所以350℃以后发生反应的化学方程式为2CaO₂$\xlongequal{\triangle }$2CaO+O₂↑,因此b点对应固体的化学式为CaO,D正确。
查看更多完整答案,请扫码查看


