第93页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
20. 现有Mg和MgO的固体混合物3 g,经测定镁元素的质量分数为80%,向固体混合物中加入100 g一定溶质质量分数的稀硫酸,恰好完全反应。下列说法不正确的是(
A.反应后溶液中的溶质只有$MgSO_4$
B.反应过程中有气泡产生
C.所用稀硫酸中溶质的质量分数为19.6%
D.生成$MgSO_4$的质量为12 g
C
)A.反应后溶液中的溶质只有$MgSO_4$
B.反应过程中有气泡产生
C.所用稀硫酸中溶质的质量分数为19.6%
D.生成$MgSO_4$的质量为12 g
答案:
C 解析:镁与硫酸反应生成硫酸镁和氢气,氧化镁与硫酸反应生成硫酸镁和水,所以Mg和MgO的固体混合物与稀硫酸恰好完全反应后溶液中的溶质只有硫酸镁,A正确。由于MgO中镁元素的质量分数为$\frac{24}{40}×100\% =60\%$,所以固体混合物中含有镁,镁与稀硫酸反应会有氢气产生,故反应过程中有气泡产生,B正确。现有Mg和MgO的固体混合物3g,经测定镁元素的质量分数为80%,则镁元素的质量为3g×80%=2.4g,反应后镁元素全部转化为MgSO₄,所以反应后生成MgSO₄的质量为$\frac{2.4\,g}{\frac{24}{24+32+16×4}×100\%}=12\,g$;根据发生反应的化学方程式可知硫酸与硫酸镁的关系式为H₂SO₄~MgSO₄,设所用稀硫酸中溶质的质量分数为x。
H₂SO₄~MgSO₄
98 120
100g×x 12g
$\frac{98}{120}=\frac{100\,g× x}{12\,g}$ $x=9.8\%$
C错误、D正确。
H₂SO₄~MgSO₄
98 120
100g×x 12g
$\frac{98}{120}=\frac{100\,g× x}{12\,g}$ $x=9.8\%$
C错误、D正确。
21. (5分)小明同学测定下列生活中物质的pH,结果如表所示:
|物质|石灰水|雨水|葡萄糖水|柠檬汁|食盐水|纯碱水|洁厕净|
|pH|9.2|5.2|7.0|2.5|7.0|12.2|1.1|

(1)由表判断:酸性最强的物质是______
(2)厕所中的污垢主要有碳酸钙、铁锈等,洁厕净的主要成分是盐酸和表面活性剂。洁厕净除去污垢中的碳酸钙的化学方程式为______
(3)石灰水敞口久置于空气中,溶液的pH会______
|物质|石灰水|雨水|葡萄糖水|柠檬汁|食盐水|纯碱水|洁厕净|
|pH|9.2|5.2|7.0|2.5|7.0|12.2|1.1|

(1)由表判断:酸性最强的物质是______
洁厕净
,能使无色酚酞溶液变红的物质是______石灰水(或纯碱水)
(写一个)。(2)厕所中的污垢主要有碳酸钙、铁锈等,洁厕净的主要成分是盐酸和表面活性剂。洁厕净除去污垢中的碳酸钙的化学方程式为______
CaCO₃+2HCl=CaCl₂+H₂O+CO₂↑
。(3)石灰水敞口久置于空气中,溶液的pH会______
减小
,溶液质量会______减小
。(填"增大"或"减小")
答案:
(1)洁厕净 石灰水(或纯碱水)(2)CaCO₃+2HCl=CaCl₂+H₂O+CO₂↑(3)减小 减小
22. (4分)(2024·泉州模拟)阅读短文并回答问题。
我国航天事业已进入创新发展快车道。空间站中去除二氧化碳的方法,有如下三种。
方法一:利用二氧化碳无法通过分子筛而吸附。低压释放出二氧化碳,直接排放到太空。
方法二:氢氧化锂(LiOH)与二氧化碳反应生成碳酸锂和水,从而除去二氧化碳。
方法三:利用电解水产生的氢气在催化剂条件下与二氧化碳反应生成水和甲烷$(CH_4)。$
(1)由方法一可知,二氧化碳分子比分子筛孔隙
(2)如图是两种不同吸收剂吸收$CO_2$的最大质量的关系图。
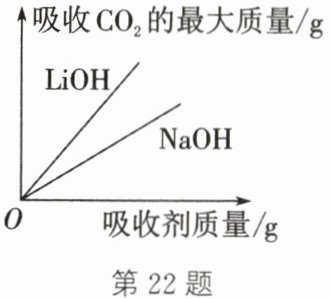
① NaOH吸收$CO_2$时反应的化学方程式为
② 结合数据信息,空间站中选用LiOH作为吸收剂的理由是
(3)相较于方法二,方法三的优点是
我国航天事业已进入创新发展快车道。空间站中去除二氧化碳的方法,有如下三种。
方法一:利用二氧化碳无法通过分子筛而吸附。低压释放出二氧化碳,直接排放到太空。
方法二:氢氧化锂(LiOH)与二氧化碳反应生成碳酸锂和水,从而除去二氧化碳。
方法三:利用电解水产生的氢气在催化剂条件下与二氧化碳反应生成水和甲烷$(CH_4)。$
(1)由方法一可知,二氧化碳分子比分子筛孔隙
大
(填"大"或"小")。(2)如图是两种不同吸收剂吸收$CO_2$的最大质量的关系图。

① NaOH吸收$CO_2$时反应的化学方程式为
CO₂+2NaOH=Na₂CO₃+H₂O
。② 结合数据信息,空间站中选用LiOH作为吸收剂的理由是
吸收剂质量相同时,氢氧化锂吸收CO₂效果更好
。(3)相较于方法二,方法三的优点是
实现物质循环利用(合理答案均可)
(写一点即可)。
答案:
(1)大(2)①CO₂+2NaOH=Na₂CO₃+H₂O ②吸收剂质量相同时,氢氧化锂吸收CO₂效果更好(3)实现物质循环利用(合理答案均可)
23. (6分)海洋中有丰富的水生生物和化学资源。海水晒盐能得到粗盐和苦卤,粗盐中含有多种可溶性杂质(硫酸钠、氯化镁、氯化钙等)和不溶性杂质(泥沙等)。现以粗盐为原料制取精盐,生产过程如图。
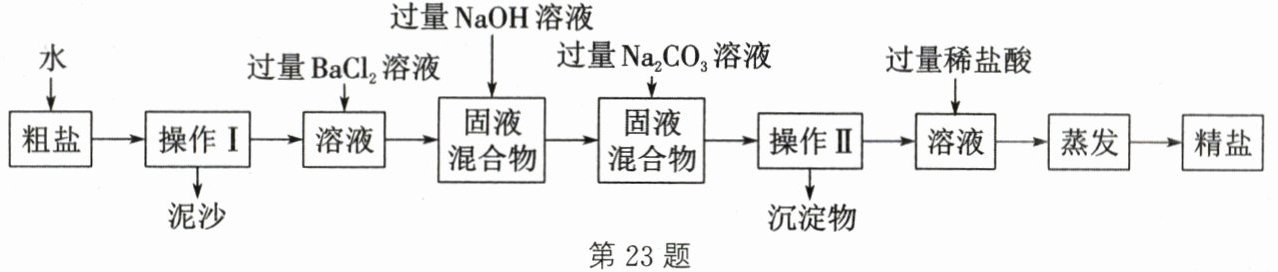
(1)操作Ⅰ和操作Ⅱ的名称是
(2)加入$BaCl_2$溶液后发生反应的化学方程式为
(3)向操作Ⅱ后所得溶液中加入过量稀盐酸,其目的是

(1)操作Ⅰ和操作Ⅱ的名称是
过滤
。(2)加入$BaCl_2$溶液后发生反应的化学方程式为
BaCl₂+Na₂SO₄=BaSO₄↓+2NaCl
。(3)向操作Ⅱ后所得溶液中加入过量稀盐酸,其目的是
除去过量的碳酸钠和氢氧化钠
,最后通过蒸发结晶得到较为纯净的氯化钠。
答案:
(1)过滤(2)BaCl₂+Na₂SO₄=BaSO₄↓+2NaCl(3)除去过量的碳酸钠和氢氧化钠 解析:(1)操作Ⅰ和操作Ⅱ均是将固体与液体分离,均为过滤操作。(2)加入BaCl₂溶液后,硫酸钠和氯化钡溶液反应生成硫酸钡沉淀和氯化钠,反应的化学方程式为BaCl₂+Na₂SO₄=BaSO₄↓+2NaCl。(3)操作Ⅱ后所得溶液中含有过量的碳酸钠和氢氧化钠,向操作Ⅱ后所得溶液中加入过量稀盐酸,其目的是除去过量的碳酸钠和氢氧化钠,以便得到纯净的氯化钠。
查看更多完整答案,请扫码查看


