第46页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
21.(4分)新情境 传统文化 国画历史悠久、风格多样,是我国的文化艺术瑰宝。
(1)国画蓝色源于石青[$\mathrm{Cu}_{3}(\mathrm{OH})_{2}(\mathrm{CO}_{3})_{2}$]。石青中铜元素呈
(2)银朱是古代作画的红色颜料。《天工开物》记载了颜料制取:“水银(汞)一斤入石亭脂(天然硫)二斤,同研不见星,……其贴口者朱($\mathrm{HgS}$)更鲜华。”写出制取银朱的化学方程式:
(1)国画蓝色源于石青[$\mathrm{Cu}_{3}(\mathrm{OH})_{2}(\mathrm{CO}_{3})_{2}$]。石青中铜元素呈
+2
价,$\mathrm{Cu}_{3}(\mathrm{OH})_{2}(\mathrm{CO}_{3})_{2}$受热分解会生成三种氧化物,写出反应的化学方程式:$\mathrm{Cu}_{3}(\mathrm{OH})_{2}(\mathrm{CO}_{3})_{2}\xlongequal{\triangle }3\mathrm{CuO}+\mathrm{H}_{2}\mathrm{O}+2\mathrm{CO}_{2}\uparrow$
。(2)银朱是古代作画的红色颜料。《天工开物》记载了颜料制取:“水银(汞)一斤入石亭脂(天然硫)二斤,同研不见星,……其贴口者朱($\mathrm{HgS}$)更鲜华。”写出制取银朱的化学方程式:
$\mathrm{Hg}+\mathrm{S}\xlongequal{\;\;}\mathrm{HgS}$
;在该反应中,化合价降低的元素是$\mathrm{S}$
(填元素符号)。
答案:
(1)+2 Cu₂(OH)₂(CO₃)₂$\xlongequal{\triangle }$H₂O+3CuO+2CO₂↑ (2)Hg+S$\xlongequal{\;\;}$HgS S
22.(5分)价类二维图表示物质中某种元素的化合价与物质类别之间的关系,如图所示的B、C、D三种物质均属于氧化物,除氧元素外另一种元素的化合价分别为+1、+2、+3,如B物质表示某+1价元素的氧化物。结合图示回答下列问题。

(1)A物质所属的物质类别是______
(2)若A、C两种物质中都含有镁元素,则A生成C的化学方程式为______
(3)若D为氧化铁,其化学式是______

(1)A物质所属的物质类别是______
单质
。(2)若A、C两种物质中都含有镁元素,则A生成C的化学方程式为______
2Mg+O₂$\xlongequal{点燃}$2MgO
,最能说明该变化属于化学变化的现象是______有白色固体生成
。(3)若D为氧化铁,其化学式是______
Fe₂O₃
。已知铁有多种氧化物,请写出铁在氧气中燃烧的化学方程式:______3Fe+2O₂$\xlongequal{点燃}$Fe₃O₄
。
答案:
(1)单质 (2)2Mg+O₂$\xlongequal{点燃}$2MgO 有白色固体生成 (3)Fe₂O₃ 3Fe+2O₂$\xlongequal{点燃}$Fe₃O₄
23.(6分)(2025·西安莲湖期末)古代“打火机”——火折子是将少量硫黄、土纸和棉花等混合物点燃后置于竹筒中,使火种不熄灭(仅剩火星)。使用时拔下竹帽,对着竹筒吹气,即刻出现火苗。回答下列问题:
(1)硫黄在氧气中燃烧产生

(2)从燃烧条件角度分析,土纸、棉花和硫黄是
(3)竹筒内火星不熄灭,仍在微弱燃烧,吹气使火种重新燃烧起来,说明影响燃烧现象的因素之一是
(4)不使用时盖上竹帽,火种“熄灭”,其灭火原理是
(5)在使用过程中闻到刺激性气味的原因是
(1)硫黄在氧气中燃烧产生
明亮的蓝紫
色火焰,放出热量,其反应的化学方程式为S+O₂$\xlongequal{点燃}$SO₂
。
(2)从燃烧条件角度分析,土纸、棉花和硫黄是
可燃物
。(3)竹筒内火星不熄灭,仍在微弱燃烧,吹气使火种重新燃烧起来,说明影响燃烧现象的因素之一是
氧气的浓度
。(4)不使用时盖上竹帽,火种“熄灭”,其灭火原理是
隔绝氧气
。(5)在使用过程中闻到刺激性气味的原因是
分子是在不断运动的
。
答案:
(1)明亮的蓝紫 S+O₂$\xlongequal{点燃}$SO₂ (2)可燃物 (3)氧气的浓度 (4)隔绝氧气 (5)分子是在不断运动的
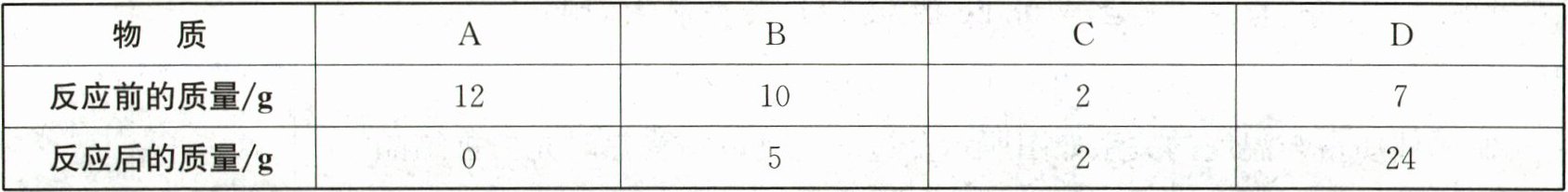
24.(4分)某同学在一次化学实验中,分别记录反应前后试管中A、B、C、D四种物质的质量,结果如表所示。回答下列问题:
|物质|A|B|C|D|
|反应前的质量/g|12|10|2|7|
|反应后的质量/g|0|5|2|24|
(1)该反应中,可能是催化剂的物质是______
(2)若A、B、C、D都为固体,则反应后试管中的剩余物质属于______
|物质|A|B|C|D|
|反应前的质量/g|12|10|2|7|
|反应后的质量/g|0|5|2|24|

(1)该反应中,可能是催化剂的物质是______
C
(填字母)。(2)若A、B、C、D都为固体,则反应后试管中的剩余物质属于______
混合物
(填“纯净物”或“混合物”)。
答案:
(1)C (2)混合物
25.(5分)质量守恒定律的发现,使得化学科学由定性研究走向定量研究,促进了化学科学的发展。
(1)a g铝与b g氧气充分反应,得到c g氧化铝,则a+b
(2)一定质量的镁条在氧气中完全燃烧后,生成的固体质量
(3)现有化学反应$\mathrm{A}+3\mathrm{B}\xlongequal{\;\;}\mathrm{C}+2\mathrm{D}$,已知A为d g,B为e g,恰好完全反应后生成D为f g,则生成C的质量为
(4)4.6 g某化合物在空气中完全燃烧,得到8.8 g二氧化碳和5.4 g水,则该化合物的组成元素是
(1)a g铝与b g氧气充分反应,得到c g氧化铝,则a+b
≥
c。(2)一定质量的镁条在氧气中完全燃烧后,生成的固体质量
大于
(填“大于”“小于”或“等于”)镁条的质量,这与质量守恒定律不矛盾
(填“矛盾”或“不矛盾”)。(3)现有化学反应$\mathrm{A}+3\mathrm{B}\xlongequal{\;\;}\mathrm{C}+2\mathrm{D}$,已知A为d g,B为e g,恰好完全反应后生成D为f g,则生成C的质量为
(d+e-f)g
。(4)4.6 g某化合物在空气中完全燃烧,得到8.8 g二氧化碳和5.4 g水,则该化合物的组成元素是
碳、氧和氢
(填元素名称)。
答案:
(1)≥ (2)大于 不矛盾 (3)(d+e-f)g (4)碳、氧和氢 解析:
(1)根据质量守恒定律,a g铝与b g氧气充分反应,得到c g氧化铝,铝与氧气有可能恰好完全反应,此时a+b=c;若物质有剩余,则a+b>c。综上所述,a+b≥c。(2)一定质量的镁条在氧气中完全燃烧生成氧化镁,氧化镁的质量是镁元素的质量和氧元素的质量和,故生成的固体质量大于镁条的质量,氧气的质量和镁的质量和等于生成的氧化镁的质量,这与质量守恒定律不矛盾。(3)化学反应A+3B$\xlongequal{\;\;}$C+2D,已知A为d g,B为e g,由质量守恒定律可知,反应前各物质的质量总和等于反应后生成各物质的质量总和,恰好完全反应后生成D为f g,则生成C的质量为(d+e-f)g。(4)4.6g某化合物在空气中完全燃烧,生成8.8g二氧化碳和5.4g水,则该化合物中一定含有碳元素、氢元素,8.8g二氧化碳中碳元素的质量为8.8g×$(\frac{12}{12+16× 2}× 100\%)$=2.4g,5.4g水中氢元素的质量为5.4g×$(\frac{1× 2}{1× 2+16}× 100\%)$=0.6g,2.4g+0.6g=3.0g<4.6g,则该化合物中存在氧元素。
(1)根据质量守恒定律,a g铝与b g氧气充分反应,得到c g氧化铝,铝与氧气有可能恰好完全反应,此时a+b=c;若物质有剩余,则a+b>c。综上所述,a+b≥c。(2)一定质量的镁条在氧气中完全燃烧生成氧化镁,氧化镁的质量是镁元素的质量和氧元素的质量和,故生成的固体质量大于镁条的质量,氧气的质量和镁的质量和等于生成的氧化镁的质量,这与质量守恒定律不矛盾。(3)化学反应A+3B$\xlongequal{\;\;}$C+2D,已知A为d g,B为e g,由质量守恒定律可知,反应前各物质的质量总和等于反应后生成各物质的质量总和,恰好完全反应后生成D为f g,则生成C的质量为(d+e-f)g。(4)4.6g某化合物在空气中完全燃烧,生成8.8g二氧化碳和5.4g水,则该化合物中一定含有碳元素、氢元素,8.8g二氧化碳中碳元素的质量为8.8g×$(\frac{12}{12+16× 2}× 100\%)$=2.4g,5.4g水中氢元素的质量为5.4g×$(\frac{1× 2}{1× 2+16}× 100\%)$=0.6g,2.4g+0.6g=3.0g<4.6g,则该化合物中存在氧元素。
查看更多完整答案,请扫码查看


