第88页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
24. (6分)归纳是学习的重要方法,小芳在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图甲所示,连线表示相互间能反应);小明为表示反应实质绘制了图乙、图丙。请根据图示和要求回答问题:
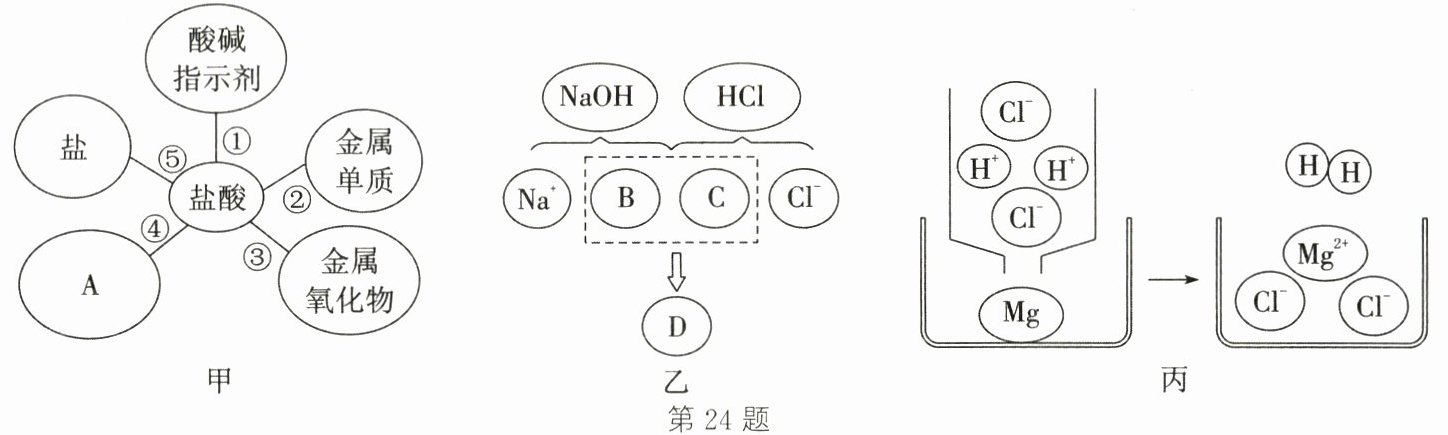
(1)为了验证图甲中的性质①,小红将紫色石蕊溶液滴入盐酸中,溶液变成
(2)图甲中A所表示的物质类别是
(3)图甲中盐酸的性质③决定了盐酸可以用来清除铁锈(主要成分为$Fe_2O_3),$该反应的化学方程式为
(4)选用合适的物质验证图甲中的性质⑤,其反应的化学方程式为
(5)图乙描述了氢氧化钠溶液与盐酸反应的微观实质,图中B、C、D处应填入的化学式或离子符号依次为
(6)图丙是镁与盐酸反应过程的微观示意图,从微观角度看,该反应中有效相互作用的微观粒子是

(1)为了验证图甲中的性质①,小红将紫色石蕊溶液滴入盐酸中,溶液变成
红
色。(2)图甲中A所表示的物质类别是
碱
。(3)图甲中盐酸的性质③决定了盐酸可以用来清除铁锈(主要成分为$Fe_2O_3),$该反应的化学方程式为
${Fe_{2}O_{3} + 6HCl\xlongequal{}2FeCl_{3} + 3H_{2}O}$
。(4)选用合适的物质验证图甲中的性质⑤,其反应的化学方程式为
${CaCO_{3} + 2HCl\xlongequal{}CaCl_{2} + H_{2}O + CO_{2}\uparrow}$
。(5)图乙描述了氢氧化钠溶液与盐酸反应的微观实质,图中B、C、D处应填入的化学式或离子符号依次为
${OH^{-}}$、${H^{+}}$、${H_{2}O}$
。(6)图丙是镁与盐酸反应过程的微观示意图,从微观角度看,该反应中有效相互作用的微观粒子是
${H^{+}}$、${Mg}$
。
答案:
(1)红 (2)碱 (3)${Fe_{2}O_{3} + 6HCl\xlongequal{}2FeCl_{3} + 3H_{2}O}$ (4)${CaCO_{3} + 2HCl\xlongequal{}CaCl_{2} + H_{2}O + CO_{2}\uparrow}$(合理答案均可) (5)${OH^{-}}$、${H^{+}}$、${H_{2}O}$ (6)${H^{+}}$、${Mg}$
25. (6分)在探究铁、铜、锌、银的金属活动性顺序时,小组同学设计了如图实验(A、B、C所用金属的大小、形状和稀盐酸的用量及浓度均相同)。
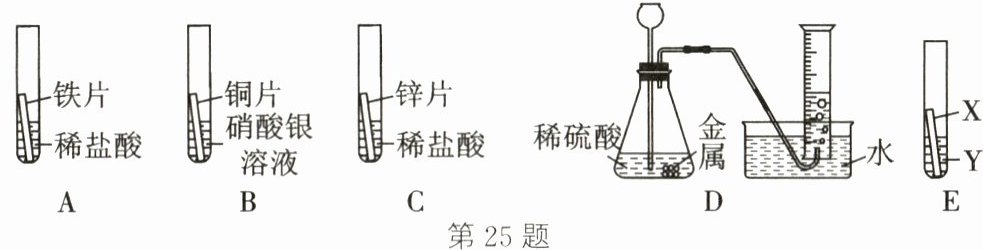
(1)一段时间后,可明显观察到实验B中铜片表面的现象是
(2)甲同学通过对比实验
(3)乙同学拟定用定量的方法测定金属与酸反应的速率,于是设计出实验D,该实验通过测定
(4)丙同学认为实验A~C不足以得出4种金属的活动性顺序,需要在上述实验基础上,补充实验E(X与Y能发生反应),写出E中发生反应的化学方程式:

(1)一段时间后,可明显观察到实验B中铜片表面的现象是
有银白色固体析出
,反应的化学方程式是${Cu + 2AgNO_{3}\xlongequal{}Cu(NO_{3})_{2} + 2Ag}$
。(2)甲同学通过对比实验
A、C
(从A、B、C中选择)中的现象,可以得出铁和锌的金属活动性。(3)乙同学拟定用定量的方法测定金属与酸反应的速率,于是设计出实验D,该实验通过测定
相同时间内收集到的气体体积(合理答案均可)
来测出金属与酸反应的速率。(4)丙同学认为实验A~C不足以得出4种金属的活动性顺序,需要在上述实验基础上,补充实验E(X与Y能发生反应),写出E中发生反应的化学方程式:
${Fe + CuSO_{4}\xlongequal{}FeSO_{4} + Cu}$(合理答案均可)
。最终得出4种金属的活动性由强到弱的顺序为锌>铁>铜>银
。
答案:
(1)有银白色固体析出 ${Cu + 2AgNO_{3}\xlongequal{}Cu(NO_{3})_{2} + 2Ag}$ (2)A、C (3)相同时间内收集到的气体体积(合理答案均可) (4)${Fe + CuSO_{4}\xlongequal{}FeSO_{4} + Cu}$(合理答案均可) 锌>铁>铜>银
查看更多完整答案,请扫码查看


