第34页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
23.(10分)某化学小组的同学加热氯酸钾与二氧化锰的混合物制取氧气,同时得到氯化钾,并从反应剩余物中回收二氧化锰,设计模拟工艺流程如图所示。分析流程,回答下列问题:
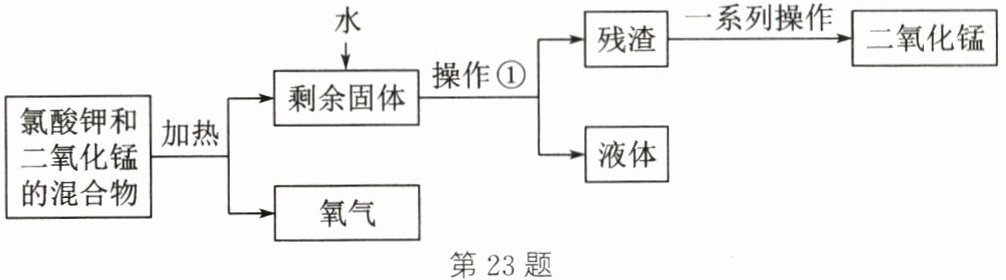
(1)制取氧气时,把氯酸钾和二氧化锰平铺在试管底部,目的是
(2)“加热”过程中发生反应的符号表达式为
(3)操作①的名称是
(4)该工艺的价值在于

(1)制取氧气时,把氯酸钾和二氧化锰平铺在试管底部,目的是
增大受热面积,有利于试剂均匀受热
。(2)“加热”过程中发生反应的符号表达式为
KClO₃$\xrightarrow[\triangle]{MnO_2}$KCl+O₂
。(3)操作①的名称是
过滤
,实验室进行该操作时,玻璃棒的作用是引流
。(4)该工艺的价值在于
回收二氧化锰,实现试剂的回收利用(或节约试剂等合理答案均可)
。
答案:
(1)增大受热面积,有利于试剂均匀受热 (2)KClO₃$\xrightarrow[\triangle]{MnO_2}$KCl+O₂ (3)过滤 引流 (4)回收二氧化锰,实现试剂的回收利用(或节约试剂等合理答案均可)
24.(9分)实验室制取气体所需的装置如图所示,请回答下列问题。
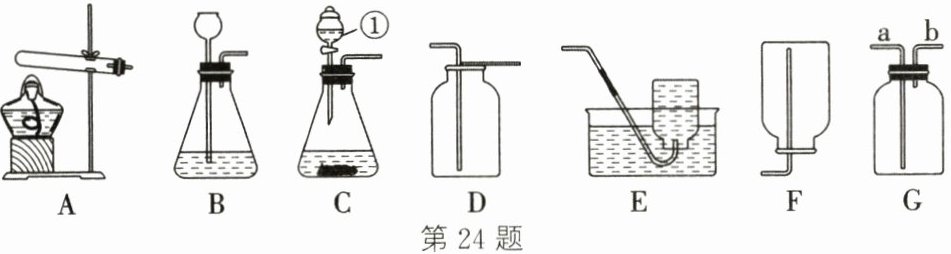
(1)写出仪器①的名称:
(2)在实验室中,用高锰酸钾制取氧气,应选择
(3)若用装置E作为收集$O_2$的装置,则
(4)硫化氢$(H_2S)$是一种密度比空气大且能溶于水的气体,实验室常用块状硫化亚铁和稀硫酸溶液在常温下反应产生。若想制取并收集$H_2S,$从图中选择的收集装置为

(1)写出仪器①的名称:
分液漏斗
。(2)在实验室中,用高锰酸钾制取氧气,应选择
A
(填字母)作为发生装置,需对该装置进行的改进措施为在试管口塞一团棉花
。若用过氧化氢溶液制取氧气,发生反应的符号表达式为H₂O₂$\xrightarrow{MnO_2}$H₂O+O₂
。(3)若用装置E作为收集$O_2$的装置,则
导管口出现连续均匀气泡
(填现象)时开始收集;若用装置G作为收集$O_2$的装置,验满时应将带火星的木条放在装置G的b
(填“a”或“b”)处,氧气已收集满的现象为带火星的木条复燃
。(4)硫化氢$(H_2S)$是一种密度比空气大且能溶于水的气体,实验室常用块状硫化亚铁和稀硫酸溶液在常温下反应产生。若想制取并收集$H_2S,$从图中选择的收集装置为
D
(填字母,在A~F中选择);与装置B相比,制备时选用装置C的优点是可以控制反应的速率
。
答案:
(1)分液漏斗 (2)A 在试管口塞一团棉花 H₂O₂$\xrightarrow{MnO_2}$H₂O+O₂ (3)导管口出现连续均匀气泡 b 带火星的木条复燃 (4)D 可以控制反应的速率 解析:
(2)高锰酸钾制取氧气的反应物是固体,反应条件是加热,应选择装置A作为发生装置,需对该装置进行的改进措施为在试管口塞一团棉花,防止加热时粉末状物质随气流进入导管。过氧化氢在二氧化锰的催化作用下分解生成水和氧气,该反应的符号表达式为H₂O₂$\xrightarrow{MnO_2}$H₂O+O₂。
(3)若用装置E作为收集氧气的装置,则应待导管口出现连续均匀气泡时才开始收集;若用装置G作为收集氧气的装置,因氧气的密度比空气的大,验满时应将带火星的木条放在装置G的b处,氧气已收集满的现象为带火星的木条复燃。
(4)硫化氢的密度比空气的大且能溶于水,应选择装置D作为收集装置,收集硫化氢气体;与装置B相比,制备时选用装置C的优点是可以控制反应的速率。
(2)高锰酸钾制取氧气的反应物是固体,反应条件是加热,应选择装置A作为发生装置,需对该装置进行的改进措施为在试管口塞一团棉花,防止加热时粉末状物质随气流进入导管。过氧化氢在二氧化锰的催化作用下分解生成水和氧气,该反应的符号表达式为H₂O₂$\xrightarrow{MnO_2}$H₂O+O₂。
(3)若用装置E作为收集氧气的装置,则应待导管口出现连续均匀气泡时才开始收集;若用装置G作为收集氧气的装置,因氧气的密度比空气的大,验满时应将带火星的木条放在装置G的b处,氧气已收集满的现象为带火星的木条复燃。
(4)硫化氢的密度比空气的大且能溶于水,应选择装置D作为收集装置,收集硫化氢气体;与装置B相比,制备时选用装置C的优点是可以控制反应的速率。
25.(11分)(2024·无锡期中)某兴趣小组的同学对铁以及含铁物质的相关现象产生了兴趣,并进行了一系列探究活动。
探究一:铁丝燃烧是否需要纯氧。取长短相同的直径为0.38 mm的铁丝,分别在$O_2$含量不同的情况下实验,现象如表。
|氧气含量|90%|70%|60%|55%|
|实验现象|燃烧剧烈,燃烧时间长,效果好|燃烧比90%弱,燃烧时间短,实验成功|燃烧比70%弱,燃烧时间更短,实验成功|难以燃烧,只是发热|
(1)在做铁丝在氧气中燃烧的实验时,为了使现象更清楚,最好用
(2)就0.38 mm铁丝而言,燃烧所需氧气的最低体积分数的范围是
探究二:对含有铁粉的“暖宝宝”进行成分及发热原理探究。
查阅资料:① 铁粉是黑色的;② 铁能与稀盐酸发生反应生成氢气与浅绿色的氯化亚铁溶液。
同学们在实验室打开一片 “暖宝宝”,取出其中黑色粉末做了下列实验。
Ⅰ. 探究黑色粉末的成分。
(3)取“暖宝宝”中的黑色粉末于试管中,加入足量的稀盐酸,观察到
(4)反应结束之后,发现仍有黑色固体残留,经过滤、洗涤、干燥,获得黑色粉末。取样,通入氧气并点燃,将产物
Ⅱ. 探究“暖宝宝”发热的原理。按图甲(夹持仪器已略去)采用湿度、氧气浓度、温度传感器收集数据,将拆除包装的“暖宝宝”倒入三颈烧瓶中密封装置,开始收集数据,观察曲线变化(图中A、B、C)。
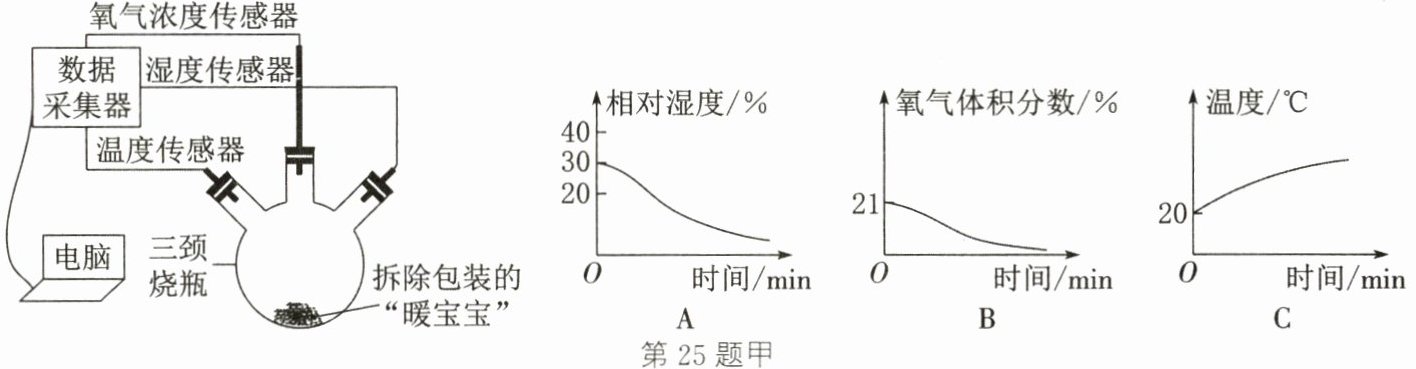
(5)从收集到的图像看,“暖宝宝”发热是因为颗粒微小的铁粉与
Ⅲ. 使用“暖宝宝”贴来测定空气中氧气的含量。实验开始前的装置如图乙(夹持仪器已略去)采用湿度、氧气浓度、温度传感器收集数据,将拆除包装的“暖宝宝”倒入三颈烧瓶中密封装置,开始收集数据,观察曲线变化(图中A、B、C)。
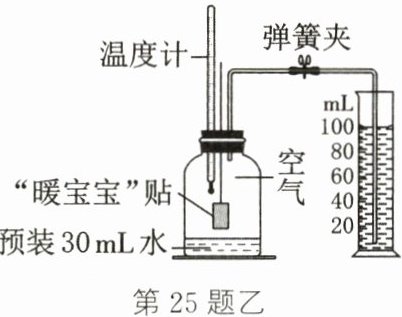
(6)实验过程中,可以观察到温度计示数
(7)冷却一段时间之后,打开弹簧夹,水从量筒中流入集气瓶(容积为250 mL),预装30mL水最后量筒内水为63 mL(铁粉生锈消耗水的体积略不计),通过计算本实验数据测得空气中氧气的体积分数约为
(8)上述结果与理论值相比,引起误差的原因可能是
探究一:铁丝燃烧是否需要纯氧。取长短相同的直径为0.38 mm的铁丝,分别在$O_2$含量不同的情况下实验,现象如表。
|氧气含量|90%|70%|60%|55%|
|实验现象|燃烧剧烈,燃烧时间长,效果好|燃烧比90%弱,燃烧时间短,实验成功|燃烧比70%弱,燃烧时间更短,实验成功|难以燃烧,只是发热|
(1)在做铁丝在氧气中燃烧的实验时,为了使现象更清楚,最好用
排水法
(填“排空气法”或“排水法”)收集氧气,理由是排水法收集的气体较为纯净
。(2)就0.38 mm铁丝而言,燃烧所需氧气的最低体积分数的范围是
55%~60%
。探究二:对含有铁粉的“暖宝宝”进行成分及发热原理探究。
查阅资料:① 铁粉是黑色的;② 铁能与稀盐酸发生反应生成氢气与浅绿色的氯化亚铁溶液。
同学们在实验室打开一片 “暖宝宝”,取出其中黑色粉末做了下列实验。
Ⅰ. 探究黑色粉末的成分。
(3)取“暖宝宝”中的黑色粉末于试管中,加入足量的稀盐酸,观察到
有气泡产生,溶液由无色变为浅绿色
,证明黑色粉末中有铁粉。(4)反应结束之后,发现仍有黑色固体残留,经过滤、洗涤、干燥,获得黑色粉末。取样,通入氧气并点燃,将产物
通入澄清石灰水,澄清石灰水变浑浊
(写出操作及现象),说明黑色粉末中还有炭粉。Ⅱ. 探究“暖宝宝”发热的原理。按图甲(夹持仪器已略去)采用湿度、氧气浓度、温度传感器收集数据,将拆除包装的“暖宝宝”倒入三颈烧瓶中密封装置,开始收集数据,观察曲线变化(图中A、B、C)。

(5)从收集到的图像看,“暖宝宝”发热是因为颗粒微小的铁粉与
氧气
和水蒸气(或水)
等物质发生反应,并放出
(填“吸收”或“放出”)热量。Ⅲ. 使用“暖宝宝”贴来测定空气中氧气的含量。实验开始前的装置如图乙(夹持仪器已略去)采用湿度、氧气浓度、温度传感器收集数据,将拆除包装的“暖宝宝”倒入三颈烧瓶中密封装置,开始收集数据,观察曲线变化(图中A、B、C)。

(6)实验过程中,可以观察到温度计示数
升高
(填“升高”或“降低”)。(7)冷却一段时间之后,打开弹簧夹,水从量筒中流入集气瓶(容积为250 mL),预装30mL水最后量筒内水为63 mL(铁粉生锈消耗水的体积略不计),通过计算本实验数据测得空气中氧气的体积分数约为
16.8%
(结果精确到0.l%)。(8)上述结果与理论值相比,引起误差的原因可能是
装置漏气(或没有等冷却到室温就打开弹簧夹等合理答案均可)
。
答案:
(1)排水法 排水法收集的气体较为纯净 (2)55%~60% (3)有气泡产生,溶液由无色变为浅绿色 (4)通入澄清石灰水,澄清石灰水变浑浊 (5)氧气 水蒸气(或水) 放出 (6)升高 (7)16.8% (8)装置漏气(或没有等冷却到室温就打开弹簧夹等合理答案均可) 解析:
(1)由现象可知,在做铁丝在氧气中燃烧的实验时,为了使现象更清楚,最好用排水法收集氧气,因为铁丝在氧气中燃烧,氧气纯度越高越好,排水法收集的气体较为纯净。
(2)根据实验数据可以看出,就0.38mm铁丝而言,在氧气含量达到55%时,铁丝难以燃烧,只是发热,而氧气含量达到60%可以燃烧,所以就0.38mm铁丝而言,燃烧所需氧气的最低体积分数的范围是55%~60%。
(3)取“暖宝宝”中的黑色粉末于试管中,加入足量的稀盐酸,根据结论黑色粉末中有铁粉,铁和稀盐酸反应生成氯化亚铁和氢气,故可观察到的实验现象为有气泡产生,溶液由无色变为浅绿色。
(4)反应结束之后,发现仍有黑色固体残留,经过滤、洗涤、干燥,获得黑色粉末。取样,通入氧气并点燃,根据结论黑色粉末中还有炭粉,则燃烧后的产物为二氧化碳,检验二氧化碳的方法为将气体通入澄清石灰水,澄清石灰水变浑浊,说明该气体是二氧化碳。
(5)探究“暖宝宝”发热的原理,通过对“暖宝宝”发热时的湿度、氧气含量和温度变化图像分析可知,“暖宝宝”发热是因为颗粒微小的铁粉与氧气、水等物质反应,并放出热量。
(6)根据上述实验可知,“暖宝宝”中颗粒微小的铁粉与氧气、水等物质反应,并放出热量,故实验过程中,可以观察到温度计示数升高。
(7)量筒内减少的水的体积即为集气瓶内消耗的氧气的体积,所以集气瓶内氧气的体积为100mL-63mL=37mL,集气瓶内空气的体积为250mL-30mL=220mL,空气中氧气的体积分数为37mL/220mL×100%≈16.8%。
(8)上述结果与理论值相比偏小,引起误差的原因可能是装置漏气,使外部气体进入瓶内;“暖宝宝”中铁粉的量不足,造成集气瓶内氧气未完全反应;未冷却至室温就打开弹簧夹,集气瓶内压强偏大或量筒读数时俯视读数,造成读数偏大等。
(1)由现象可知,在做铁丝在氧气中燃烧的实验时,为了使现象更清楚,最好用排水法收集氧气,因为铁丝在氧气中燃烧,氧气纯度越高越好,排水法收集的气体较为纯净。
(2)根据实验数据可以看出,就0.38mm铁丝而言,在氧气含量达到55%时,铁丝难以燃烧,只是发热,而氧气含量达到60%可以燃烧,所以就0.38mm铁丝而言,燃烧所需氧气的最低体积分数的范围是55%~60%。
(3)取“暖宝宝”中的黑色粉末于试管中,加入足量的稀盐酸,根据结论黑色粉末中有铁粉,铁和稀盐酸反应生成氯化亚铁和氢气,故可观察到的实验现象为有气泡产生,溶液由无色变为浅绿色。
(4)反应结束之后,发现仍有黑色固体残留,经过滤、洗涤、干燥,获得黑色粉末。取样,通入氧气并点燃,根据结论黑色粉末中还有炭粉,则燃烧后的产物为二氧化碳,检验二氧化碳的方法为将气体通入澄清石灰水,澄清石灰水变浑浊,说明该气体是二氧化碳。
(5)探究“暖宝宝”发热的原理,通过对“暖宝宝”发热时的湿度、氧气含量和温度变化图像分析可知,“暖宝宝”发热是因为颗粒微小的铁粉与氧气、水等物质反应,并放出热量。
(6)根据上述实验可知,“暖宝宝”中颗粒微小的铁粉与氧气、水等物质反应,并放出热量,故实验过程中,可以观察到温度计示数升高。
(7)量筒内减少的水的体积即为集气瓶内消耗的氧气的体积,所以集气瓶内氧气的体积为100mL-63mL=37mL,集气瓶内空气的体积为250mL-30mL=220mL,空气中氧气的体积分数为37mL/220mL×100%≈16.8%。
(8)上述结果与理论值相比偏小,引起误差的原因可能是装置漏气,使外部气体进入瓶内;“暖宝宝”中铁粉的量不足,造成集气瓶内氧气未完全反应;未冷却至室温就打开弹簧夹,集气瓶内压强偏大或量筒读数时俯视读数,造成读数偏大等。
查看更多完整答案,请扫码查看


