第130页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
19. (10 分)图甲是工业上利用黄铁矿(主要成分为$FeS_{2}$)制取硫的流程图,图乙是硫元素的价类二维图。请回答:(已知:沸腾炉中的主要反应为$4FeS_{2}+11O_{2}\frac {\underline {{高温}}}{}2Fe_{2}O_{3}+8SO_{2}$)
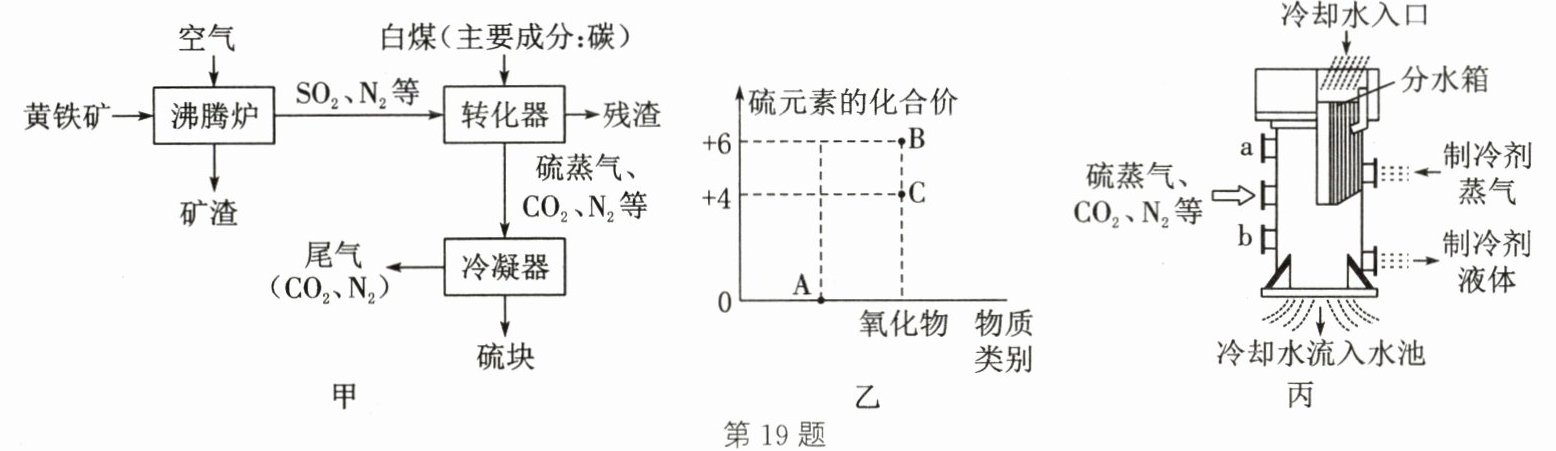
(1) 为提高黄铁矿的利用率,可对其进行______处理。
(2) 在加热条件下,转化器中发生反应的基本反应类型为______,请在图乙中用箭头表示相关物质的转化过程。
(3) 图丙为冷凝器的结构图,硫块从______(填“a”或“b”)出口产出。
(4) 沸腾炉中产生的$SO_{2}$除了用于制硫,还可用来生产硫酸,生产中的一个关键步骤是在一定条件下$SO_{2}$与氧气反应生成图乙中的 B 物质,写出反应的化学方程式:______。
(5) 流程中产生的矿渣可用于______。

(1) 为提高黄铁矿的利用率,可对其进行______处理。
(2) 在加热条件下,转化器中发生反应的基本反应类型为______,请在图乙中用箭头表示相关物质的转化过程。
(3) 图丙为冷凝器的结构图,硫块从______(填“a”或“b”)出口产出。
(4) 沸腾炉中产生的$SO_{2}$除了用于制硫,还可用来生产硫酸,生产中的一个关键步骤是在一定条件下$SO_{2}$与氧气反应生成图乙中的 B 物质,写出反应的化学方程式:______。
(5) 流程中产生的矿渣可用于______。
答案:
(1)粉碎 (2)置换反应 如图所示 (3)b (4)2SO₂ + O₂一定条件2SO₃ (5)炼铁(合理答案均可)

(1)粉碎 (2)置换反应 如图所示 (3)b (4)2SO₂ + O₂一定条件2SO₃ (5)炼铁(合理答案均可)

20. (6 分)(2025·苏州姑苏期末)用$Fe(CO)_{5}$分解制得的铁粉称为“羰基铁粉”,在国防军工领域有重要应用。以海绵铁为原料制备羰基铁粉的流程如下。
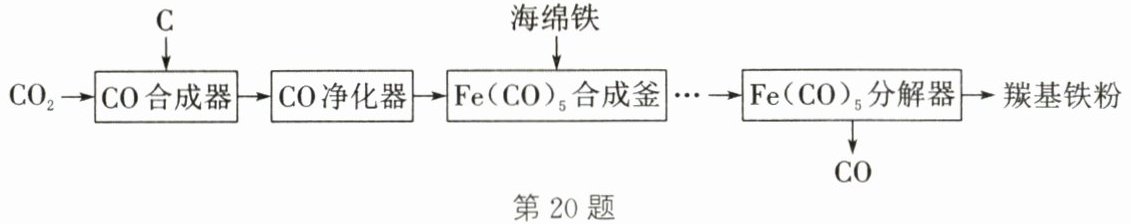
(1) “CO 合成器”中发生反应的基本反应类型为______
(2) “CO 净化器”中可利用 KOH 溶液除去$CO_{2}$。补充完整除去$CO_{2}$的化学方程式:$2KOH+CO_{2}= K_{2}CO_{3}+$______
(3) “$Fe(CO)_{5}$合成釜”中发生反应:$Fe+5CO\frac {100\sim 250^{\circ }C}{8MPa}Fe(CO)_{5}$。加热前,先向设备中通入一段时间$N_{2}$,排出设备中的空气,其目的是______
(4) “$Fe(CO)_{5}$分解器”中发生反应:$Fe(CO)_{5}\frac {200\sim 300^{\circ }C}{}Fe+5CO\uparrow $。
① 制得的铁粉平均粒度细,活性强,不耐酸。Fe 与盐酸发生反应的化学方程式为______
② “$Fe(CO)_{5}$分解器”中常添加其他气体抑制 CO 分解,来减少所得铁粉中杂质的含量。该杂质的成分可能是______
(5) 上述流程中,能循环使用的物质是______

(1) “CO 合成器”中发生反应的基本反应类型为______
化合反应
。(2) “CO 净化器”中可利用 KOH 溶液除去$CO_{2}$。补充完整除去$CO_{2}$的化学方程式:$2KOH+CO_{2}= K_{2}CO_{3}+$______
H₂O
。(3) “$Fe(CO)_{5}$合成釜”中发生反应:$Fe+5CO\frac {100\sim 250^{\circ }C}{8MPa}Fe(CO)_{5}$。加热前,先向设备中通入一段时间$N_{2}$,排出设备中的空气,其目的是______
防止加热时CO和空气混合发生爆炸、海绵铁被空气中的氧气氧化
。(4) “$Fe(CO)_{5}$分解器”中发生反应:$Fe(CO)_{5}\frac {200\sim 300^{\circ }C}{}Fe+5CO\uparrow $。
① 制得的铁粉平均粒度细,活性强,不耐酸。Fe 与盐酸发生反应的化学方程式为______
Fe + 2HCl=FeCl₂ + H₂↑
。② “$Fe(CO)_{5}$分解器”中常添加其他气体抑制 CO 分解,来减少所得铁粉中杂质的含量。该杂质的成分可能是______
C
(填化学式)。(5) 上述流程中,能循环使用的物质是______
CO
(填化学式)。
答案:
(1)化合反应 (2)H₂O (3)防止加热时CO和空气混合发生爆炸、海绵铁被空气中的氧气氧化 (4)① Fe + 2HClFeCl₂ + H₂↑ ② C (5)CO
查看更多完整答案,请扫码查看


