2025年学习与评价江苏凤凰教育出版社高中化学必修第二册苏教版河北专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年学习与评价江苏凤凰教育出版社高中化学必修第二册苏教版河北专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第28页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
3. 下列反应过程中的能量变化情况符合右图的是 ( )
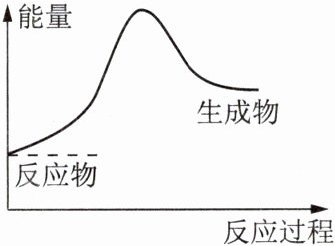
A. 氢氧化钡晶体与氯化铵晶体的反应
B. 氧化钙和水反应
C. 铝热反应
D. 一氧化碳气体的燃烧

A. 氢氧化钡晶体与氯化铵晶体的反应
B. 氧化钙和水反应
C. 铝热反应
D. 一氧化碳气体的燃烧
答案:
A
4. 在可逆反应$CO(g) + H_{2}O(g)\rightleftharpoons CO_{2}(g) + H_{2}(g)$(正反应为放热反应)中,改变下列条件,不能使$v_{正}$增大的是 ( )
A. 升高温度
B. 降低温度
C. 使用催化剂
D. 增大$CO$的浓度
A. 升高温度
B. 降低温度
C. 使用催化剂
D. 增大$CO$的浓度
答案:
B
5. 下列措施对增大反应速率明显有效的是 ( )
A. $Na$与水反应时增大水的用量
B. $Fe$与稀硫酸反应制取氢气时,改用浓硫酸
C. 在$K_{2}SO_{4}$与$BaCl_{2}$两溶液反应时,增大压强
D. 将铝片改为铝粉,做铝与氧气反应的实验
A. $Na$与水反应时增大水的用量
B. $Fe$与稀硫酸反应制取氢气时,改用浓硫酸
C. 在$K_{2}SO_{4}$与$BaCl_{2}$两溶液反应时,增大压强
D. 将铝片改为铝粉,做铝与氧气反应的实验
答案:
D
6. 茫茫黑夜中,航标灯为航海员指明了方向。航标灯的电源必须长效、稳定。我国科研工作者研制出以铝合金、$Pt - Fe$合金网为电极材料的海水电池。在这种电池中 ( )
①铝合金是正极 ②铝合金是负极 ③海水是电解质溶液 ④铝合金电极发生还原反应
A. ②③
B. ②④
C. ①③
D. ①④
①铝合金是正极 ②铝合金是负极 ③海水是电解质溶液 ④铝合金电极发生还原反应
A. ②③
B. ②④
C. ①③
D. ①④
答案:
A
7. 在一定温度下,某容积固定的密闭容器中,建立下列化学平衡:$C(s) + H_{2}O(g)\rightleftharpoons CO(g) + H_{2}(g)$。下列叙述中,不能说明上述可逆反应已达到化学平衡状态的是 ( )
A. 体系的压强不再发生变化
B. $v_{正}(CO)=v_{逆}(H_{2}O)$
C. 生成$nmol CO$的同时生成$nmol H_{2}$
D. $1mol H - H$键断裂的同时断裂$2mol H - O$键
A. 体系的压强不再发生变化
B. $v_{正}(CO)=v_{逆}(H_{2}O)$
C. 生成$nmol CO$的同时生成$nmol H_{2}$
D. $1mol H - H$键断裂的同时断裂$2mol H - O$键
答案:
C [解析]选项A,由于该反应是一个气体体积增大的反应,当体系的压强不再发生变化时,说明反应达到化学平衡状态;选项B,根据v正(CO)=v逆(H2O),可知CO的消耗量等于其生成量,说明反应达到化学平衡状态;选项C,二者表示的都是正反应,不能说明反应达到化学平衡状态;选项D,1mol H—H键断裂的同时断裂2mol H—O键,即消耗1mol H2,同时消耗了1mol H2O,可知H2的消耗量等于其生成量,说明反应达到化学平衡状态。
8. 一定条件下,可逆反应$2A\rightleftharpoons B + 3C$在下列四种状态中,处于平衡状态的是 ( )
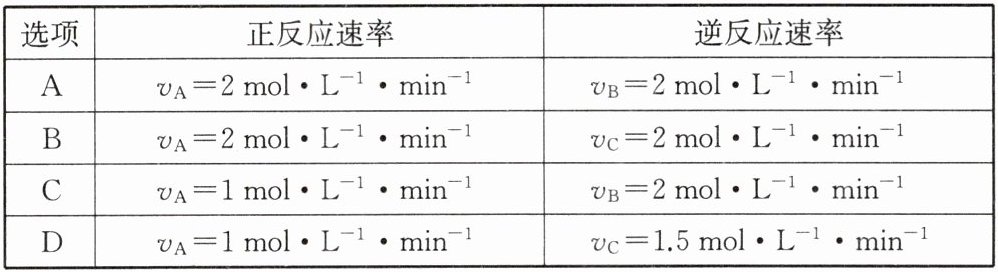

答案:
D [解析]将逆反应速率根据化学方程式统一换算成A表示的反应速率,即A的生成速率。
9. 在一定温度下,容器内某一反应中$M$、$N$的物质的量随反应时间变化的曲线如右图所示,下列表述正确的是 ( )

A. 化学方程式为$2M = N$
B. $t_{2}min$时,正、逆反应速率相等,达到平衡
C. $t_{3}min$时,正反应速率大于逆反应速率
D. $t_{1}min$时,$N$的浓度是$M$浓度的$2$倍

A. 化学方程式为$2M = N$
B. $t_{2}min$时,正、逆反应速率相等,达到平衡
C. $t_{3}min$时,正反应速率大于逆反应速率
D. $t_{1}min$时,$N$的浓度是$M$浓度的$2$倍
答案:
D [解析]由图像可知N为反应物,M为生成物,相同时间段内M、N的物质的量变化之比(与是否达平衡无关)等于M、N的化学计量数之比,即化学方程式是2N = M。t2时刻M、N的物质的量相等,但此时M、N的物质的量仍在发生变化,反应未达到平衡状态,因此正反应速率不等于逆反应速率。t3时刻及t3时刻之后,M、N的物质的量不再改变,证明已达平衡状态,此时,正、逆反应速率相等。
10. 某学生将电流表用导线与两个电极连接在一起,再将两个电极同时插入某种电解质溶液中,能观察到有电流产生的是 ( )
A. 用铜片、铅笔芯作电极插入稀硫酸中
B. 用两个铜片作电极插入硝酸银溶液中
C. 用锌片、铜片作电极插入番茄中
D. 用铜片、铁片作电极插入酒精中
A. 用铜片、铅笔芯作电极插入稀硫酸中
B. 用两个铜片作电极插入硝酸银溶液中
C. 用锌片、铜片作电极插入番茄中
D. 用铜片、铁片作电极插入酒精中
答案:
C [解析]要构成原电池,除要形成闭合回路外,还需要有两个活动性不同的电极材料,其中一个电极要能与电解质溶液发生自发的氧化还原反应。A项,铜和石墨与稀硫酸均不反应;B项,电极材料相同;D项,酒精是非电解质;C项,一些水果中含有有机酸,可作电解质溶液。
查看更多完整答案,请扫码查看


