2025年学习与评价江苏凤凰教育出版社高中化学必修第二册苏教版河北专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年学习与评价江苏凤凰教育出版社高中化学必修第二册苏教版河北专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第136页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
6.为了除去硫酸铜溶液中含有的Fe²⁺杂质,先加入合适的氧化剂使Fe²⁺氧化为Fe³⁺,下列物质中最好选用 ( )
A.H₂O₂溶液
B.KMnO₄溶液
C.氯水
D.HNO₃溶液
A.H₂O₂溶液
B.KMnO₄溶液
C.氯水
D.HNO₃溶液
答案:
A [解析]A项,H₂O₂ + 2Fe²⁺ + 2H⁺ = 2Fe³⁺ + 2H₂O,不会引入杂质;B、C和D选项,能将Fe²⁺氧化为Fe³⁺,但会引入新的杂质。
7.某工程师为了从含有FeCl₃、FeCl₂、CuCl₂的腐蚀废液中回收铜,并重新获得FeCl₃溶液,准备采用右图所示实验步骤。
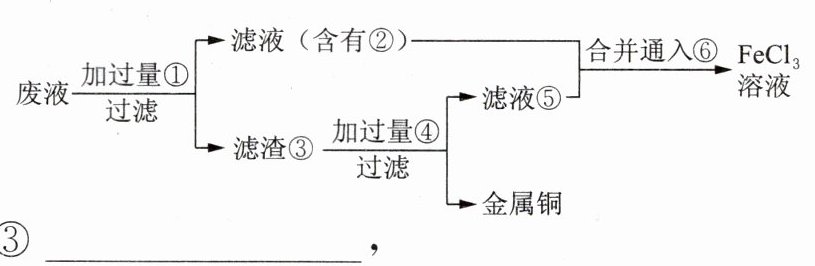
(1)请写出该步骤中加入或生成的有关物质的化学式:①________________,②________________,③________________,④________________,⑤________________,⑥________________。
(2)请写出相关反应的化学方程式。
______________________________。

(1)请写出该步骤中加入或生成的有关物质的化学式:①________________,②________________,③________________,④________________,⑤________________,⑥________________。
(2)请写出相关反应的化学方程式。
______________________________。
答案:
(1)①Fe ②FeCl₂ ③Fe和Cu ④HCl ⑤FeCl₂ ⑥Cl₂
(2)CuCl₂ + Fe = FeCl₂ + Cu,2FeCl₃ + Fe = 3FeCl₂,Fe + 2HCl = FeCl₂ + H₂↑,2FeCl₂ + Cl₂ = 2FeCl₃
(1)①Fe ②FeCl₂ ③Fe和Cu ④HCl ⑤FeCl₂ ⑥Cl₂
(2)CuCl₂ + Fe = FeCl₂ + Cu,2FeCl₃ + Fe = 3FeCl₂,Fe + 2HCl = FeCl₂ + H₂↑,2FeCl₂ + Cl₂ = 2FeCl₃
8.A、B、C、D、E分别是铁或铁的化合物,其中D是一种红褐色沉淀,其相互反应关系如右图所示,据此回答下列问题。
(1)写出A、E的化学式。
A____________,E____________。
(2)写出其中几步反应的化学方程式。
C→B:______________________________。
B→D:______________________________。
E→A:______________________________。
(3)B中加入NaOH溶液,看到的现象是______________________________。
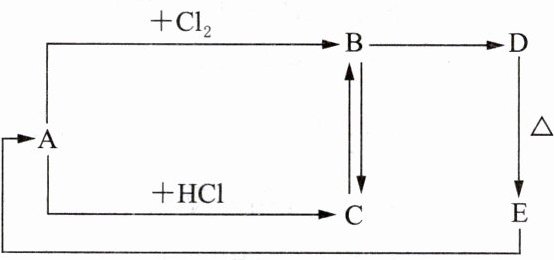
(1)写出A、E的化学式。
A____________,E____________。
(2)写出其中几步反应的化学方程式。
C→B:______________________________。
B→D:______________________________。
E→A:______________________________。
(3)B中加入NaOH溶液,看到的现象是______________________________。

答案:
(1)Fe Fe₂O₃
(2)2FeCl₂ + Cl₂ = 2FeCl₃(合理即可) FeCl₃ + 3NaOH = Fe(OH)₃↓ + 3NaCl(合理即可) Fe₂O₃ + 3CO =高温= 2Fe + 3CO₂(或Fe₂O₃ + 2Al =高温= 2Fe + Al₂O₃)
(3)生成红褐色沉淀
(1)Fe Fe₂O₃
(2)2FeCl₂ + Cl₂ = 2FeCl₃(合理即可) FeCl₃ + 3NaOH = Fe(OH)₃↓ + 3NaCl(合理即可) Fe₂O₃ + 3CO =高温= 2Fe + 3CO₂(或Fe₂O₃ + 2Al =高温= 2Fe + Al₂O₃)
(3)生成红褐色沉淀
9.用下面两种方法可以制得白色的Fe(OH)₂沉淀。
方法一:用不含Fe³⁺的FeSO₄溶液与用不含O₂的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO₄溶液时还需加入____________________。
(2)除去蒸馏水中溶解的O₂常采用________的方法。
(3)生成白色Fe(OH)₂沉淀的操作是用长滴管吸取不含O₂的NaOH溶液,插入FeSO₄溶液液面下,再挤出NaOH溶液。这样操作的理由是______________________________。
方法二:在右图所示装置中,用NaOH溶液、铁屑、稀硫酸等试剂制备。
(4)在试管I中加入的试剂是____________________。
(5)在试管II中加入的试剂是____________。
(6)为了制得白色Fe(OH)₂沉淀,在试管I和II中加入试剂,打开止水夹,塞紧塞子后的实验步骤是______________________________
(7)这样生成的Fe(OH)₂沉淀能较长时间保持白色,其理由是____________________________

方法一:用不含Fe³⁺的FeSO₄溶液与用不含O₂的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO₄溶液时还需加入____________________。
(2)除去蒸馏水中溶解的O₂常采用________的方法。
(3)生成白色Fe(OH)₂沉淀的操作是用长滴管吸取不含O₂的NaOH溶液,插入FeSO₄溶液液面下,再挤出NaOH溶液。这样操作的理由是______________________________。
方法二:在右图所示装置中,用NaOH溶液、铁屑、稀硫酸等试剂制备。
(4)在试管I中加入的试剂是____________________。
(5)在试管II中加入的试剂是____________。
(6)为了制得白色Fe(OH)₂沉淀,在试管I和II中加入试剂,打开止水夹,塞紧塞子后的实验步骤是______________________________
(7)这样生成的Fe(OH)₂沉淀能较长时间保持白色,其理由是____________________________

答案:
(1)稀硫酸、铁屑
(2)煮沸
(3)避免生成的Fe(OH)₂沉淀接触O₂而被氧化为Fe(OH)₃
(4)稀硫酸、铁屑
(5)NaOH溶液
(6)检验试管II出口处排出H₂的纯度,当排出的H₂纯净时再夹紧止水夹
(7)试管I中反应生成的H₂充满了I和II,使外界空气不易进入
(1)稀硫酸、铁屑
(2)煮沸
(3)避免生成的Fe(OH)₂沉淀接触O₂而被氧化为Fe(OH)₃
(4)稀硫酸、铁屑
(5)NaOH溶液
(6)检验试管II出口处排出H₂的纯度,当排出的H₂纯净时再夹紧止水夹
(7)试管I中反应生成的H₂充满了I和II,使外界空气不易进入
查看更多完整答案,请扫码查看


