2025年学习与评价江苏凤凰教育出版社高中化学必修第二册苏教版河北专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年学习与评价江苏凤凰教育出版社高中化学必修第二册苏教版河北专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第20页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
1.比较金属活动性。原电池中,作________的金属活动性一般比作________的金属活动性强。
答案:
负极 正极
2.改变化学反应速率。如:在Zn和稀硫酸反应时,滴加少量CuSO4溶液,则Zn置换出的铜与________构成原电池的正、负极,从而________Zn与稀硫酸反应的速率。
答案:
锌 加快
3.设计原电池。例如,把Fe + 2Fe³⁺ = 3Fe²⁺设计成原电池,可用________作负极,________作正极,____________________作电解质溶液。
答案:
Fe 铜(或石墨) FeCl3溶液
4.保护金属设备。例如,船体是钢铁材料,在海水中易被腐蚀,在船体外壳焊接上比铁__________的金属(如________),则构成以________为电极的原电池,________被消耗掉而Fe得到保护。
答案:
活泼 Zn、Fe Zn
1.下面是四个化学反应,你认为理论上不可用于设计原电池的化学反应是 ( )
A.2Al + 2NaOH + 2H₂O = 2NaAlO₂ + 3H₂↑
B.2H₂ + O₂ = 2H₂O
C.Mg₃N₂ + 6H₂O = 3Mg(OH)₂ + 2NH₃↑
D.CH₄ + 2O₂ = CO₂ + 2H₂O
A.2Al + 2NaOH + 2H₂O = 2NaAlO₂ + 3H₂↑
B.2H₂ + O₂ = 2H₂O
C.Mg₃N₂ + 6H₂O = 3Mg(OH)₂ + 2NH₃↑
D.CH₄ + 2O₂ = CO₂ + 2H₂O
答案:
C [解析]只有氧化还原反应,才能用于设计原电池。
2.为将反应2Al + 6H⁺ = 2Al³⁺ + 3H₂↑的化学能转化为电能,下列装置能达到目的的是(铝条均已除去了氧化膜) ( )
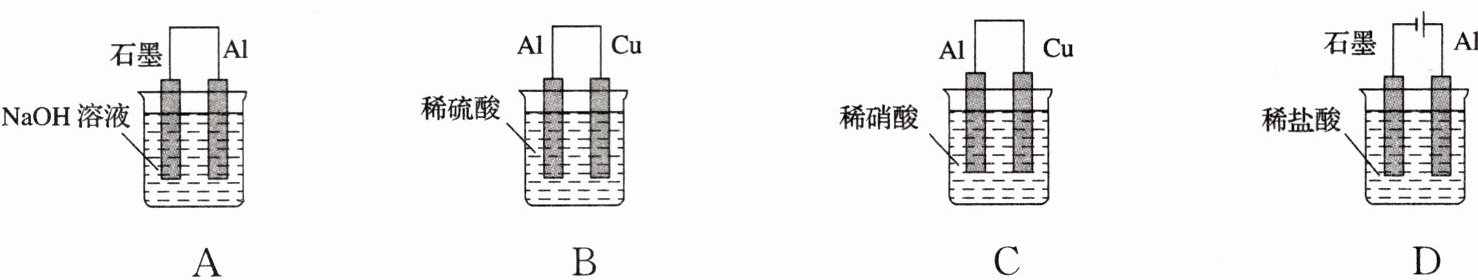

答案:
B [解析]A项为原电池,铝为负极,但总反应为2Al + 2OH⁻ + 2H₂O = 2AlO₂⁻ + 3H₂↑,不符合;C项为原电池,但硝酸是氧化性酸,总反应为Al + 4H⁺ + NO₃⁻ = Al³⁺ + NO↑ + 2H₂O,不符合;D项装置中有外接电源,不属于原电池,不符合。
3.下列关于金属材料的锈蚀说法不一,其中没有科学道理的是 ( )
A.金属接触水和空气锈蚀加快
B.改变金属的内部结构形成合金能抵御金属锈蚀
C.金属表面刷油漆可以抵御金属锈蚀
D.不断擦去铝表面的锈能抵御铝的继续锈蚀

A.金属接触水和空气锈蚀加快
B.改变金属的内部结构形成合金能抵御金属锈蚀
C.金属表面刷油漆可以抵御金属锈蚀
D.不断擦去铝表面的锈能抵御铝的继续锈蚀

答案:
D [解析]D项,不断擦去铝表面的锈,使得内部金属暴露出来,加快了铝的腐蚀而不是抵御铝的继续锈蚀,错误。
4.小颖同学用如下图所示装置研究原电池原理,下列说法错误的是 ( )
化学反应与能量变化专题6瓤
A.若将图1装置的Zn、Cu直接接触,Cu片上能看到气泡产生
B.图2装置中SO₄²⁻向Cu片移动
C.若将图2中的Zn片改为Mg片,Cu片上产生气泡的速率加快
D.图2与图3中正极生成物的质量比为1:32时,Zn片减轻的质量相等
化学反应与能量变化专题6瓤
A.若将图1装置的Zn、Cu直接接触,Cu片上能看到气泡产生
B.图2装置中SO₄²⁻向Cu片移动
C.若将图2中的Zn片改为Mg片,Cu片上产生气泡的速率加快
D.图2与图3中正极生成物的质量比为1:32时,Zn片减轻的质量相等
答案:
B [解析]Zn、Cu直接接触就能构成闭合回路而形成原电池,Cu片上可看到有气泡产生,A项正确。SO₄²⁻带负电荷,应该向负极Zn片移动,B项错误。由于Mg的失电子能力强于Zn,所以将Zn片改为Mg片后,电子转移速率加快,生成H₂的速率也加快,C项正确。假设图2中正极产生2gH₂,则转移2mol电子,消耗负极65gZn,而图3中正极析出64gCu,也转移2mol电子,消耗负极65gZn,故Zn片减轻的质量相等,D项正确。
查看更多完整答案,请扫码查看


