2025年新课程学习指导高中化学选择性必修1人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年新课程学习指导高中化学选择性必修1人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第92页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
1. 下图是学生搭建的两套装置图,下列说法正确的是 ( )
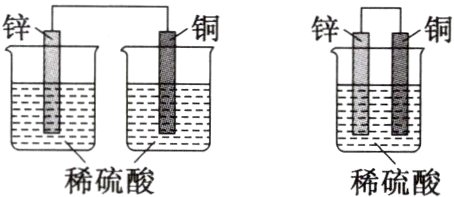
A. 两套装置都可将化学能转化为电能
B. 电池工作时锌作正极,电极反应式为$Zn - 2e^{-}=Zn^{2 + }$
C. 电池工作时,电子由锌片流出经过外电路流向铜
D. 电池工作时,$H^{ + }$移向锌片

A. 两套装置都可将化学能转化为电能
B. 电池工作时锌作正极,电极反应式为$Zn - 2e^{-}=Zn^{2 + }$
C. 电池工作时,电子由锌片流出经过外电路流向铜
D. 电池工作时,$H^{ + }$移向锌片
答案:
C
2. 将如下图所示实验装置的 K 闭合(已知:盐桥中装有琼脂凝胶,内含 KCl),下列判断正确的是 ( )
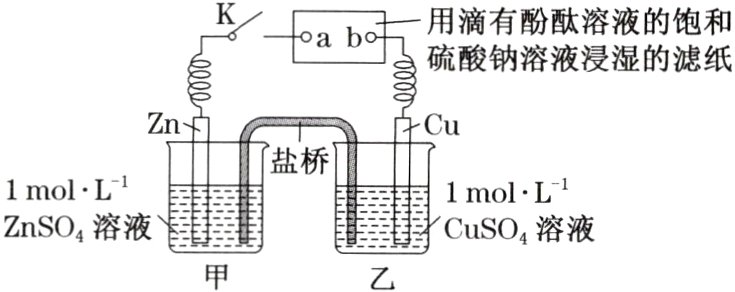
A. Cu 电极上发生还原反应
B. 电子沿$Zn→a→b→Cu$路径移动
C. 片刻后甲池中$c(SO_{4}^{2 - })$增大
D. 盐桥中的$K^{ + }$移向左边烧杯

A. Cu 电极上发生还原反应
B. 电子沿$Zn→a→b→Cu$路径移动
C. 片刻后甲池中$c(SO_{4}^{2 - })$增大
D. 盐桥中的$K^{ + }$移向左边烧杯
答案:
A
3. 能源是现代社会发展的三大支柱之一,化学在提高能源的利用率和开发新能源中起到了重要的作用。电能是现代社会中应用最广泛的二次能源。
(1)下列装置中能够实现化学能转化为电能的是________。(填字母)
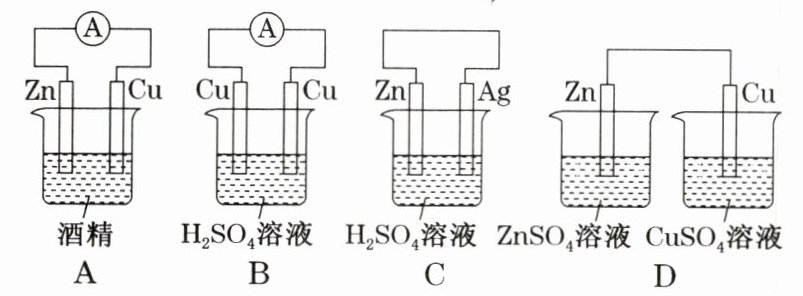
(2)写出所选装置正极反应的电极反应式:____________________。
(3)所选装置中溶液里的阴离子移向________(填电极的化学式)极。
(4)若所选装置中转移了 0.2 mol 电子,则理论上溶液增加的质量是________。
(1)下列装置中能够实现化学能转化为电能的是________。(填字母)

(2)写出所选装置正极反应的电极反应式:____________________。
(3)所选装置中溶液里的阴离子移向________(填电极的化学式)极。
(4)若所选装置中转移了 0.2 mol 电子,则理论上溶液增加的质量是________。
答案:
解析:
(1)原电池的构成条件:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发地进行氧化还原反应,C装置符合构成原电池的条件。
(2)C装置中Ag作正极,正极上氢离子得电子生成氢气,其电极反应式为$2H^{+}+2e^{-}=H_{2}\uparrow$。
(3)阴离子移向负极锌。
(4)装置中转移了0.2mol电子,根据总反应式$2H^{+}+Zn=Zn^{2+}+H_{2}\uparrow$,则理论上溶液质量增重$0.1×65g - 0.1×2g = 6.3g$。
答案:
(1)C
(2)$2H^{+}+2e^{-}=H_{2}\uparrow$
(3)Zn
(4)6.3g
(1)原电池的构成条件:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发地进行氧化还原反应,C装置符合构成原电池的条件。
(2)C装置中Ag作正极,正极上氢离子得电子生成氢气,其电极反应式为$2H^{+}+2e^{-}=H_{2}\uparrow$。
(3)阴离子移向负极锌。
(4)装置中转移了0.2mol电子,根据总反应式$2H^{+}+Zn=Zn^{2+}+H_{2}\uparrow$,则理论上溶液质量增重$0.1×65g - 0.1×2g = 6.3g$。
答案:
(1)C
(2)$2H^{+}+2e^{-}=H_{2}\uparrow$
(3)Zn
(4)6.3g
“鲲龙”AG600是我国自主研制的大型灭火/水上救援水陆两栖飞机。飞机上的多种设备都需要用到电源提供动力,常用的化学电源有哪些?它们的反应原理又是怎样的呢?


答案:
略。
(一)化学电源的分类
1.化学电源包括一次电池、二次电池和燃料电池等。________是各种化学电源的雏形。
2.电池与其他能源相比,优点有方便携带,易于维护,________________,供能稳定可靠,可以制成各种形状、大小和容量不同的电池及电池组等。
1.化学电源包括一次电池、二次电池和燃料电池等。________是各种化学电源的雏形。
2.电池与其他能源相比,优点有方便携带,易于维护,________________,供能稳定可靠,可以制成各种形状、大小和容量不同的电池及电池组等。
答案:
原电池
@@能量转化效率较高
@@能量转化效率较高
查看更多完整答案,请扫码查看


