2025年新课程学习指导高中化学选择性必修1人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年新课程学习指导高中化学选择性必修1人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第84页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
1. 为研究沉淀的生成及其转化,某小组进行如下图所示的实验。下列关于该实验的分析不正确的是 ( )

A. ①浊液中存在平衡:$\text{AgSCN}(s)\rightleftharpoons\text{Ag}^+(aq) + \text{SCN}^-(aq)$
B. ②中颜色变化说明上层清液中含有$\text{SCN}^-$
C. 该实验可以证明$\text{AgI}$比$\text{AgSCN}$更难溶
D. ③中颜色变化说明有$\text{AgI}$生成

A. ①浊液中存在平衡:$\text{AgSCN}(s)\rightleftharpoons\text{Ag}^+(aq) + \text{SCN}^-(aq)$
B. ②中颜色变化说明上层清液中含有$\text{SCN}^-$
C. 该实验可以证明$\text{AgI}$比$\text{AgSCN}$更难溶
D. ③中颜色变化说明有$\text{AgI}$生成
答案:
C ①中生成的白色沉淀为AgSCN,在溶液中存在沉淀溶解平衡,则有AgSCN(s)Ag+(aq)+SCN.(aq),故A正确;取上层清液,加入Fe(NO)3溶液,溶液变红,说明上层清液中含有SCN,故B正确;因在①中AgNO过量,余下的浊液中含有过量的Ag+,与KI反应生成黄色沉淀,不能证明AgSCN 转化为AgI,即不能证明Ag1比AgSCN更难溶,故C错误;Ag+与I结合生成AgI黄色沉淀,③中颜色变化说明有AgI 生成,故D正确。
2. 工业上采用湿法炼锌的过程中,以$\text{ZnSO}_{4}$为主要成分的浸出液中含有$\text{Fe}^{3 + }$、$\text{Fe}^{2 + }$、$\text{Cu}^{2 + }$、$\text{Cl}^{-}$等杂质,这些杂质不利于锌的电解,必须先除去。现有下列试剂可供选择:①酸性$\text{KMnO}_{4}$溶液 ②$\text{NaOH}$溶液 ③$\text{ZnO}$ ④$\text{H}_{2}\text{O}_{2}$溶液 ⑤$\text{Zn}$ ⑥$\text{Fe}$ ⑦$\text{AgNO}_{3}$ ⑧$\text{Ag}_{2}\text{SO}_{4}$。下列说法不正确的是 ( )
A. 用酸性$\text{KMnO}_{4}$溶液将$\text{Fe}^{2 + }$氧化成$\text{Fe}^{3 + }$,再转化为$\text{Fe(OH)}_{3}$沉淀除去
B. 用$\text{ZnO}$调节浸出液的酸碱性,可使某些离子形成氢氧化物沉淀
C. 在实际生产过程中,加入$\text{Ag}_{2}\text{SO}_{4}$可除去$\text{Cl}^{-}$,利用的是沉淀转化原理
D. 可以用$\text{ZnCO}_{3}$代替$\text{ZnO}$调节溶液的酸碱性
A. 用酸性$\text{KMnO}_{4}$溶液将$\text{Fe}^{2 + }$氧化成$\text{Fe}^{3 + }$,再转化为$\text{Fe(OH)}_{3}$沉淀除去
B. 用$\text{ZnO}$调节浸出液的酸碱性,可使某些离子形成氢氧化物沉淀
C. 在实际生产过程中,加入$\text{Ag}_{2}\text{SO}_{4}$可除去$\text{Cl}^{-}$,利用的是沉淀转化原理
D. 可以用$\text{ZnCO}_{3}$代替$\text{ZnO}$调节溶液的酸碱性
答案:
A 用酸性KMnO溶液氧化Fe²+时,会引入K+、Mn²+等杂质离子,这些离子在后续反应中难以除去,A项错误。生产中应使用H2O溶液氧化Fe2+,然后加入ZnO或ZnCO调节溶液的pH,使Fe³+等形成氢氧化物沉淀而除去,没有引入新的杂质,B、D项正确。AgC1比Ag2SO4更难溶,利用沉淀转化可除去C1−,C项正确。
绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉$(\text{CdS})$是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如上图所示。下列说法错误的是 ( )
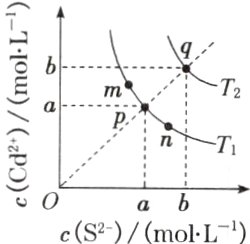
A. 图中$a$和$b$分别为$T_1$、$T_2$温度下$\text{CdS}$在水中的溶解度
B. 图中各点对应的$K_{sp}$的关系为$K_{sp}(m)=K_{sp}(n)\lt K_{sp}(p)\lt K_{sp}(q)$
C. 向$m$点的溶液中加入少量$\text{Na}_{2}\text{S}$固体,溶液组成由$m$沿$mpn$线向$p$方向移动
D. 温度降低时,$q$点的饱和溶液的组成由$q$沿$qp$线向$p$方向移动

A. 图中$a$和$b$分别为$T_1$、$T_2$温度下$\text{CdS}$在水中的溶解度
B. 图中各点对应的$K_{sp}$的关系为$K_{sp}(m)=K_{sp}(n)\lt K_{sp}(p)\lt K_{sp}(q)$
C. 向$m$点的溶液中加入少量$\text{Na}_{2}\text{S}$固体,溶液组成由$m$沿$mpn$线向$p$方向移动
D. 温度降低时,$q$点的饱和溶液的组成由$q$沿$qp$线向$p$方向移动
答案:
B A对:难溶物质的溶解度可以用物质的量浓度(摩尔浓度)表示,即题图中a、b分别表示T1、T温度下,1LCdS饱和溶液里含amol、bmolCdS。B错:Ks在一定温度下是一个常数,所以K(m)=K(n)=Kp(p)<K(q)。C对:向m点的溶液中加入NaS固体,K保持不变,S2−浓度增大,则Cd²+浓度减小,溶液组成由m沿mpn线向p方向移动。D对:温度降低时,溶解度减小,q点的饱和溶液的组成由q沿qp线向p方向移动。
查看更多完整答案,请扫码查看


