2026年新高考5年真题高中化学全一册通用版广东专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年新高考5年真题高中化学全一册通用版广东专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第54页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
3. [2025·云南卷,16T,14分]三氟甲基亚磺酸锂($M_r=140$)是我国科学家通过人工智能设计开发的一种锂离子电池补锂剂,其合成原理如下:

实验步骤如下:
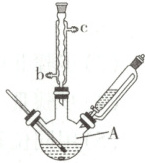
Ⅰ. 向 A 中加入 3.5 g $NaHCO_3$、5.2 g $Na_2SO_3$ 和 20.0 mL 蒸馏水,搅拌下逐滴加入 2.1 mL (3.3 g)三氟甲磺酰氯($M_r=168.5$),有气泡产生(装置如右图,夹持及加热装置省略)。80 $^{\circ} C$ 下反应 3 h 后,减压蒸除溶剂得浅黄色固体。
Ⅱ. 向上述所得固体中加入 10.0 mL 四氢呋喃(THF),充分搅拌后,加入无水 $Na_2SO_4$,振荡、抽滤、洗涤。将所得滤液减压蒸除 THF,得黏稠状固体。加入适量乙醇进行重结晶。
Ⅲ. 将所得三氟甲基亚磺酸钠和 3.0 mL THF 加入圆底烧瓶中,搅拌溶解后逐滴加入足量浓盐酸,析出白色固体。抽滤、洗涤。
Ⅳ. 将滤液转入圆底烧瓶中,加入 2.0 mL 蒸馏水和过量 LiOH。室温搅拌反应 1 h 后,减压蒸除溶剂,得粗产品。加入适量乙醇进行重结晶,得产品 1.1 g。
已知:THF 是一种有机溶剂,与水任意比互溶。
回答下列问题:
(1) 仪器 A 的名称为
(2) 步骤Ⅰ反应中有气泡产生,其主要成分为
(3) 步骤Ⅱ中第一次洗涤的目的是
(4) 步骤Ⅲ中发生反应的化学方程式为 $\mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{ONa}}} + \mathrm{HCl} \xlongequal{\mathrm{THF}} \mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{OH}}} + \mathrm{NaCl} \downarrow$,判断加入浓盐酸已足量的方法为
$\mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{ONa}}} + \mathrm{HCl} \xlongequal{\mathrm{THF}} \mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{OH}}} + \mathrm{NaCl} \downarrow$,判断加入浓盐酸已足量的方法为
(5) 步骤Ⅳ中加入蒸馏水的作用是
(6) 三氟甲基亚磺酸锂的产率为

实验步骤如下:

Ⅰ. 向 A 中加入 3.5 g $NaHCO_3$、5.2 g $Na_2SO_3$ 和 20.0 mL 蒸馏水,搅拌下逐滴加入 2.1 mL (3.3 g)三氟甲磺酰氯($M_r=168.5$),有气泡产生(装置如右图,夹持及加热装置省略)。80 $^{\circ} C$ 下反应 3 h 后,减压蒸除溶剂得浅黄色固体。
Ⅱ. 向上述所得固体中加入 10.0 mL 四氢呋喃(THF),充分搅拌后,加入无水 $Na_2SO_4$,振荡、抽滤、洗涤。将所得滤液减压蒸除 THF,得黏稠状固体。加入适量乙醇进行重结晶。
Ⅲ. 将所得三氟甲基亚磺酸钠和 3.0 mL THF 加入圆底烧瓶中,搅拌溶解后逐滴加入足量浓盐酸,析出白色固体。抽滤、洗涤。
Ⅳ. 将滤液转入圆底烧瓶中,加入 2.0 mL 蒸馏水和过量 LiOH。室温搅拌反应 1 h 后,减压蒸除溶剂,得粗产品。加入适量乙醇进行重结晶,得产品 1.1 g。
已知:THF 是一种有机溶剂,与水任意比互溶。
回答下列问题:
(1) 仪器 A 的名称为
三颈烧瓶
,冷凝管中冷却水应从b
(填“b”或“c”)口通入。(2) 步骤Ⅰ反应中有气泡产生,其主要成分为
$\mathrm{CO_2}$
。(3) 步骤Ⅱ中第一次洗涤的目的是
将吸附在滤渣上的三氟甲基亚磺酸钠尽可能全部转入滤液中,提高产率
。(4) 步骤Ⅲ中发生反应的化学方程式为
 $\mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{ONa}}} + \mathrm{HCl} \xlongequal{\mathrm{THF}} \mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{OH}}} + \mathrm{NaCl} \downarrow$
$\mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{ONa}}} + \mathrm{HCl} \xlongequal{\mathrm{THF}} \mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{OH}}} + \mathrm{NaCl} \downarrow$将混合物静置,向上层清液中滴加浓盐酸,若无白色沉淀产生,则浓盐酸已足量
。(5) 步骤Ⅳ中加入蒸馏水的作用是
增大LiOH的溶解度,使反应物充分接触,加快反应速率,使反应更充分
。(6) 三氟甲基亚磺酸锂的产率为
$\frac{1.1}{140 × 3.3} × \frac{1}{168.5} × 100\%$
(列出计算式即可)。
答案:
(1)三颈烧瓶 b
(2)$\mathrm{CO_2}$
(3)将吸附在滤渣上的三氟甲基亚磺酸钠尽可能全部转入滤液中,提高产率
(4) $\mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{ONa}}} + \mathrm{HCl} \xlongequal{\mathrm{THF}} \mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{OH}}} + \mathrm{NaCl} \downarrow$ 将混合物静置,向上层清液中滴加浓盐酸,若无白色沉淀产生,则浓盐酸已足量
$\mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{ONa}}} + \mathrm{HCl} \xlongequal{\mathrm{THF}} \mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{OH}}} + \mathrm{NaCl} \downarrow$ 将混合物静置,向上层清液中滴加浓盐酸,若无白色沉淀产生,则浓盐酸已足量
(5)增大LiOH的溶解度,使反应物充分接触,加快反应速率,使反应更充分
(6)$\frac{1.1}{140 × 3.3} × \frac{1}{168.5} × 100\%$
命题意图本题以三氟甲基亚磺酸锂的合成实验为情境,考查步骤分析、产率计算等知识,体现了“科学探究与创新意识”等化学学科核心素养。
解题思路
(2)A中$\mathrm{Na_2SO_3}$与三氟甲磺酰氯生成了三氟甲基亚磺酸钠、$\mathrm{Na_2SO_4}$和HCl,$\mathrm{NaHCO_3}$与HCl反应生成$\mathrm{CO_2}$,所以有气泡产生。
(4)将所得三氟甲基亚磺酸钠和3.0mLTHF加入圆底烧瓶中,搅拌溶解后逐滴加入足量浓盐酸,发生反应的化学方程式为 $\mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{ONa}}} + \mathrm{HCl} \xlongequal{\mathrm{THF}} \mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{OH}}} + \mathrm{NaCl} \downarrow$,析出白色固体为NaCl。
$\mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{ONa}}} + \mathrm{HCl} \xlongequal{\mathrm{THF}} \mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{OH}}} + \mathrm{NaCl} \downarrow$,析出白色固体为NaCl。
(6)三氟甲磺酰氯少量,理论上消耗的三氟甲磺酰氯与生成的三氟甲基亚磺酸锂的物质的量之比为1:1,三氟甲基磺酸锂的理论产量为$\frac{140 × 3.3}{168.5}\ g$,产率为$\frac{1.1}{140 × 3.3} × \frac{1}{168.5} × 100\%$。
(1)三颈烧瓶 b
(2)$\mathrm{CO_2}$
(3)将吸附在滤渣上的三氟甲基亚磺酸钠尽可能全部转入滤液中,提高产率
(4)
 $\mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{ONa}}} + \mathrm{HCl} \xlongequal{\mathrm{THF}} \mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{OH}}} + \mathrm{NaCl} \downarrow$ 将混合物静置,向上层清液中滴加浓盐酸,若无白色沉淀产生,则浓盐酸已足量
$\mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{ONa}}} + \mathrm{HCl} \xlongequal{\mathrm{THF}} \mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{OH}}} + \mathrm{NaCl} \downarrow$ 将混合物静置,向上层清液中滴加浓盐酸,若无白色沉淀产生,则浓盐酸已足量 (5)增大LiOH的溶解度,使反应物充分接触,加快反应速率,使反应更充分
(6)$\frac{1.1}{140 × 3.3} × \frac{1}{168.5} × 100\%$
命题意图本题以三氟甲基亚磺酸锂的合成实验为情境,考查步骤分析、产率计算等知识,体现了“科学探究与创新意识”等化学学科核心素养。
解题思路
(2)A中$\mathrm{Na_2SO_3}$与三氟甲磺酰氯生成了三氟甲基亚磺酸钠、$\mathrm{Na_2SO_4}$和HCl,$\mathrm{NaHCO_3}$与HCl反应生成$\mathrm{CO_2}$,所以有气泡产生。
(4)将所得三氟甲基亚磺酸钠和3.0mLTHF加入圆底烧瓶中,搅拌溶解后逐滴加入足量浓盐酸,发生反应的化学方程式为
 $\mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{ONa}}} + \mathrm{HCl} \xlongequal{\mathrm{THF}} \mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{OH}}} + \mathrm{NaCl} \downarrow$,析出白色固体为NaCl。
$\mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{ONa}}} + \mathrm{HCl} \xlongequal{\mathrm{THF}} \mathrm{F_3C} \overset{\mathrm{O}}{\underset{\mathrm{S}}{\mathrm{OH}}} + \mathrm{NaCl} \downarrow$,析出白色固体为NaCl。(6)三氟甲磺酰氯少量,理论上消耗的三氟甲磺酰氯与生成的三氟甲基亚磺酸锂的物质的量之比为1:1,三氟甲基磺酸锂的理论产量为$\frac{140 × 3.3}{168.5}\ g$,产率为$\frac{1.1}{140 × 3.3} × \frac{1}{168.5} × 100\%$。
查看更多完整答案,请扫码查看


