2026年新高考5年真题高中化学全一册通用版广东专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年新高考5年真题高中化学全一册通用版广东专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第100页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
10. [2023·湖南卷,13T,3分]向一恒容密闭容器中加入$1mol\ CH_4$和一定量的$H_2O$,发生反应:$CH_4(g)+H_2O(g)\rightleftharpoons CO(g)+3H_2(g)$。$CH_4$的平衡转化率按不同投料比$x[x=\frac{n(CH_4)}{n(H_2O)}]$随温度的变化曲线如图所示。下列说法错误的是 (

A.$x_1<x_2$
B.反应速率:$v_{b, 正}<v_{c, 正}$
C.点a、b、c对应的平衡常数:$K_a<K_b=K_c$
D.反应温度为$T_1$,当容器内压强不变时,反应达到平衡状态
B
)
A.$x_1<x_2$
B.反应速率:$v_{b, 正}<v_{c, 正}$
C.点a、b、c对应的平衡常数:$K_a<K_b=K_c$
D.反应温度为$T_1$,当容器内压强不变时,反应达到平衡状态
答案:
10.参考答案B
命题意图本题考查化学反应速率与平衡,意在考查考生的识图能力,体现了“变化观念与平衡思想”化学学科核心素养。
解题思路由图可知,相同温度下,投料比为$x_1$时,$ CH_4$的平衡转化率更大,又$n( CH_4)=1 mol$,说明投料比为$x_1$时,$n( H_2 O)$更大,则$x_1<x_2$,A项正确。由A项分析可知,投料比为$x_1$时,容器中反应物的量更多,反应物浓度更大,反应速率更快,则温度为$T_1$时,反应速率$v_{ b正}>v_{ c正}$,B项错误。由图可知,x一定时,温度升高,$ CH_4$的平衡转化率增大,说明平衡正向移动,则该反应为吸热反应,温度升高,平衡常数增大,故平衡常数$K_ a<K_ b=K_ c$,C项正确。该反应前后气体分子数不相等,恒温恒容时,容器内压强不再发生变化,说明反应达到平衡状态,D项正确。
命题意图本题考查化学反应速率与平衡,意在考查考生的识图能力,体现了“变化观念与平衡思想”化学学科核心素养。
解题思路由图可知,相同温度下,投料比为$x_1$时,$ CH_4$的平衡转化率更大,又$n( CH_4)=1 mol$,说明投料比为$x_1$时,$n( H_2 O)$更大,则$x_1<x_2$,A项正确。由A项分析可知,投料比为$x_1$时,容器中反应物的量更多,反应物浓度更大,反应速率更快,则温度为$T_1$时,反应速率$v_{ b正}>v_{ c正}$,B项错误。由图可知,x一定时,温度升高,$ CH_4$的平衡转化率增大,说明平衡正向移动,则该反应为吸热反应,温度升高,平衡常数增大,故平衡常数$K_ a<K_ b=K_ c$,C项正确。该反应前后气体分子数不相等,恒温恒容时,容器内压强不再发生变化,说明反应达到平衡状态,D项正确。
11. [2023·海南卷,13T,4分](双选)工业上苯乙烯的生产主要采用乙苯脱氢工艺:$C_6H_5CH_2CH_3(g)\rightleftharpoons C_6H_5CH=CH_2(g)+H_2(g)$。某条件下无催化剂存在时,该反应的正、逆反应速率$v$随时间$t$的变化关系如图所示。下列说法正确的是 (

A.曲线①表示的是逆反应的$v-t$关系
B.$t_2$时刻体系处于平衡状态
C.反应进行到$t_1$时,$Q>K$($Q$为浓度商)
D.催化剂存在时,$v_1$、$v_2$都增大
BD
)
A.曲线①表示的是逆反应的$v-t$关系
B.$t_2$时刻体系处于平衡状态
C.反应进行到$t_1$时,$Q>K$($Q$为浓度商)
D.催化剂存在时,$v_1$、$v_2$都增大
答案:
11.参考答案BD
命题意图本题以苯乙烯的制备为载体,涉及反应速率等知识,体现了“变化观念与平衡思想”化学学科核心素养。
解题思路开始反应物浓度最大,随着反应进行反应物浓度逐渐减小,则正反应速率逐渐减小,所以曲线①表示的是正反应的$v-t$关系,A项错误。由图可知,$t_2$时,正、逆反应速率相等,反应达到平衡状态,B项正确。反应进行到$t_1$时,正反应速率大于逆反应速率,反应正向进行,故$Q<K$,C项错误。催化剂能降低反应的活化能,使反应速率增大,即$v_1$、$v_2$都增大,D项正确。
命题意图本题以苯乙烯的制备为载体,涉及反应速率等知识,体现了“变化观念与平衡思想”化学学科核心素养。
解题思路开始反应物浓度最大,随着反应进行反应物浓度逐渐减小,则正反应速率逐渐减小,所以曲线①表示的是正反应的$v-t$关系,A项错误。由图可知,$t_2$时,正、逆反应速率相等,反应达到平衡状态,B项正确。反应进行到$t_1$时,正反应速率大于逆反应速率,反应正向进行,故$Q<K$,C项错误。催化剂能降低反应的活化能,使反应速率增大,即$v_1$、$v_2$都增大,D项正确。
12. [2023·河北卷,12T,3分]在恒温恒容密闭容器中充入一定量$W(g)$,发生如下反应:
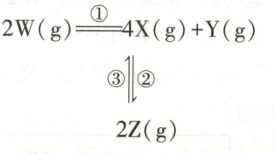
反应②和③的速率方程分别为$v_2=k_2c^2(X)$和$v_3=k_3c(Z)$,其中$k_2$、$k_3$分别为反应②和③的速率常数,反应③的活化能大于反应②。测得$W(g)$的浓度随时间的变化如表。

下列说法正确的是 (
A.$0\sim2min$内,$X$的平均反应速率为$0.080mol· L^{-1}· min^{-1}$
B.若增大容器容积,平衡时$Y$的产率增大
C.若$k_2=k_3$,平衡时$c(Z)=c(X)$
D.若升高温度,平衡时$c(Z)$减小
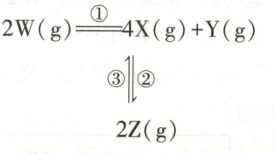
反应②和③的速率方程分别为$v_2=k_2c^2(X)$和$v_3=k_3c(Z)$,其中$k_2$、$k_3$分别为反应②和③的速率常数,反应③的活化能大于反应②。测得$W(g)$的浓度随时间的变化如表。

下列说法正确的是 (
D
)A.$0\sim2min$内,$X$的平均反应速率为$0.080mol· L^{-1}· min^{-1}$
B.若增大容器容积,平衡时$Y$的产率增大
C.若$k_2=k_3$,平衡时$c(Z)=c(X)$
D.若升高温度,平衡时$c(Z)$减小
答案:
12.参考答案D
命题意图本题考查化学反应速率与化学平衡,涉及化学反应速率的计算、化学平衡的移动等知识,体现了“变化观念与平衡思想”化学学科核心素养。
解题思路该气相反应体系中,有三个化学反应共存,反应②和反应③互为逆反应。W和Y只参与了反应①,X和Z同时参与了①②③三个反应。其中反应②为气体分子数减小的反应,反应③为气体分子数增大的反应。由表可知,$0\sim2 min$内,$\Delta c( W)=0.080 mol· L^{-1}$,反应①生成$\Delta c( X)=2\Delta c( W)=0.160 mol· L^{-1}$,X同时参与了①②③三个反应,其平均反应速率由三个反应共同决定,则$\Delta c( X)\neq0.160 mol· L^{-1}$,即$0\sim2 min$内,X的平均反应速率不为$0.080 mol· L^{-1}· min^{-1}$,A项错误。过程①是完全反应,过程②是可逆反应,改变容器的体积,只对过程②有影响,对过程①生成Y的反应无影响,平衡时Y的产率不变,B项错误。X和Z的反应是可逆反应,达平衡时,正、逆反应速率相等,即$v_2=v_3$,若$k_2=k_3$,则$c( Z)=c^2( X)$,C项错误。反应③的活化能大于反应②,则$\Delta H=$正反应活化能-逆反应活化能$<0$,即$4 X(g)\rightleftharpoons2 Z(g)\ \Delta H<0$,升高温度,平衡逆向移动,平衡时,$c( Z)$减小,D项正确。
命题意图本题考查化学反应速率与化学平衡,涉及化学反应速率的计算、化学平衡的移动等知识,体现了“变化观念与平衡思想”化学学科核心素养。
解题思路该气相反应体系中,有三个化学反应共存,反应②和反应③互为逆反应。W和Y只参与了反应①,X和Z同时参与了①②③三个反应。其中反应②为气体分子数减小的反应,反应③为气体分子数增大的反应。由表可知,$0\sim2 min$内,$\Delta c( W)=0.080 mol· L^{-1}$,反应①生成$\Delta c( X)=2\Delta c( W)=0.160 mol· L^{-1}$,X同时参与了①②③三个反应,其平均反应速率由三个反应共同决定,则$\Delta c( X)\neq0.160 mol· L^{-1}$,即$0\sim2 min$内,X的平均反应速率不为$0.080 mol· L^{-1}· min^{-1}$,A项错误。过程①是完全反应,过程②是可逆反应,改变容器的体积,只对过程②有影响,对过程①生成Y的反应无影响,平衡时Y的产率不变,B项错误。X和Z的反应是可逆反应,达平衡时,正、逆反应速率相等,即$v_2=v_3$,若$k_2=k_3$,则$c( Z)=c^2( X)$,C项错误。反应③的活化能大于反应②,则$\Delta H=$正反应活化能-逆反应活化能$<0$,即$4 X(g)\rightleftharpoons2 Z(g)\ \Delta H<0$,升高温度,平衡逆向移动,平衡时,$c( Z)$减小,D项正确。
查看更多完整答案,请扫码查看


